单细胞转录组测序与空间转录组测序已经为广大科研人员所熟知。如果说单细胞+空转是实现了从单细胞转录组水平到空间原位转录组水平的跨越,那单细胞+空转+空间代谢组则是在这个基础之上进一步升华,贯穿了同一组织转录组和代谢组的联合,甚至可以通过转录组的一些工具如SCENIC预测DNA水平TF的调控,真正从中心法则DNA到RNA到下游代谢水平去更加全面且详细的探究机制问题。
如何理解单细胞+空间转录组+空间代谢组的联合呢?以上3个组学联合的核心在于空间转录组,它起到了“承上启下”的作用。首先单细胞和空转的联合在于同为转录组水平且同一块组织(注意:样本最优选择是同一个体同一组织进行三组学分析),可以将高分辨率和空间位置同时兼得。而空间代谢组的加入也是由空转进行联系,他们连接点主要在于相同的空间位置(空转加空代一般会采用连续切片的方式,这个空间位置上“几乎”是一致的),从相同空间位置进行两个组学的穿插。我们从欧易上半年发的两篇客户文章(国内仅有2篇空转空代联合文章)进行解析多组学联合思路。

单细胞+空转+空代联合分析整体思路
1. 空间定位+空间代谢分析+转录组基因验证
第一篇是关于空转空代联合分析胃癌的客户文章[1],是通过空转结合HE染色结果锁定重点区域(可以是重点关注的病理区域也可以通过单细胞细胞类型或基因进行映射得到),然后结合空代数据进行解析。
文献解读详情,请点此查阅:
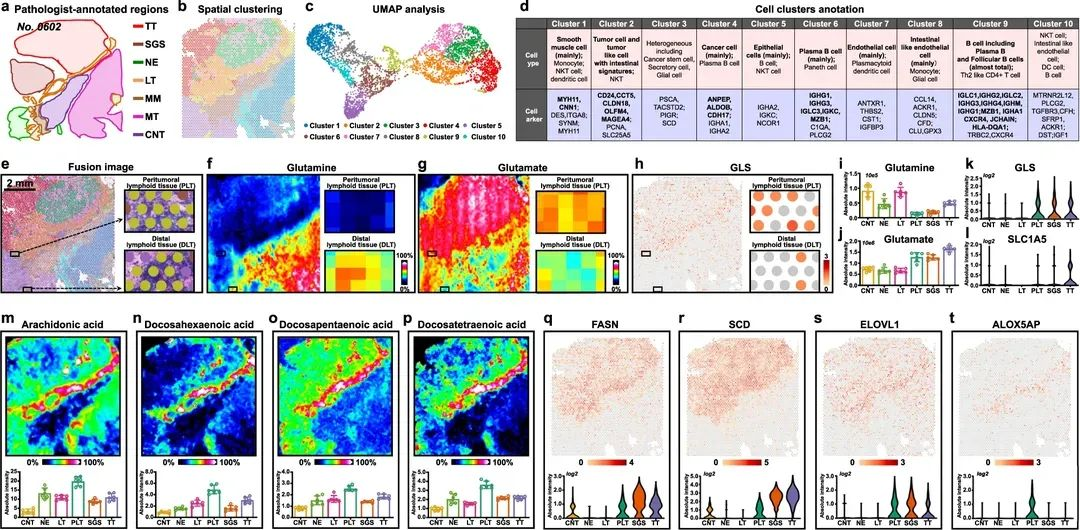
图1 胃癌肿瘤界面区域的免疫代谢重编程的成像
文章应用空间定位,通过空转数据的聚类与HE染色的匹配,发现肿瘤和邻近组织的交界处有一个明显的“界面”cluster9(图1b)。同时利用转录组信息通过细胞注释确定了cluster 9现出明显的免疫和炎症相关特征,从而寻找到该群转录特征。在cluster 9中,作者发现了两个与肿瘤边界有远近不同距离的淋巴组织DLT、PLT(图1e)。典型的通过空间转录组进行切入根据相同位置进行定位探索与代谢组学联系。
文章继续推进,通过相同位置定位空间代谢组学,而空间代谢组和空间脂质组的数据表明,谷氨酰胺的摄取和代谢在PLT中被上调了,利于几乎相同空间位置直接定位到相应代谢物的表达。同时找到相应代谢物对应基因,通过空间转录组进行反向验证,结果表明FA合成相关的FASN、SCD和ELOVL等基因在PLT中也被上调(图1q-t),再一次通过转录组学验证代谢组学结果。这些长链多不饱和脂肪酸在PLT中的上调与免疫和炎症相关cluster 9的生物学特征相吻合,也表明PLT比DLT表现出更强的炎症反应,抑制肿瘤细胞的增殖。本文即通过空间进行定位特定位置,然后根据相同位置信息锁定代谢物,最后在通过转录组学进行验证,即空转入手穿插空代。
2. 单细胞筛选基因+空间定位+空代锁定代谢物+相关性联系
另一篇单细胞+空转+空代联合分析脑损伤的客户文章[2],该文章除了要联系空转空代还要串联单细胞转录组,所以区别于上一种思路。
文献解读详情,请点此查阅:
项目文章 | Cell 子刊(IF:16.988)空间代谢组+空间转录组联合单细胞转录组揭示受损大脑中复杂的转录及代谢调剂
首先该文章利用单细胞高分辨率优势进行了细胞类型鉴定区分了不同细胞,并进行了marker基因的筛选,例如发现过氧化相关的基因如S1PR5和SEPTIN4主要在重度TBI组中表达(图2A和4C),同时通过空间转录组确定这个两个基因的空间表达区域,然后作者将这两个基因高表达的区域映射到空间代谢组上,发现,S1PR5定义的结构中PC(44:7)的丰度较高,这是一种脂质标记,被称为脂质过氧化(图2B)。相比之下,SEPTIN4定义了神经元损失区(图2D),其特点是天冬氨酸(aspartic acid)的丰度较低(图2D)。

图2 基于S1PR5和SEPTIN4空间标记基因的空间转录组和代谢物之间的联系
同时空间转录组相比单细胞转录组优势在空间,劣势在于分辨率达不到单细胞,所以如何将单细胞分别率结合到空间转录组上也是一个关键问题。本文采取的方式是addmoudlescore打分的方式,主要利用单细胞分辨率确定该样本中的该群细胞,然后锁定该细胞的marker(这种方式要比常规的经典marker更加准确更有针对性),然后将一定数量的marker基因作为一个基因集进行打分锁定空间细胞类型(图3)。当然了,除了该方法以外还有许多其他方式将单细胞细胞类型映射至空转数据上进行更好的联合,比如MIA、RCTD、SPOTlight等方式。


图3 基于单细胞数据Addmoudlescore打分鉴定空转细胞类型
上一篇文章从空转作为切入点与空代进行了联合,而本篇文章的最后一部分从另一种角度进行研究,即通过空代利用重要或者关注代谢物的表达从而锁定重点区域,然后结合空转结果进行联合探究,也就是以代谢物为入手点进行深入研究。作者在脑损伤样本中通过空间代谢组学发现了异质性的代谢物,于是作者通过对空间代谢组数据分为高PC区和低PC区,并将区域映射到空间转录组数据上(几乎相同空间位置),发现区域间的差异基因主要富集于减少的突触和神经元突起,这表明脂质过氧化可能对突触的形成和神经元的发育有影响。同时使用代谢物相关基因进行验证,比如SLC5A11、S1PR5和SEPTIN4的在重度TBI组表达量增加(图4A)。上调的基因富集在醚脂代谢和组氨酸代谢(图4B),而下调的基因富集在突触、神经元细胞体和ATP活性等通路(图4C)。而通过以上富集结果,发现这些差异基因主要富集的通路与空间代谢组结果相当一致(图4)。
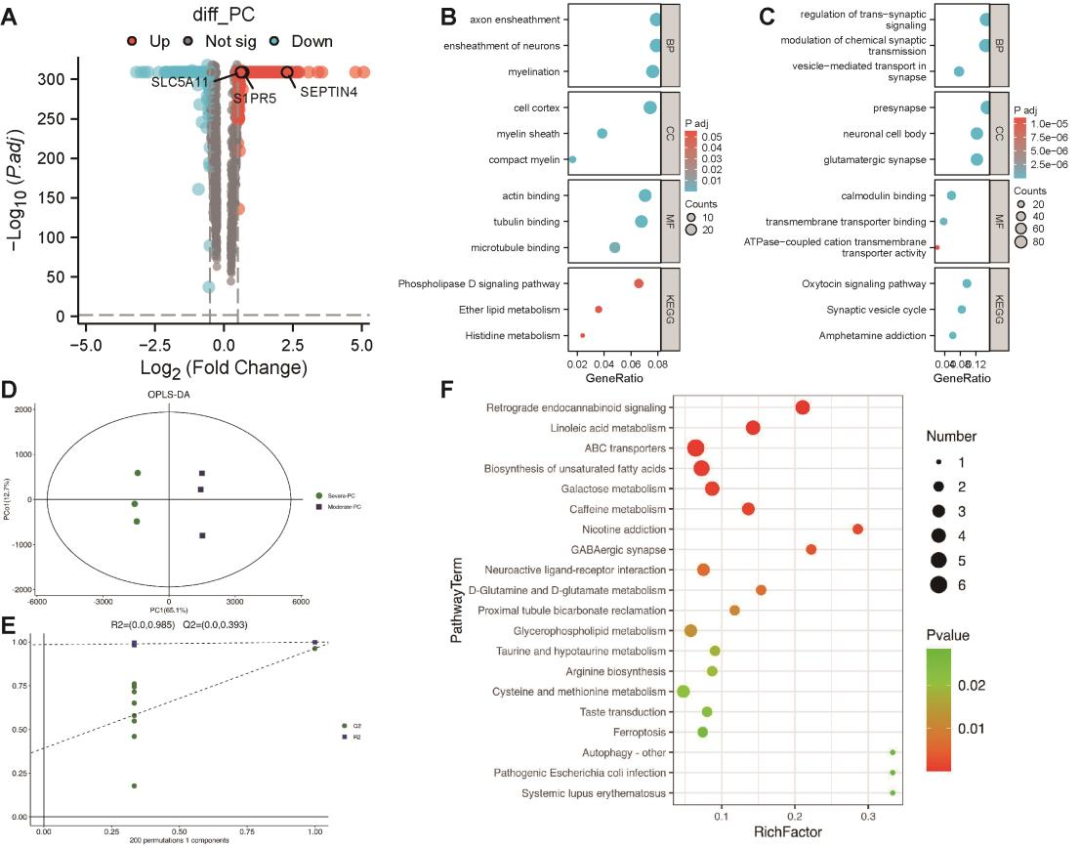
图4 脑损伤代空代与空转分析
欧易生物在时空多组学领域拥有非常丰富的经验,目前已协助客户发表单细胞转录组相关文章216篇,其中包含多篇空间转录组,空转空代联合的时空多组学文章。更多科研资料与技术咨询,欢迎添加小欧老师(微信:17317724501)或者联系欧易生物销售工程师进行详细沟通。
参考文献
1. Sun C, Wang A, Zhou Y, et al. Spatially resolved multi-omics highlights cell-specific metabolic remodeling and interactions in gastric cancer[J]. Nature Communications, 2023, 14(1): 2692.
2. Zheng P, Zhang N, Ren D, et al. Integrated spatial transcriptome and metabolism study reveals metabolic heterogeneity in human injured brain[J]. Cell Reports Medicine, 2023.






