近日,上海交通大学医学院附属第九人民医院张建军研究员、陈万涛教授为共同通讯作者,在 Molecular Therapy (IF: 11.454) 期刊发表了题为“Long noncoding RNA lnc-POP1-1 upregulated by VN1R5 promotes cisplatin resistance in head and neck squamous cell carcinoma through interaction with MCM5”的研究论文,报道了长链非编码 RNA lnc-POP1-1 在头颈鳞癌顺铂耐药中的作用及调控机制。
上海交通大学医学院附属第九人民医院蒋英英博士后和郭海艳医师为共同第一作者。文章中表达谱芯片、标记定量蛋白组 iTRAQ、蛋白质谱鉴定实验均由欧易生物协助完成。
研究背景
头颈部鳞状细胞癌(HNSCC)是口腔颌面部常见的恶性肿瘤之一。由于其高局部复发、高转移和不良预后,HNSCC 严重影响患者健康和生活质量。目前 HNSCC 主要治疗手段包括手术、放疗和化疗。其中顺铂是 HNSCC 化疗治疗的核心药物,但部分中容易出现顺铂获得性耐药性,导致 HNSCC 治疗失败。因此,研究导致顺铂耐药的关键调控因素,探索顺铂耐药的分子机制,对于开发有效的治疗方法,提高 HNSCC 疗法的临床疗效具有重要意义。
、
研究内容
本研究通过标记定量蛋白组 iTRAQ 鉴定到一个与顺铂耐药相关的蛋白 VN1R5,它在顺铂耐药的 HNSCC 细胞和组织中高表达。通过表达谱芯片的筛选,发现 lncRNA lnc-POP1-1 是 VN1R5 的下游靶标。进一步研究证实,VN1R5 通过 cAMP/PKA 途径激活转录因子 Sp1 的转录活性来调控 lnc-POP1-1 的表达。VN1R5 以 lnc-POP1-1 依赖的方式促进 HNSCC 细胞的顺铂耐药性:lnc-POP1-1 与 MCM5 蛋白结合,通过抑制 MCM5 的泛素化直接减缓了其降解,而 MCM5 蛋白促进了顺铂引起的 DNA 损伤的修复。
研究结果
1. VN1R5 促进了 HNSCC 细胞获得顺铂耐药性
针对顺铂耐药和顺铂敏感的 HNSCC 细胞系,利用标记定量蛋白组 iTRAQ 进行差异表达蛋白质筛选,结果显示 VN1R5 在顺铂耐药细胞中高表达,并通过 qRT-PCR 和 Western blotting 得以证实(图 A-C)。进一步发现,VN1R5 在顺铂耐药组织中高表达;且 VN1R5 高表达组 5 年生存率明显低于低表达组(图 D,E)。
在顺铂耐药细胞系中,VN1R5 敲除显著降低了对顺铂耐受的剂量(图 F),而 VN1R5 过表达显著提高了对顺铂耐受的剂量(图 G);利用顺铂治疗,与对照相比,VN1R5 敲除裸鼠皮下移植瘤的大小和重量明显下降(图 H-I),而过表达 VN1R5 裸鼠肿瘤的大小和重量明显升高(图 J-K)。以上结果表明 VN1R5 促进了 HNSCC 细胞获得顺铂耐药性。
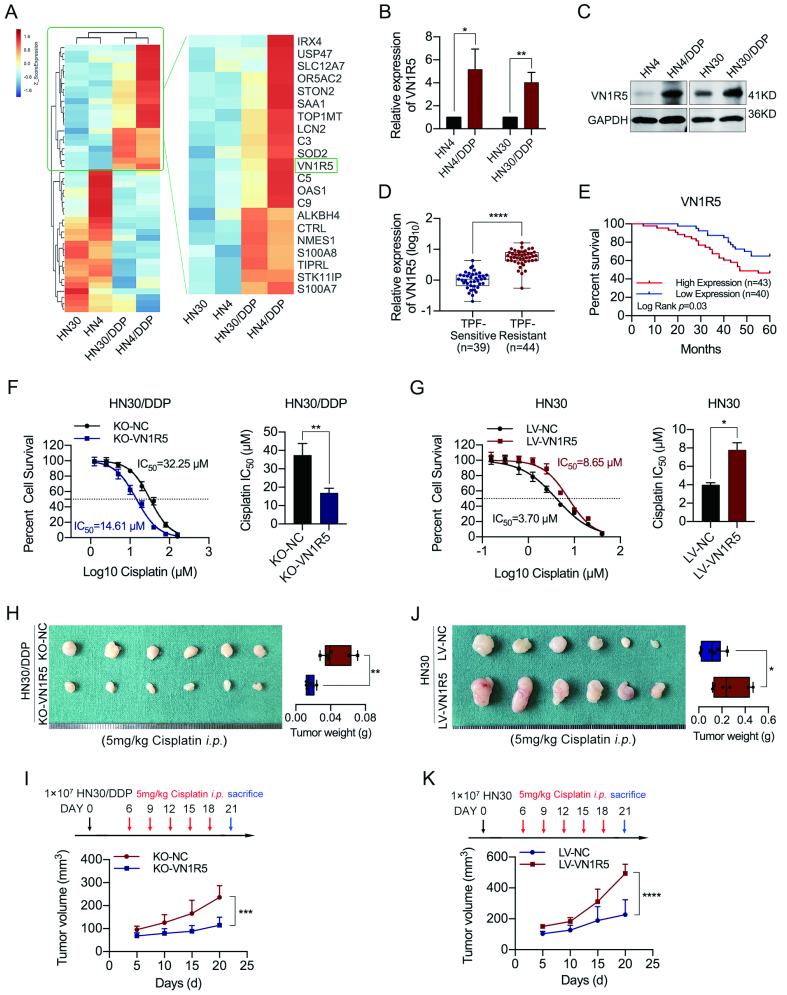
图 1 | VN1R5 上调表达与 HNSCC 细胞顺铂耐药相关
2. Lnc-POP1-1 被 VN1R5 所上调并促进 HNSCC 细胞获得顺铂耐药性
为了筛选 VN1R5 所调控的下游基因,利用表达谱芯片对 VN1R5 敲除或过表达的细胞进行检测,结果显示筛选到一个 lncRNA lnc-POP1-1(图 A, B)。
RT-PCR 显示,HNSCC 细胞和组织中 lnc-POP1-1 与 VN1R5 表达存在正相关,且 lnc-POP1-1 在 HNSCC 顺铂耐药细胞、组织中亦高表达(图 C-G)。亚细胞定位显示 lnc-POP1-1 主要分布于头颈鳞癌细胞核中(见附图)。
在顺铂耐药细胞系中,lnc-POP1-1 下调显著降低了对顺铂耐受的剂量(图 H);利用顺铂治疗,与对照相比,lnc-POP1-1 下调导致裸鼠肿瘤的大小和重量明显抑制(图 I-J)。反之,在细胞或动物实验中过表达 lnc-POP1-1,得到相反的结果(图 K-M)。以上结果表明,lnc-POP1-1 能够促进 HNSCC 细胞的顺铂耐药性。
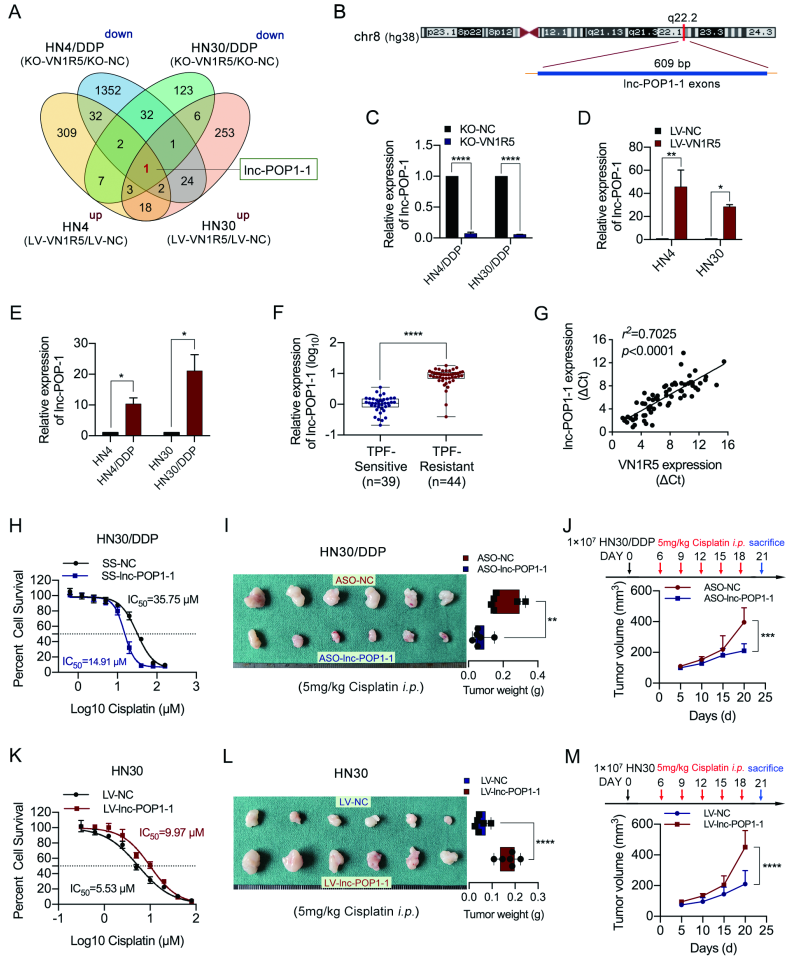
图 2 | lnc-POP1-1 表达受 VN1R5 上调并与 HNSCC 细胞顺铂耐药相关
3. lnc-POP1-1 介导 VN1R5 对 HNSCC 细胞顺铂耐药性的促进作用
在顺铂耐药细胞系中,敲除 VN1R5 或敲低 lnc-POP1-1 均可引起细胞凋亡的显著增加。在顺铂敏感的细胞系中,lnc-POP1-1 下调可以显著抑制 VN1R5 对 HNSCC 细胞的顺铂耐药性(图 A),而过表达 lnc-POP1-1 可以部分逆转 VN1R5 敲除引起的 HNSCC 细胞顺铂耐药性(图 B)。在过表达 VN1R5 的 HNSCC 细胞中敲低 lnc-POP1-1 可以显著促进细胞凋亡(图 C-D),在裸鼠皮下移植瘤模型中 lnc-POP1-1 下调可以抑制 VN1R5 过表达引起的肿瘤大小和重量的升高(图 E-F),lnc-POP1-1 过表达可以抑制 VN1R5 敲除引起的肿瘤大小和重量的下降(图 G-H)。

图 3 | lnc-POP1-1 受 VN1R5 调控影响 HNSCC 细胞的顺铂耐药性
4. VN1R5 通过激活转录因子 Sp1 的转录活性调控 lnc-POP1-1 的表达
利用转录因子预测数据库 AliBaba 和 JASPAR 来预测 lnc-POP1-1 启动子区域的转录因子并进行实验验证。进一步实验显示,敲降 Sp1 可以逆转 VN1R5 过表达所引起的 lnc-POP1-1 表达上调;反之,过表达 Sp1 可以逆转 VN1R5 敲除所引起的 lnc-POP1-1 表达下调(图 A-D)。
ChIP-PCR 结果显示,Sp1 主要结合到 lnc-POP1-1 启动子的 -2000/-1801 片段(图 E-G),并通过荧光素酶报告实验得以证实(图 H-J)。
已有研究表明 Sp1 表达受到多个信号通路的影响,进一步通过实验验证,发现经 PKA 通路抑制剂 H-89 处理、过表达或敲低 PKA可以引起 HNSCC 细胞中 lnc-POP1-1 表达的改变(见附图)。
以上结果表明 VN1R5 可以通过 cAMP/PKA 途径调节 Sp1 的转录活性以影响 lnc-POP1-1 的表达。
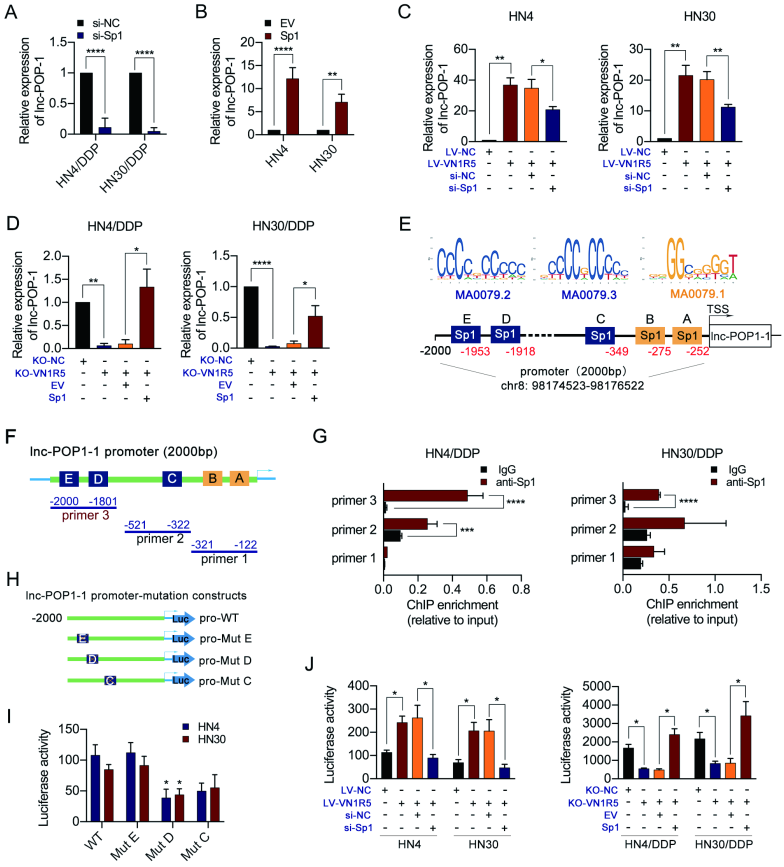
图 4 | VN1R5 通过调节 Sp1 启动子活性来调控 lnc-POP1-1 表达
5. lnc-POP1-1 促进 DNA 损伤修复且与 MCM5 结合
为进一步研究 lnc-POP1-1 参与顺铂耐药的作用机制,利用 RNA pull-down 结合蛋白质谱鉴定,结果显示与 lnc-POP1-1 结合的蛋白主要参与了 DNA 修复通路。实验也证实在 HNSCC 顺铂耐药细胞中,DNA 修复通路是活化的。
通过数据库筛选和实验验证,发现 lnc-POP1-1 可能与蛋白 MCM5 结合,western blot、RIP 实验证实了两者之间的结合(图 A-C)。与 lnc-POP1-1 一样,MCM5 也主要分布于细胞核中(图 D)。PRIdictor 预测 lnc-POP1-1与 MCM5 的可能结合位点并进行位点突变实验,发现 MCM5 第 724 位氨基酸、lnc-POP1-1 第 600-609 位核苷酸可能是两者结合位点(图 E-F)。Lnc-POP1-1 过表达可以上调 MCM5 表达并抑制细胞的 DNA 损伤,且两者结合影响细胞顺铂耐药性(图 G-J)。
以上结果表明,lnc-POP1-1 能够与MCM5 结合并参与 DNA 损伤修复。
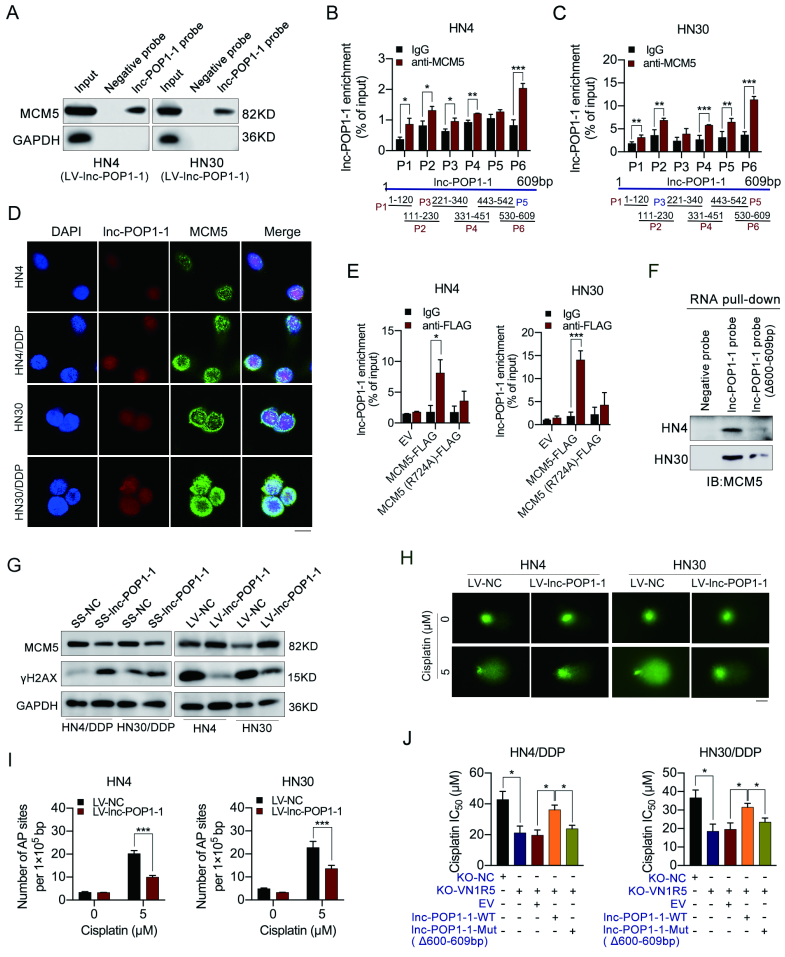
图 5 | lnc-POP1-1 与 MCM5 结合并参与 DNA 修复过程
6. lnc-POP1-1 通过降低 MCM5 的泛素化以抑制 MCM5 通过蛋白酶体途径的降解
利用蛋白质合成抑制剂 CHX 和(/或)蛋白酶体抑制剂 MG132 处理 HNSCC 细胞,结果显示,与对照相比,MG132 处理后 MCM5 蛋白更稳定(图 A),表明 MCM5 的降解部分通过蛋白酶体途径;另外,过表达 lnc-POP1-1 可以减缓 MCM5 的降解(图 B)。进一步结果显示 lnc-POP1-1 有助于 MCM5 在细胞核内的滞留(图 C-D)。同时免疫沉淀结果显示,lnc-POP1-1 敲减细胞中 MCM5 蛋白泛素化水平升高,而 lnc-POP1-1 过表达的细胞中 MCM5 蛋白泛素化水平下降(图 E-F)。
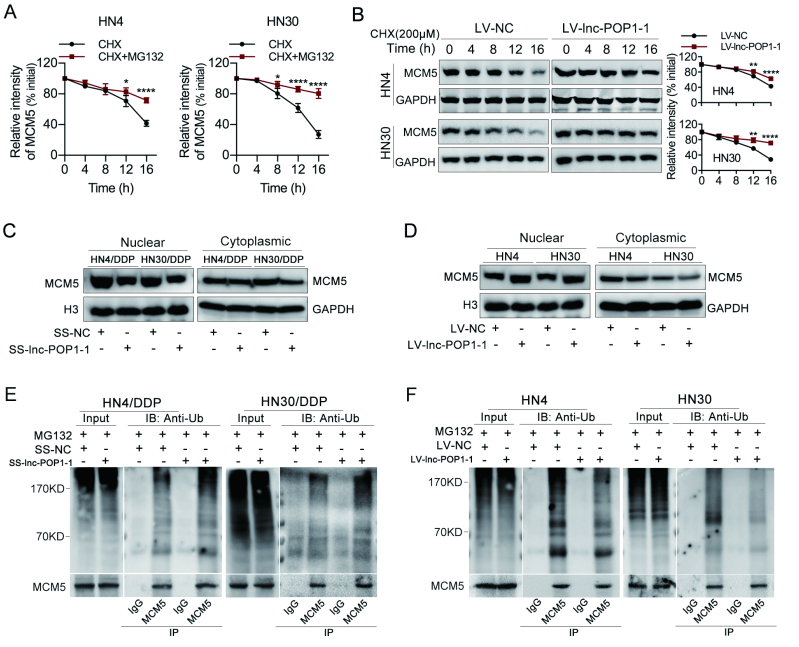
图 6 | lnc-POP1-1 与 MCM5 结合以抑制 MCM5 的泛素化降解
7. lnc-POP1-1 通过与 MCM5 相互作用影响 HNSCC 细胞顺铂耐药性
MCM5 过表达能够增强 HNSCC 细胞的顺铂耐药性(图 A),而 MCM5 敲低能够降低细胞的顺铂耐药性(图 B)。另外,lnc-POP1-1 下调能够显著阻断由 MCM5 引起的顺铂耐药性(图 C),也可以明显促进由 MCM5 敲减引起的顺铂敏感性(图 D)。
同样,体内实验显示,敲低 lnc-POP1-1 可以逆转裸鼠由 MCM5 过表达引起的肿瘤大小和重量的增加(图 E-F);另外,lnc-POP1-1 下调可以加重裸鼠由 MCM5 敲减引起的肿瘤大小和重量的降低(图 G-H)。
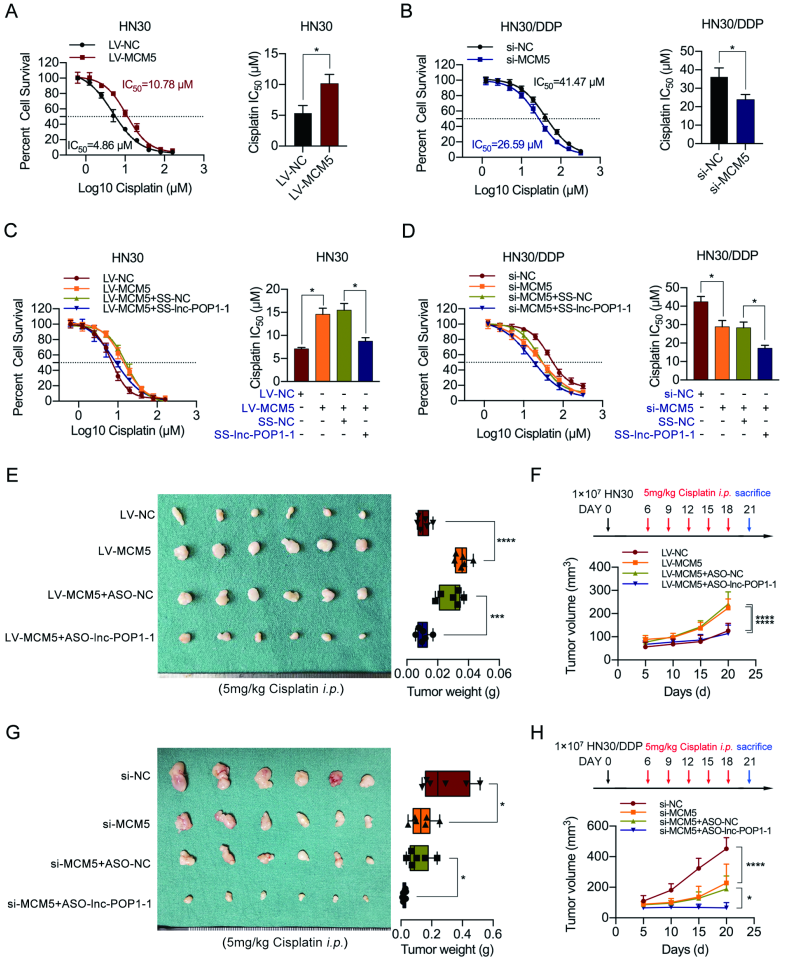
图 7 | lnc-POP1-1 通过与 MCM5 相互作用影响 HNSCC 细胞顺铂耐药性
研究结论
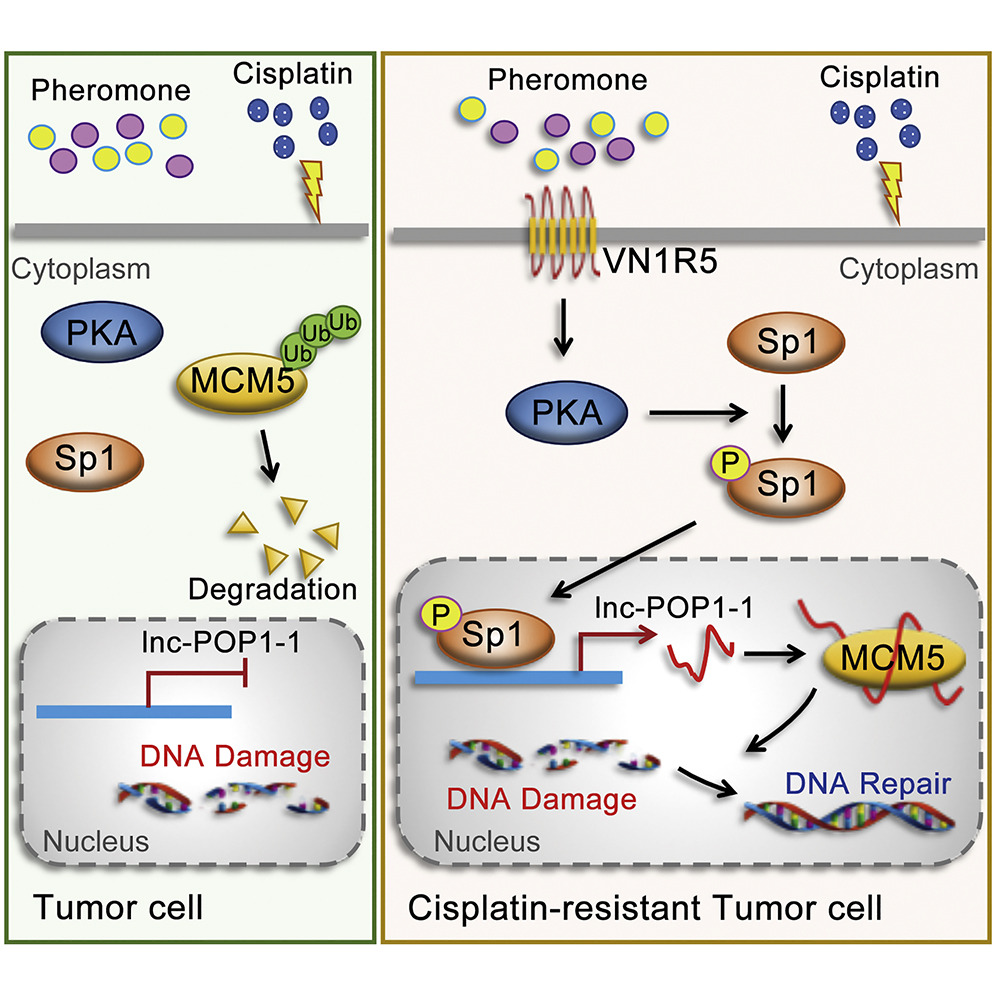
本研究揭示了头颈鳞癌中顺铂耐药新的分子机制:VN1R5 通过 cAMP/PKA 信号通路促进 转录因子 Sp1 的转录活性而上调 lnc-POP1-1 的表达;lnc-POP1-1 与 DNA 修复蛋白 MCM5 结合并减缓其泛素化降解,以参与 DNA 修复途径,从而促进了 HNSCC 细胞对顺铂的抗性。VN1R5 和 lnc-POP1-1 有望成为顺铂耐药性的预测标志物和逆转顺铂耐药性的治疗靶点,值得进一步研究。
参考文献
Jiang Y, Guo H, Tong T, et al. Long noncoding RNA lnc-POP1-1 upregulated by VN1R5 promotes cisplatin resistance in head and neck squamous cell carcinoma through interaction with MCM5. Molecular Therapy 2021; doi: 10.1016/j.ymthe.2021.06.006.
近期活动
活动一:微生物多样性测序优惠大放送

活动二:宏基因组产品钜惠来袭

精彩回顾






