前言
还在为如何联系单细胞组学、空间转录组学与湿实验发愁吗?近日,海军军医大学东方肝胆外科医院及国家肝癌科学中心分子肿瘤研究室主任苏长青教授团队与复旦大学附属华山医院肿瘤转移研究所所长钦伦秀教授团队联合在Journal for ImmunoTherapy of Cancer(IF:13.751)发表具有多重协同抗肿瘤机制的新型溶瘤腺病毒,苏英晗和黎江博士为该文第一作者,苏长青教授和钦伦秀教授为通讯作者。欧易生物提供了该项目单细胞转录组以及空间转录组测序和分析相关工作。
基本信息
材料:单细胞转录组测序:2个小鼠肿瘤样本;空间转录组测序:4个小鼠肿瘤样本
期刊:Journal for ImmunoTherapy of Cancer
发表时间:2022年5月
方法:10X Genomics scRNA-seq(欧易生物单细胞转录组测序)、10XGenomics visium(欧易生物空间转录组测序)
研究背景和研究目的
溶瘤病毒(Oncolytic virus, OV)是一类具有复制能力的肿瘤杀伤型病毒,能选择性感染肿瘤细胞,在肿瘤细胞内大量复制并最终摧毁肿瘤细胞,同时激发免疫反应,吸引更多的免疫细胞继续杀死残余的肿瘤细胞。理想情况下,在基因调控元件的调控下,改造后的溶瘤病毒在正常细胞内不具有复制的能力,因而对正常细胞不会产生影响。目前,溶瘤病毒治疗已成为肿瘤免疫治疗的一个重要分支。
然而在实际应用中,溶瘤病毒的肿瘤靶向特异性以及破坏肿瘤细胞的效应,远没有达到人们的期望值。临床上单独应用溶瘤病毒治疗肿瘤的效果也不理想。如何提高OV产品的安全性和有效性是溶瘤病毒治疗面临的最大挑战。因此,本文作者旨在设计一种新型溶瘤病毒,提高溶瘤病毒的安全性以及靶向肿瘤的有效性。
内容概述
作者构建了一种新型溶瘤病毒——OncoViron,并通过细胞学实验以及多个实体瘤细胞系的移植模型验证其抗癌效果,病毒溶瘤和转基因抗癌活性的协同作用,以及溶瘤病毒治疗与免疫治疗结合治疗的效果。结果发现,OncoViron的选择性复制介导抗癌因子的高表达,并且能够特异性靶向多种实体瘤,显著抑制癌细胞增殖。同时,在免疫缺陷小鼠、免疫健全小鼠和人源化小鼠的多种实体瘤移植模型上,OncoViron展示出自身以及联合PD-1、CAR-T出色的抗癌作用。接下来,作者通过对动物模型的移植瘤进行病理表征实验,以及通过单细胞测序和空间转录组测序分析,进一步证实OncoViron使得被感染肿瘤细胞基因表达谱发生巨大转变,OncoViron不仅招募大量淋巴细胞、NK细胞核单核巨噬细胞进入肿瘤微环境(Tumor microenvironment, TME),激活免疫细胞,尤其是T细胞的激活,而且诱导巨噬细胞向M1极化,促进更多免疫细胞因子的释放,从而实现重塑TME,协同PD-1、CAR-T进行靶向治疗。
具体研究内容解析
1、OncoViron具有高度的肿瘤选择性复制活性并介导抗癌细胞因子高效表达
作者设计并构建了一款针对广谱实体瘤的溶瘤腺病毒OncoViron,其具有在基因转录和蛋白翻译两个层次上精准控制自身在人类多种实体瘤癌细胞中的复制(图1A)。伴随病毒的复制,其携带的抗癌基因也得到了高效表达(图1B)。
通过转录组测序发现,感染了溶瘤腺病毒OncoViron的细胞系癌细胞系HCCLM3、MDA-MB-231、SGC-996,其mRNA表达谱发生了明显改变,差异表达基因(DEGs)主要富集于细胞病理生理过程中的局灶性粘附、吞噬体功能、PI3K-Akt、细胞因子-细胞因子受体相互作用和MAPK通路(图1C)。KEGG分析结果显示,细胞功能的变化和信号通路在不同肿瘤细胞类型中是相似的。
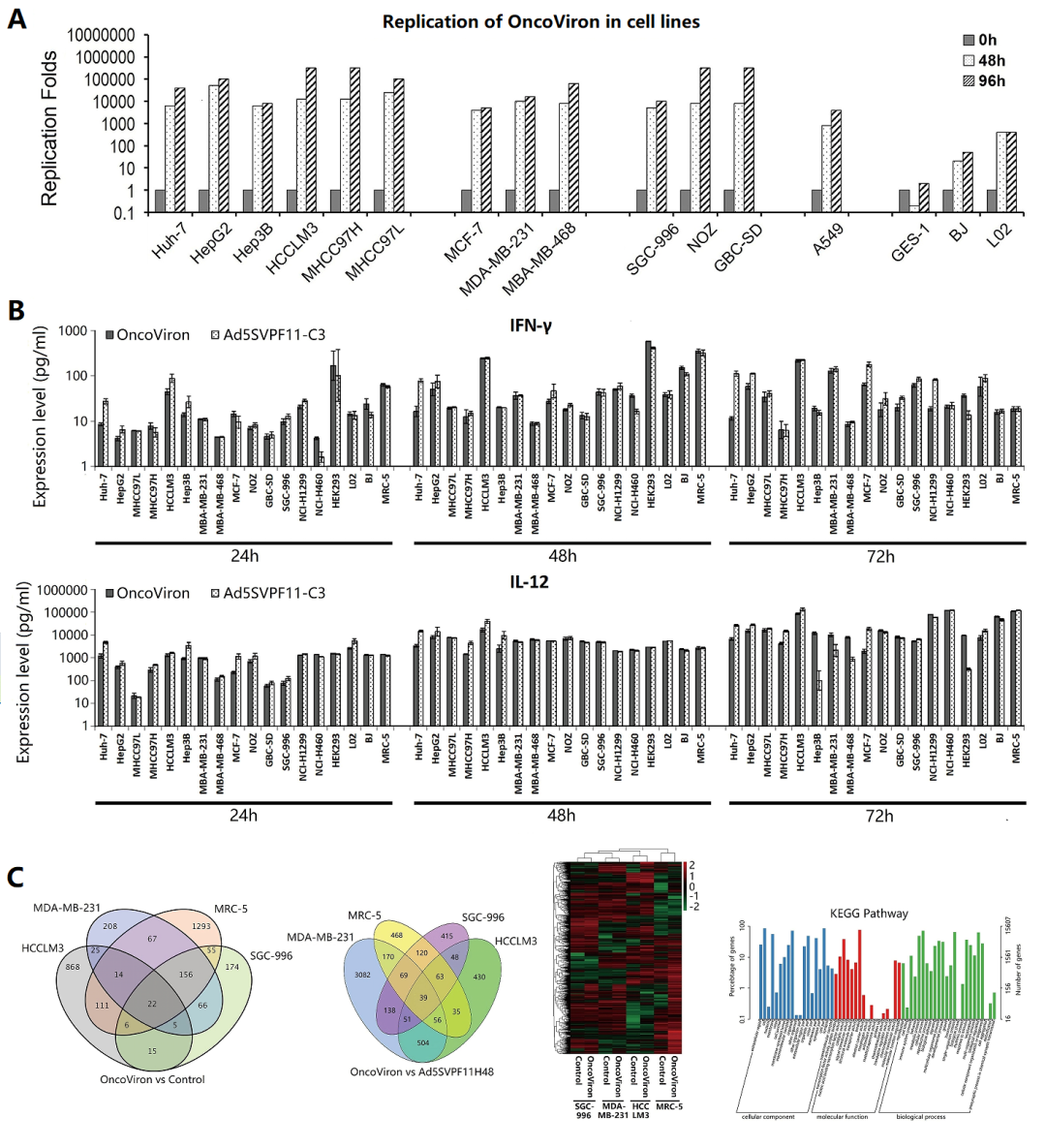
图1|OncoViron在肿瘤细胞系中的选择性复制及其抗癌细胞因子的高效表达
2、Ad5F11嵌合型Fiber和Ad5H48嵌合型Hexon增强了OncoViron的抗癌功效
柯萨奇-腺病毒受体(Coxsackievirus-adenovirus receptor, CAR)是5型腺病毒(Ad5)的受体。在Ad5基础上嵌合Ad11型腺病毒的纤毛蛋白(Fiber)形成嵌合型的溶瘤腺病毒,病毒识别的受体转换为CD46分子。流式分析发现在大多数肿瘤细胞系中CD46的表达水平明显高于CAR(图2A),因此Ad5F11的嵌合显著增强了OncoViron在大多数肿瘤细胞中的感染能力(图2B)。
由于Ad5型腺病毒在大多数人都存在既往感染,体内存在中和抗体。为防止OncoViron在治疗时被预存中和抗体拦截,作者将与Ad48型腺病毒外壳蛋白Hexon与Ad5嵌合,形成嵌合型外壳蛋白Ad5H48。通过将野生型Ad5 (wAd5)注射到BALB/C小鼠尾静脉,预免疫48小时后,再尾静脉给予嵌合型腺病毒注射,96小时后取小鼠血液、心脏、肝脏、肺、肾、脑进行检测。结果发现,经过改造的溶瘤腺病毒OncoViron能够有效避免wAd5预处理产生的中和抗体的拦截(图2C),而且肝细胞对OncoViron的粘附和感染也显著减少(图2D)。
图2|Ad5F11和Ad5H48嵌合增强OncoViron的功效
3、OncoViron诱导肿瘤选择性杀伤活性
OncoViron具有靶向癌细胞进行特异性复制并溶解癌细胞,而对正常细胞影响很小。通过实时无标记细胞分析技术(RealTime Cellular Analysis,RTCA)观测表明,OncoViron及其对照病毒对各种实体瘤癌细胞系均具有依赖于剂量效应和时间效应的细胞毒性作用(图3A)。CCK-8细胞活性实验进一步证实了OncoViron及其对照病毒对多种实体瘤细胞具有抑制作用,而对正常细胞的作用有限,需要极高的感染强度(MOI)才能发挥一定的杀伤作用 (图3B)。
图3|OncoViron在肿瘤细胞系中的选择性杀伤活性
4、OncoViron在动物移植瘤模型中发挥抗肿瘤活性
OncoViron对多种实体肿瘤表现出良好的抗癌活性。总的来说,在实体瘤裸鼠模型中,OncoViron表达抗癌细胞因子,其抗癌效果优于空载病毒,并且呈剂量依赖性。在转染人PBMCs的NCG-hILl5人源化小鼠皮下异种移植模型MDA-MB-231中,OncoViron完全抑制肿瘤生长,高剂量组的肿瘤抑制率(Tumor inhibition rate, TIR)达到97.57%。在CT26和B16肿瘤免疫健全小鼠模型中,OncoViron瘤内注射疗效是显著,甚至能在一定程度上抑制未直接治疗的对侧移植瘤的生长(图4A)。
免疫组化结果显示,经OncoViron处理的裸鼠SGC-996模型肿瘤组织出现大面积坏死,癌细胞呈E1a、Survivin、hIFN-γ呈阳性,p-AKT下调(图4B)。在B16免疫小鼠模型中,肿瘤细胞感染OncoViron后表达E1a。与对照组相比,OncoViron治疗组TME中CD3+细胞、CD4+和CD8+ T细胞数量显著增加(图4C)。结果提示,OncoViron不但能使癌细胞增殖活性下降,而且浸润性免疫细胞数量增加,说明肿瘤免疫微环境发生了明显改变。
图4|OncoViron及其对照病毒在小鼠移植瘤模型中的抗肿瘤活性
5、OncoViron联合免疫治疗协同抑制小鼠移植瘤生长
OncoViron具有协同增效免疫治疗的机制。在PBMC人源化小鼠皮下异种移植人咽部鳞状细胞癌FaDu模型中检测OncoViron的抗癌活性,低剂量的OncoViron抑瘤效果比PD-1抗体(Keytruda)更好,与Keytruda联合使用时,OncoViron的抑瘤效果明显增强(图5A)。在C57-hPD1人源化小鼠结肠癌MC38移植瘤模型中,检测OncoViron模拟品Ad5SVPF11H48-mC3(表达鼠源细胞因子)联合PD-1抗体的疗效,结果显示两者联合具有明显的协同作用(图5B)。
对MC38模型对照组(G1组)和Ad5SVPF11H48-mC3联合Keytruda组(G4组)的移植瘤组织进行单细胞测序,根据经典细胞类型标志物,共鉴定出5种细胞,Top25热图显示两组肿瘤之间基因表达谱的变化(图5C)。使用CNV评价肿瘤恶性程度,作者发现,G4组总体CNV水平低于G1组(图5D)。TME中巨噬细胞分为5个亚群,其中亚群5在G4组中显著增加(图5E)。使用巨噬细胞极化数据集针对巨噬细胞亚群进行评分结果发现,G4组中的亚群5表现出明显的M1特征(图5F)。在G4组中,肿瘤细胞高表达CCL5,而且还发现T细胞中Lag3表达显著下调(图5G)。
作者进一步针对来自对照组(G1组)、Ad5SVPF11H48-mC3 (G2组)、Keytruda (G3组)、Ad5SVPF11H48-mC3+Keytruda (G4组)的MC38肿瘤进行空间转录组测序分析。在空间层面上,降维聚类得到8个亚群。结果发现,与G1对照组相比,各治疗组亚群2显著减少,亚群6显著增加。针对趋化因子进行分析,发现G3和G4组中病毒介导的CCL5高表达,亚群6中CXCL3和CXCL5均显著上调(图5H,I)。此外,与单细胞测序结果一致,空间转录组测序分析也发现各处理组CD68+巨噬细胞数量增加,尤其是G4组中发现CD14+单核巨噬细胞局灶性聚集(图5J),CD79b+ B细胞增加,伴随基质中胶原生成减少(图5K)。促炎/抗炎以及M1/M2极化评分结果发现,G4样品促炎活性高,M1极化更明显(图5L)。
通过对CD3d+ T细胞、CD79b+ B细胞、CD14+单核巨噬细胞以及CD3d+ T细胞、CD79b+ B细胞、CD68+巨噬细胞进行共定位,发现两组细胞在OncoViron处理下均明显增加(图5M,N)。免疫组化进一步分析结果表明,在OncoViron分布并且表达mE1a的区域,肿瘤组织大面积坏死,伴有淋巴细胞、单核巨噬细胞、树突状细胞和成纤维细胞聚集,形成TME中的三级淋巴样结构,对肿瘤细胞具有原位协同杀伤作用,从而增强免疫治疗的疗效。
图5|OncoViron联合PD-1抗体对动物移植瘤模型的协同抗癌作用
作者除了观察OncoViron联合PD-1治疗效果之外,还制备了嵌合抗原受体(CAR-T细胞),探究OncoViron联合CAR-T的治疗效果。实验结果证明,在NCG小鼠的前列腺癌Du145和乳腺癌MDA-MB-231异种移植模型中,溶瘤腺病毒联合CAR-T细胞治疗显示出肿瘤抑制作用增强 (图6A,B)。在Du145模型中,OncoViron的TIR为80.19% ,OncoViron+CAR - T组的TIR为97.56%);在MDA-MB-231模型中,溶瘤腺病毒与CAR-T联合组也显示生存期延长 (图6C)。流式分析证实, OncoViron表达的细胞因子显著延长了CAR-T的生存时间,并增加了血液中CAR-T细胞的数量 (图6D,E)。免疫组化显示,OncoViron+CAR-T组移植瘤组织中,hCD45阳性CAR-T细胞浸润数量增加 (图6F,G)。研究证实,OncoViron确实能够促进CAR-T细胞的增殖和浸润,形成一种协同机制,显著提高治疗效果。
图6|OncoViron联合CAR T对动物异种移植瘤模型的协同抗癌作用
研究结论
这篇文章作者研究开发了一种新型溶瘤病毒——OncoViron,在特异性和有效性方面都取得了显著提高。OncoViron可以作为一种免疫治疗增效剂,通过单细胞转录组测序和空间转录组测序发现,其与免疫检查点抑制剂PD-1联合治疗能够显著改善TME,放大免疫治疗的效果。此外,与CAR-T治疗联合使用也能得到协同抗癌的效果。以上研究进一步拓宽了溶瘤病毒的应用范围。
参考文献
Su Y, Li J, Ji W, et al. Triple-serotype chimeric oncolytic adenovirus exerts multiple synergistic mechanisms against solid tumors. J Immunother Cancer. 2022;10(5):e004691. doi:10.1136/jitc-2022-004691

长按扫码
咨询欧易生物技术工程师
猜你想看
1、SCI ADV | 欧易单细胞测序助力解析转录因子c-Maf介导细胞代谢调控T17细胞发挥效应功能的作用机制
3、IJBM │“无惧遗忘”酵母双杂交研究阿尔茨海默症的病理机制
4、ACTA PHARM SIN B | 空间分辨代谢组学揭示糖尿病肾病中具有组织异质性的代谢重编程
原创声明:本文由欧易生物(OEBIOTECH)学术团队报道,本文著作权归文章作者所有。欢迎个人转发及分享,未经作者的允许禁止转载。






