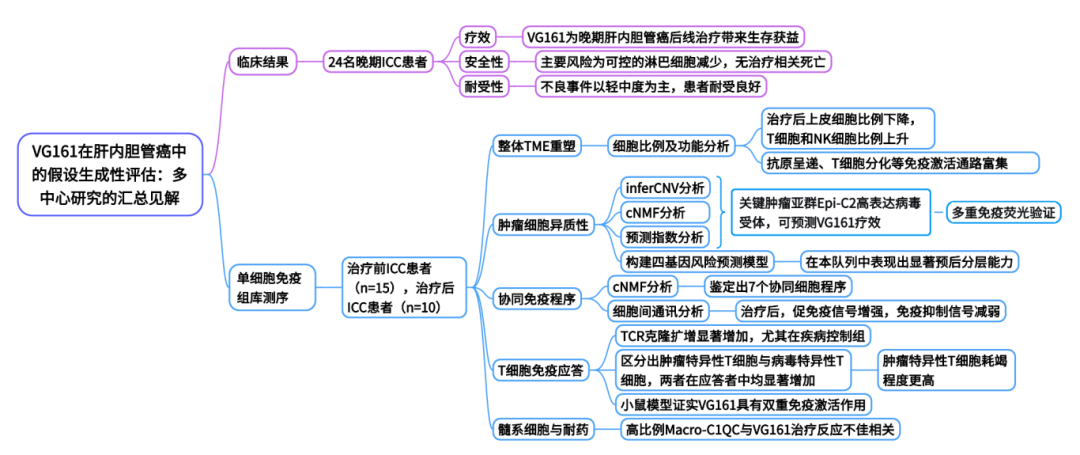
2025年9月29日,浙江大学医学院附属第一医院梁廷波团队在Gut(IF=25.8)上发表题为“Hypothesis-generating evaluation of multi-armoured oncolytic HSV-1 (VG161) in intrahepatic cholangiocarcinoma: pooled insights from multicentre studies”的研究论文。作者首次证实,新型多武装溶瘤病毒VG161能在经多线治疗的晚期肝内胆管癌患者中重塑肿瘤免疫微环境并带来生存获益,同时鉴定出可预测疗效和耐药的关键细胞亚群,为联合免疫治疗提供了新方向。本项目由欧易生物提供单细胞免疫组库测序等服务内容。

发表期刊:Gut
影响因子:25.8
涉及的欧易生物服务产品:单细胞RNA测序(scRNA-seq)和单细胞T细胞受体测序(scTCR-seq)
单细胞测序样本:
患者总数: 15名ICC患者
采样时间点: 基线(治疗前,Day 0)和治疗后(Day 7)
样本分组与数量:
基线组(Pretreatment): n = 15 (所有15名患者均提供了基线活检)
治疗后组(Post-treatment): n = 10 (这15名患者中有10名提供了治疗后第7
天的配对活检)
肝内胆管癌(ICC)是第二常见的原发性肝脏恶性肿瘤,发病率近年来显著上升,预后极差。手术切除是唯一可能的治愈手段,但多数患者确诊时已属晚期,失去手术机会。吉西他滨联合顺铂的一线化疗效果有限,客观缓解率低,且后线治疗选择匮乏,二线FOLFOX化疗疗效甚微。尽管靶向和免疫治疗为部分患者带来希望,但其适用人群狭窄。因此,开发适用于更广泛ICC患者的新型有效疗法成为迫切临床需求。溶瘤病毒疗法能选择性裂解肿瘤细胞并激活抗肿瘤免疫,为攻克这一难题提供了新思路。
本研究旨在评估新型多武装溶瘤疱疹病毒VG161在治疗晚期肝内胆管癌(ICC)中的安全性、初步疗效及免疫机制。研究汇集了两项早期临床试验数据,共纳入24例经治晚期ICC患者,通过超声引导下瘤内注射VG161进行治疗。研究采用单细胞RNA测序、T细胞受体测序等多组学技术,系统性分析治疗前后配对肿瘤活检组织的免疫微环境动态变化。重点探究VG161对肿瘤细胞的直接溶瘤作用、对T细胞/自然杀伤细胞的激活效应,并鉴定与临床反应相关的肿瘤上皮细胞亚群和免疫细胞亚群,旨在揭示其作用机制并为后续联合治疗策略提供依据。
1. 患者基线特征
在2021年6月至2023年10月期间,本次汇总分析从四个中心招募了24名晚期ICC患者。其中,20名患者来自VG161-C201研究,4名来自VG161-C102。中位随访时间为7.7个月。中位年龄为60岁,58.3%为男性。大多数患者具有ECOG体能状态。91.7%的患者患有转移性疾病,而8.3%患有不可切除的局部晚期肿瘤(图1A)。
2. 疗效结果
在22名可评估患者中,1名达到部分缓解(PR),6名达到疾病稳定(SD),客观缓解率(ORR)为4.55%,疾病控制率(DCR)为31.82%。图1B和C说明了靶病灶大小和治疗持续时间的变化。中位无进展生存期(PFS)为1.9个月,总生存期(OS)为7.8个月(图2A和B)。
一个包含11名在入组前接受CPI治疗 > 3个月(PreCPI > 3个月)的亚组表现出比那些PreCPI ≤ 3个月的患者显著更长的OS(图2D),尽管PFS未显示显著差异(图2C)。此外,一名患者的淋巴结转移灶在VG161给药后表现出显著的坏死和缩小,如增强CT和对比增强超声成像所示(图2E)。
3. 安全性和耐受性概况
在所有24名接受了至少一剂VG161的患者中进行了安全性评估。所有患者经历了至少一次治疗中出现的不良事件,其中大多数为1级或2级。≥3级不良事件发生率为79.1%,其中50%被认为与VG161相关。最常见的不良事件为短暂性淋巴细胞计数下降,无治疗相关死亡事件发生。

图1 临床特征、治疗持续时间和缓解结局
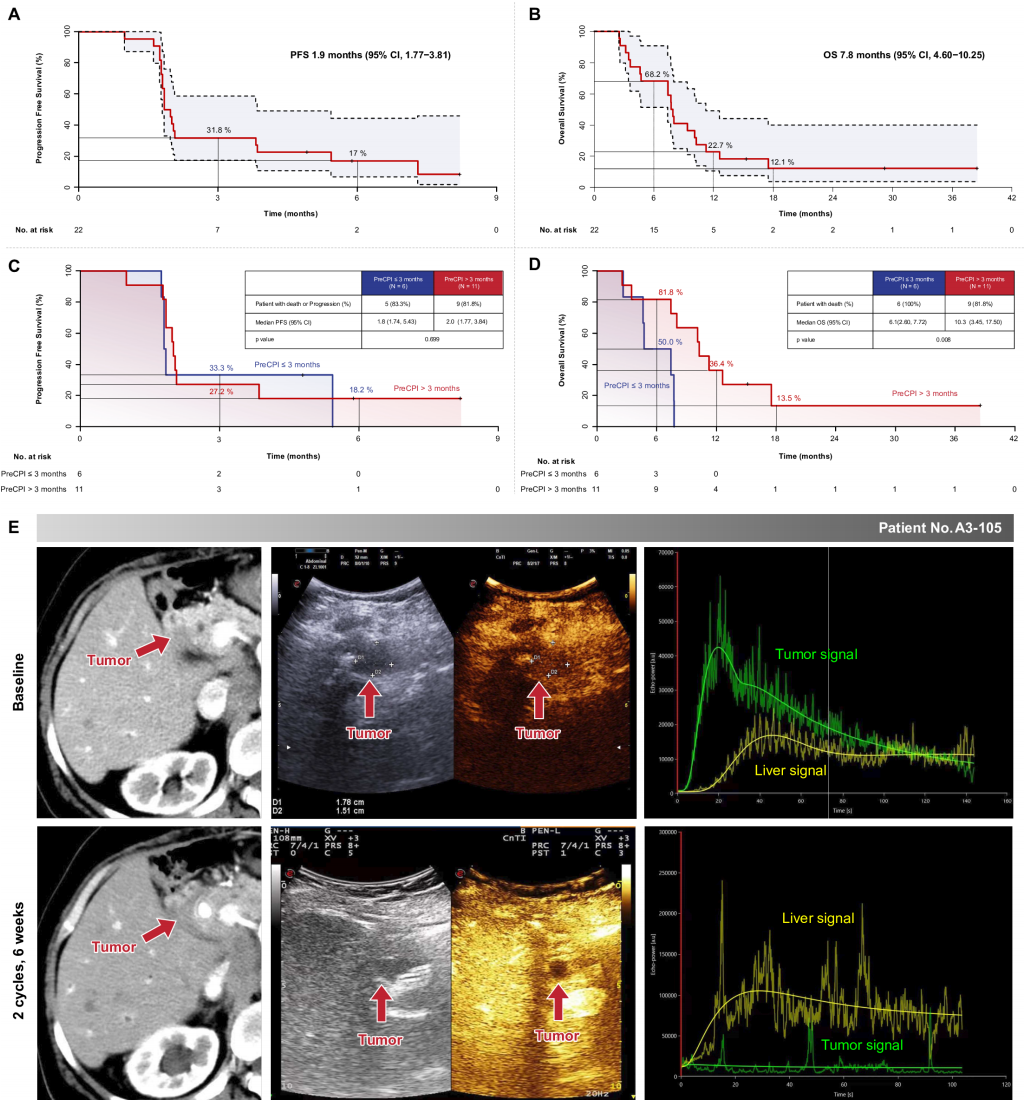
图2 患者A3-105的肿瘤缓解和生存结果评价
4. VG161诱导的ICC中TME重塑
为评估VG161诱导的ICC中肿瘤微环境(TME)变化,作者在治疗前和治疗后均收集了活检组织,用于scRNA-seq和scTCR-seq(图3A)。总计147,051个经过质量控制的细胞使用Harmony进行整合以校正批次效应,随后进行UMAP聚类和注释,识别出43个不同的细胞簇(图3B)。所有鉴定出的细胞类型均表现出独特的分子特征,凸显了其独特的性质和异质性(图3C)。值得注意的是,上皮细胞的比例下降,而T细胞和NK细胞的比例在治疗后组的组织中显著增加(图3D–F)。此外,抗原加工与呈递、T细胞分化以及病毒感染通路均在治疗后组中富集,表明治疗后存在免疫细胞激活状态。
在临床层面,疾病控制(DC)组表现出比疾病进展(PD)组更低的治疗后髓系细胞水平。预测模型显示:基线高髓系细胞水平提示疗效不佳,而治疗后B细胞增加则与良好预后相关。细胞因子动态显示IFN-γ短暂峰值证实免疫激活,而IL-6/TNF-α的异质性反应则体现个体化免疫调节特征。
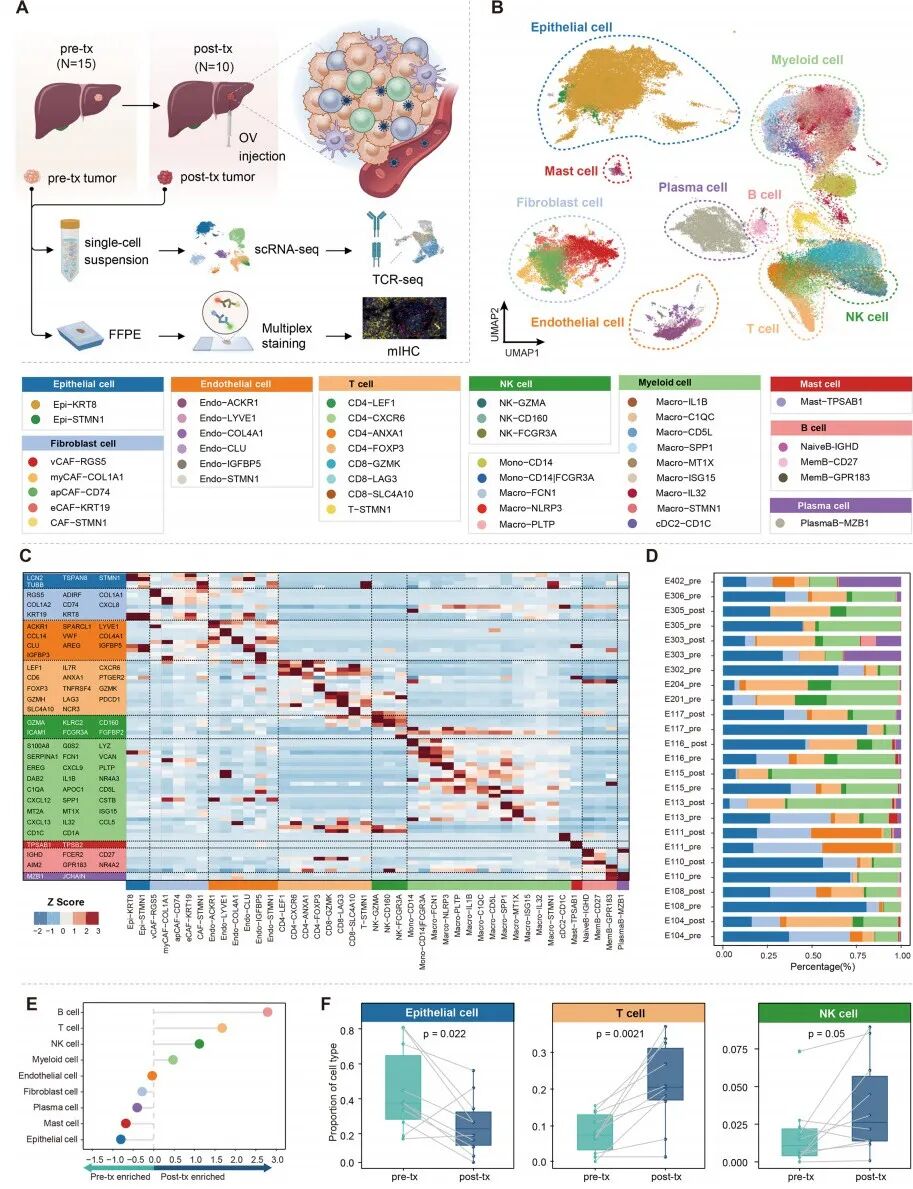
图3 VG161治疗期间ICC患者的动态单细胞景观
5. 对VG161的异质性肿瘤反应
VG161感染并在肿瘤细胞内复制的特性影响了相应的治疗反应。通过单细胞RNA测序的拷贝数变异分析鉴定的肿瘤细胞,在不同患者间显示出显著的异质性(图4A)。共识性非负矩阵分解识别出四个上皮细胞簇,从Epi-C1到Epi-C4(图4B),每个簇具有不同的分子谱。预测指数(Pi)分析显示,较高的Epi-C2基线水平与对VG161治疗的更佳反应相关(图4C)。此外,在治疗后组中,记忆性B细胞-CD27、初始B细胞-IGHD、浆细胞-MZB1和CD8-GZMK的细胞比例与Epi-C2相关(图4D)。在治疗后组中,Epi-C2表现出与免疫细胞,特别是B细胞和T细胞的相互作用增加(图4E)。而且,在疾病控制组的Epi-C2细胞中,Nectin2和TNFRSF14(HVEM)表达上调,这表明具有高水平Epi-C2基线水平的患者可能有更好的机会从VG161治疗中获益(图4F)。多重免疫荧光证实了HSV-1与肿瘤细胞的共定位,支持了VG161的肿瘤选择性趋向性(图4G)。
基于疾病控制组与进展组的肿瘤细胞表达谱差异,研究构建了四基因(HDGF、SNORC、TNFRSF21、CALM2)风险预测模型(图4H、I)。该模型在本队列中表现出显著预后分层能力:低风险组生存率显著优于高风险组,且时间依赖性ROC曲线证实其在3-15个月内具有持续预测效能。但在TCGA胆管癌队列中未验证成功,提示其特异性需进一步确认。

图4 VG161治疗对肿瘤细胞簇反应性和疗效的预测
6. VG161应答中的协同免疫程序
与治疗前相比,治疗后组在细胞亚群间表现出更强的相关性:免疫细胞与基质细胞呈现明显的负相关,而T细胞与巨噬细胞则呈现正相关(图5A)。这些发现表明,在VG161治疗后,免疫细胞程序可能表现出协同相互作用。
通过一致性非负矩阵分解,作者在肿瘤微环境中识别出七个对VG161治疗产生应答的协同细胞程序(NMF1-7)(图5B)。其中,NMF1程序包含Epi-C1、Epi-C4和Macro-CD5L,被归类为肿瘤发生程序;NMF4程序富含CD8-GZMK、MemB-CD27、PlasmaB-MZB1和Epi-C2,被表征为肿瘤应答程序;NMF7程序作为免疫抑制程序,包含了CD8-LAG3、CD4-FOXP3、Macro-C1QC和Macro-SPP1等关键抑制性细胞群体。
在治疗后组中,NMF2程序的比例呈现下降趋势,而NMF3和NMF7程序的比例则显示增加(图5C)。单细胞配体-受体相互作用分析显示,治疗后细胞间通讯网络发生显著重塑:NMF4程序中的促免疫原性信号传导增强,而NMF7程序中的免疫抑制性串扰减弱(图5D)。
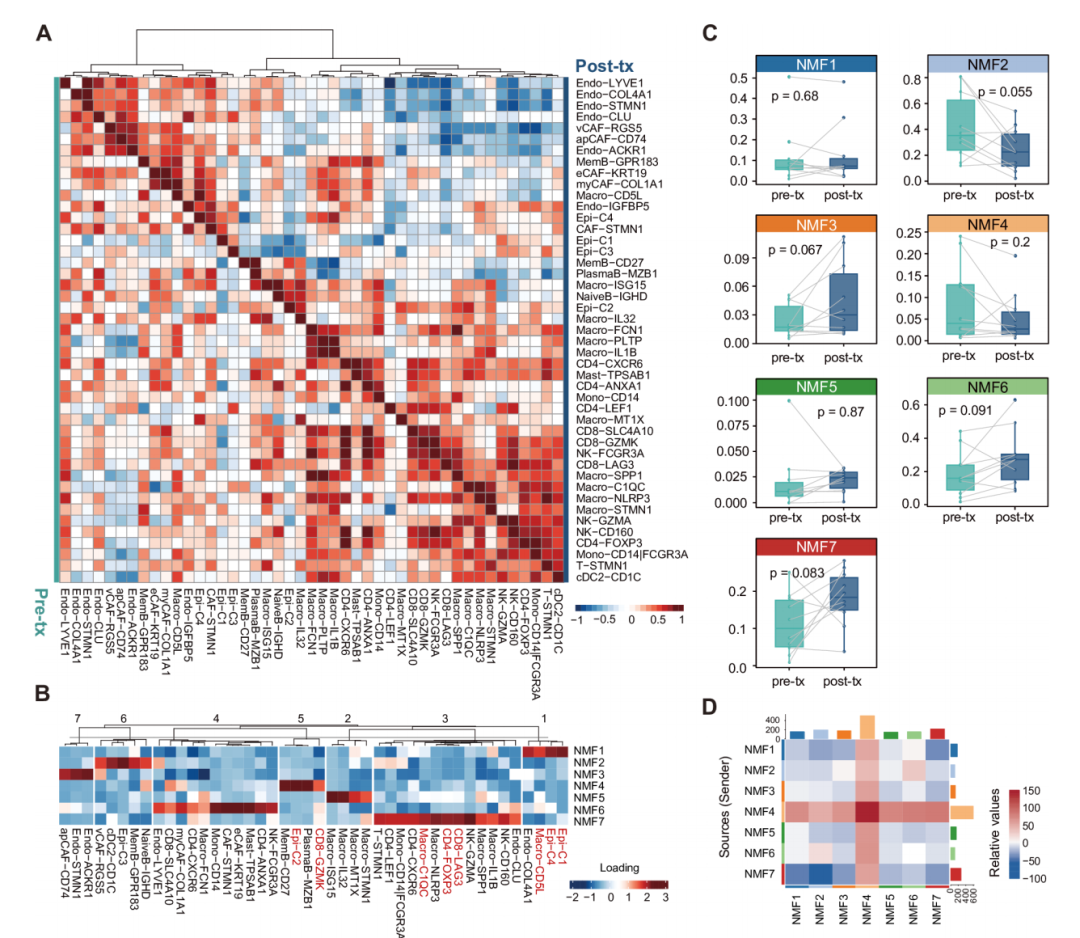
图5 细胞程序对VG161处理的动态重塑
7. VG161增强抗肿瘤和抗病毒免疫激活
研究发现VG161治疗导致肿瘤组织中T细胞和NK细胞在治疗后显著浸润。高分辨率图谱分析识别出不同的CD4+ T细胞、CD8+ T细胞和NK细胞亚群,其在治疗后的比例均显著增加(图6A和B)。TCR分析显示治疗后TCR克隆扩增明显增加,尤其在疾病控制组相比疾病进展组更为显著,表明应答者中免疫激活增强(图6C-E)。此外,IL12RB2和IL15RA表达显著升高,这与VG161经工程化改造的设计一致,可能进一步强化免疫应答。多重免疫荧光分析显示治疗后HSV-1和CD8+ T细胞富集,表明HSV-1感染促进了T细胞在免疫抑制性ICC肿瘤微环境内的招募和聚集(图6F)。此外,预测指数和治疗指数分析表明,较高的CD4+FOXP3+基线水平与对VG161治疗的不良反应相关,提示了潜在的免疫抑制机制。
为确定浸润的T细胞是抗病毒免疫反应还是抗肿瘤免疫反应的一部分,使用CellTypist并参考数据集,将CD8-GZMK、CD8-LAG3和T-STMN1细胞分别注释为肿瘤特异性T细胞和病毒特异性T细胞(图6G)。疾病控制和疾病进展患者均显示治疗后肿瘤特异性和病毒特异性T细胞增加;然而,疾病控制患者表现出显著更高的浸润程度,表明应答者产生了更强劲的免疫反应(图6H)。值得注意的是,肿瘤特异性T细胞表现出更高的耗竭评分,表明尽管浸润增加,但仍存在潜在的免疫功能障碍(图6I)。小鼠模型证实VG161具有双重免疫激活作用:经mVG161治疗后,小鼠的T细胞同时显示出针对肿瘤细胞(H22)和病毒抗原(mVG161)的IFN-γ分泌能力增强,表明其能协同激发抗肿瘤与抗病毒免疫。
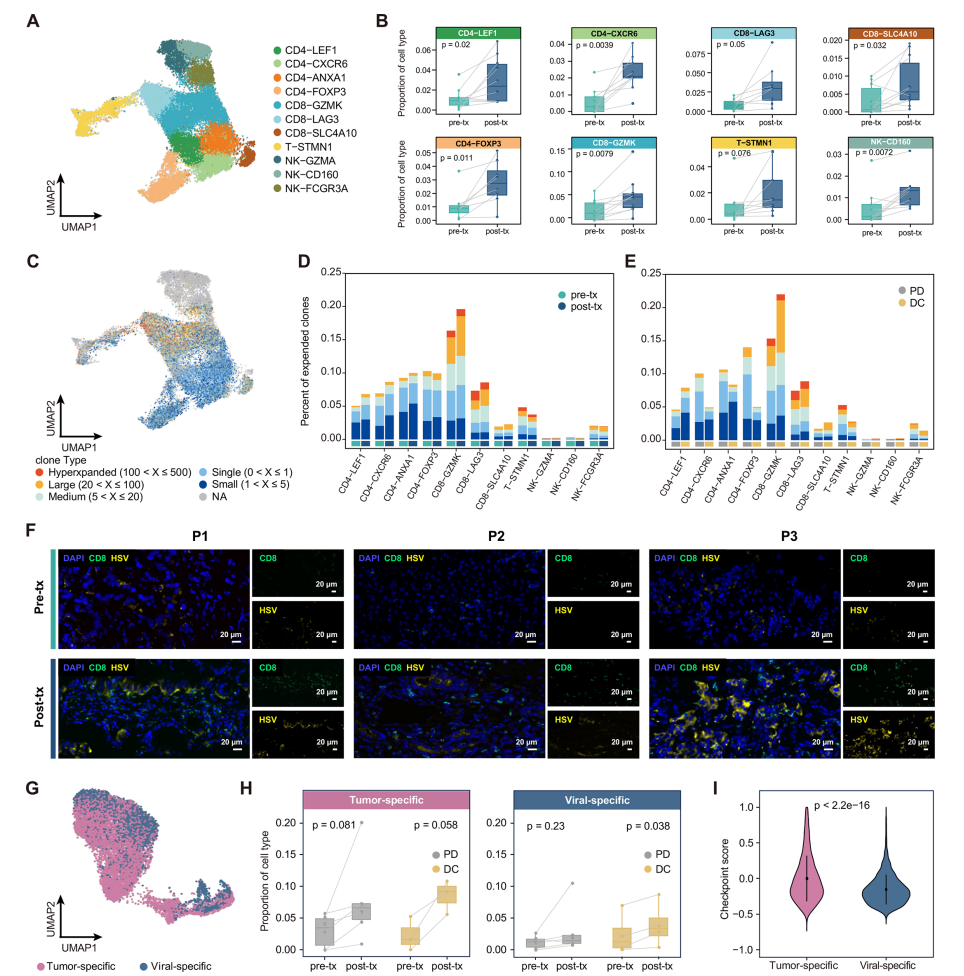
图6 VG161治疗期间T细胞免疫激活
8. 高比例Macro-C1QC与VG161治疗反应不佳相关
作者鉴定出15个髓系细胞亚群(图7A)。治疗后,VG161诱导了Macro-ISG15、cDC2-CD1C、Macro-IL32和Mono-CD14|FCGR3A的富集,表明肿瘤微环境内发生了免疫调节(图7B)。
进一步分析显示,较高的Macro-C1QC和Mono-CD14|FCGR3A基线水平与VG161治疗反应不佳相关(图7C和D)。在疾病控制组中,Mono-CD14|FCGR3A、Macro-FCN1、Macro-C1QC和Macro-CD5L的表达水平均低于疾病进展组(图7E)。此外,KEGG分析表明,疾病控制组中的Macro-C1QC在抗原呈递、TNF信号传导和病毒应答通路中富集(图7F),提示其在免疫激活中可能发挥作用。
治疗后,Macro-C1QC与Macro-NLRP3、CD4-FOXP3、T-STMN1、Mono-CD14|FCGR3A和CD8-LAG3表现出显著相关性,表明存在一个协调影响肿瘤微环境的免疫网络(图7H)。通过使用功能特异性髓系亚型的基因特征,发现疾病控制组的髓系亚型表现出更高的抗病毒和吞噬作用特征,特别是在Macro-C1QC和Macro-CD5L细胞中(图7G)。
此外,多重免疫荧光分析显示,治疗后HSV-1与Macro-C1QC之间存在负共定位,提示Macro-C1QC可能通过介导空间区室化来调节抗病毒免疫应答(图7I)。
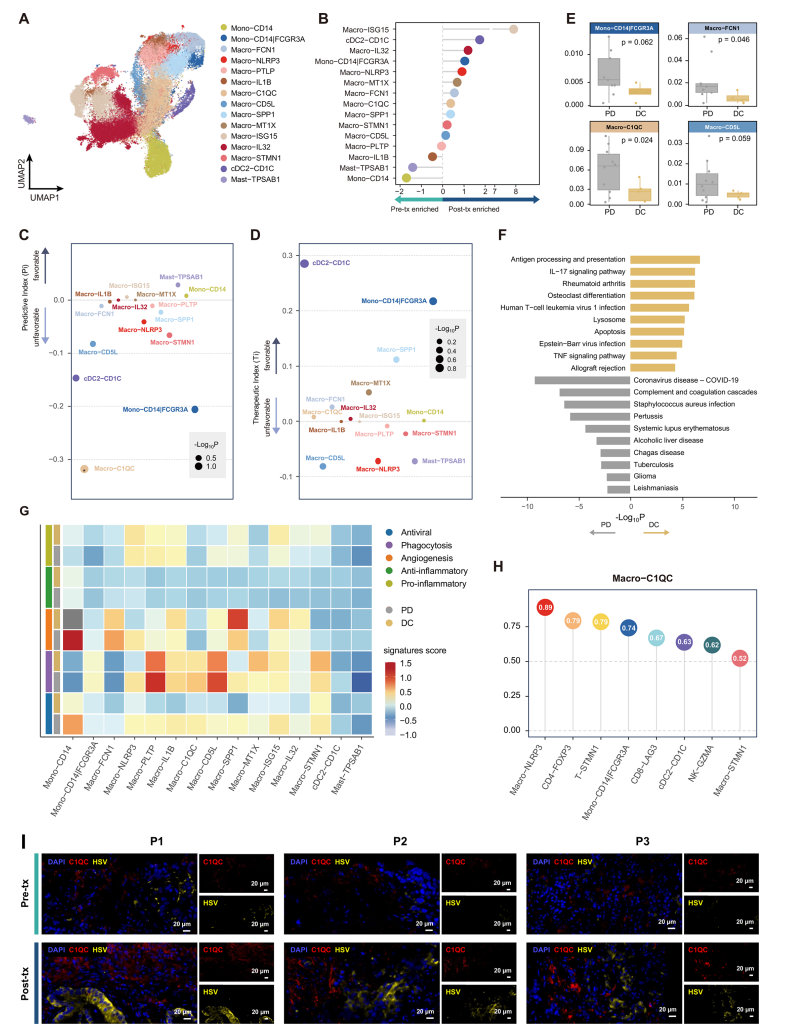
图7 Macro-C1QC细胞与VG161治疗有效性的相关性
本研究证实,溶瘤病毒VG161在经多线治疗的晚期肝内胆管癌患者中展现出有前景的临床价值。研究显示VG161具有可控的安全性,并能诱导肿瘤微环境发生有利的重塑:包括增加T细胞和NK细胞浸润、激活抗原呈递通路,并诱导肿瘤特异性T细胞应答。研究首次识别出关键生物标志物:高表达HSV-1进入受体的上皮细胞亚群Epi-C2与治疗敏感性相关,而巨噬细胞亚群Macro-C1QC则与治疗抵抗相关。值得注意的是,既往接受免疫检查点抑制剂长期治疗的患者获益更为显著。这些发现不仅为VG161的临床应用提供了依据,更指明了其与免疫检查点抑制剂联合治疗的潜力及未来的精准治疗方向。
参考文献:
doi:10.1136/gutjnl-2025-335904






