镉(Cd)是一种重金属,且有研究已证实长期的镉暴露会增加乳腺癌患病风险。5‘-甲硫基腺苷(MTA)是一种含硫核苷,有证据表明 MTA 及其代谢衍生物与肿瘤进展动力学有关。DOT1L 是乳腺癌发生的主要表观遗传驱动因素,但关于 DOT1L 活性和 MTA 代谢途径之间潜在交叉调节的知识差距仍然存在。作者前期研究发现,自噬功能障碍会显著促进镉诱导的乳腺癌细胞增殖、迁移及侵袭能力。然而,在镉诱导的乳腺癌进展过程中,MTA的作用机制有待进一步探索。
2025年9月,陆军军医大学余争平教授、皮会丰副教授和重庆大学周舟教授团队在Advanced Science期刊(IF:14.1)发表题为“5’-Methylthioadenosine Metabolic Reprogramming Drives H3K79 Monomethylation-Mediated PAK2 Upregulation to Promote Cadmium-Induced Breast Cancer Progression by Impairing Autophagic Flux”的研究成果,通过LC+GC代谢双平台+iTRAQ蛋白组学研究,构建了代谢-蛋白调控网络,发现MTA缺失特异性降低P21活化激酶2(PAK2)启动子区域的DOT1L甲基转移酶活性,并提升H3K79me1水平,从而促进PAK2表达,从而阻断乳腺癌进展所需的自噬流。
【欧易生物提供LC-GC代谢双平台+iTRAQ蛋白组学服务】

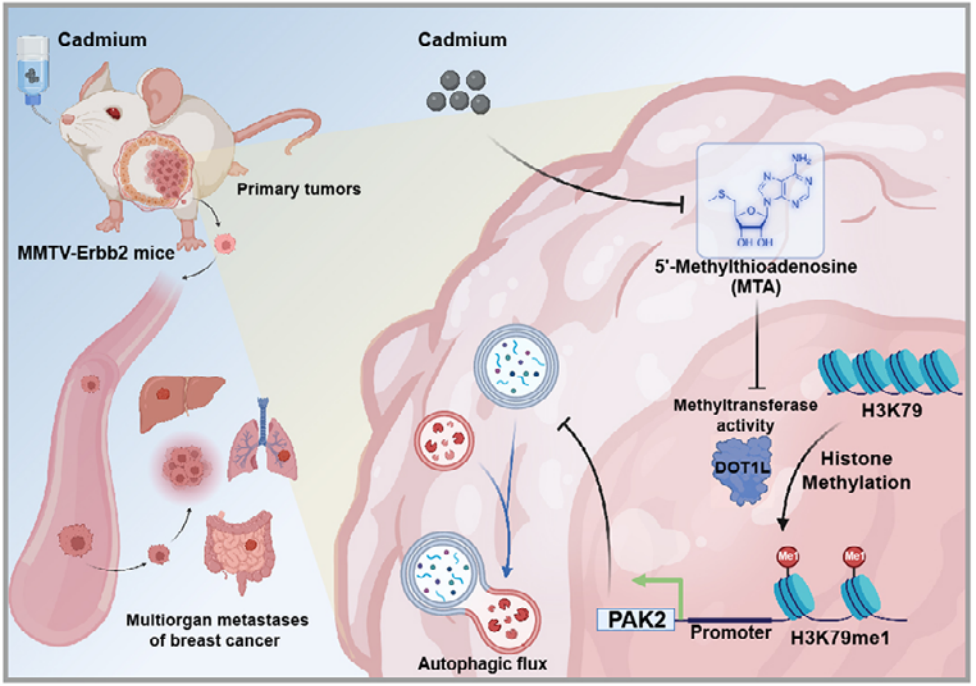
1、镉通过破坏自噬通量促进BC细胞的增殖、迁移和侵袭
为了探究镉暴露对乳腺癌进展的影响,作者将T-47D和MCF-7细胞分别暴露于0、1.5、3和6 μM镉溶液中培养72小时。CCK-8检测和Transwell实验表明,72小时暴露于6μM镉可显著促进乳腺癌细胞的增殖、迁移和侵袭能力。
为深入解析镉诱导乳腺癌进展的分子机制,作者采用iTRAQ技术对正常对照细胞和6μM镉溶液暴露的T-47D细胞进行标记定量蛋白质组学分析,GO和KEGG富集分析结果显示自噬调控功能的蛋白以及自噬相关通路可能是镉诱导乳腺癌的关键调控机制。通过对自噬的关键生物标志物以及对自噬流的检测发现,镉处理的乳腺癌细胞存在自噬清除功能缺陷。
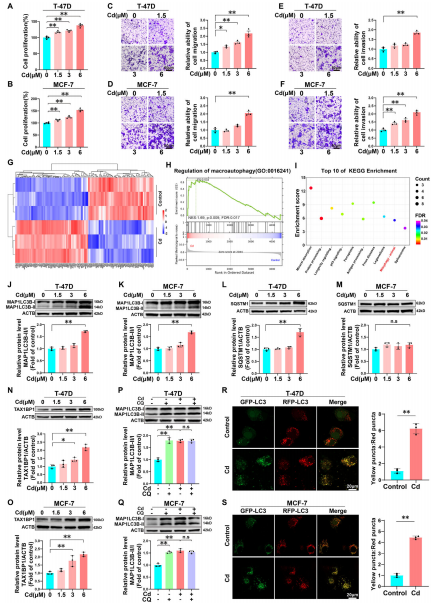
图1 镉暴露促进T-47D和MCF-7细胞的增殖、迁移和侵袭,同时破坏自噬通量
2、MTA缺乏导致Cd诱导的自噬通量阻滞和BC细胞增殖、迁移和侵袭的增加
为深入探究镉诱导阻断自噬流通路的分子机制,作者整合了LC+GC代谢双平台+iTRAQ蛋白组学数据,并通过IPA构建代谢物-蛋白质互作网络,发现MTA与组蛋白H3、SQSTM1等多个自噬蛋白存在显著相互作用关系。鉴于MTA分子的抗癌特性,作者评估了乳腺癌患者的临床特征与其含量的相关性,发现低MTA组的淋巴结转移发生率及TNM分期的晚期程度均显著高于高MTA组。
为探究镉诱导自噬功能障碍的乳腺癌细胞中MTA代谢重编程的作用,作者在镉处理组和未处理组的T47D和MCF7细胞系中补充MTA,监测到自噬标志物MAP1LC3B-II/I、SQSTM1和TAX1BP1水平升高。 此外,MTA给药显著抑制了镉处理乳腺癌细胞的增殖、迁移和侵袭能力。这些发现强调了MTA缺乏在镉诱导自噬流阻滞中的关键作用,以及其对乳腺癌细胞增殖、侵袭和迁移的影响。
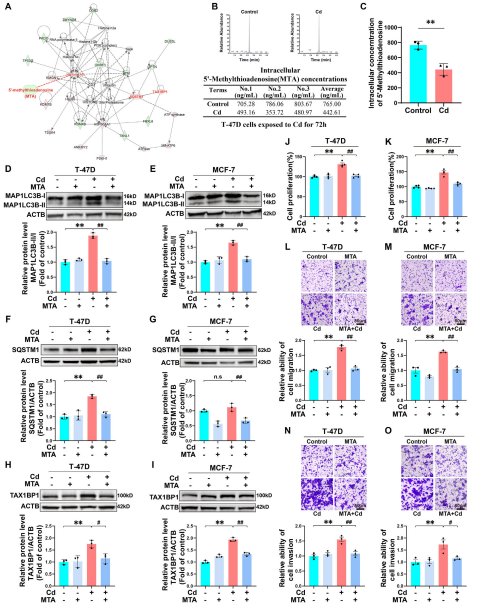
图2 MTA缺乏导致Cd诱导的自噬通量阻滞和BC细胞增殖、迁移和侵袭的增加
3、MTA通过降低细胞中DOT1L的活性来拮抗Cd诱导的H3K79me1
作者利用蛋白质谱技术研究了MTA与组蛋白H3之间的相互作用关系,最终确定了13个可能是镉和MTA互作的靶点的甲基化修饰肽段。其中,只有H3K79me1的甲基化水平在T-47D和MCF-7两种细胞变化模式一致,随着镉暴露增加,且在MTA补充后恢复。然而,DOT1L是唯一催化H3K79甲基化的甲基转移酶。
作者构建了DOT1L敲低和过表达细胞模型,发现DOT1L表达与H3K79me1水平显著正相关。同时,过表达DOT1L显著增强了细胞增殖能力、迁移潜能和侵袭能力,这些与镉暴露乳腺癌模型中观察到的表型一致。
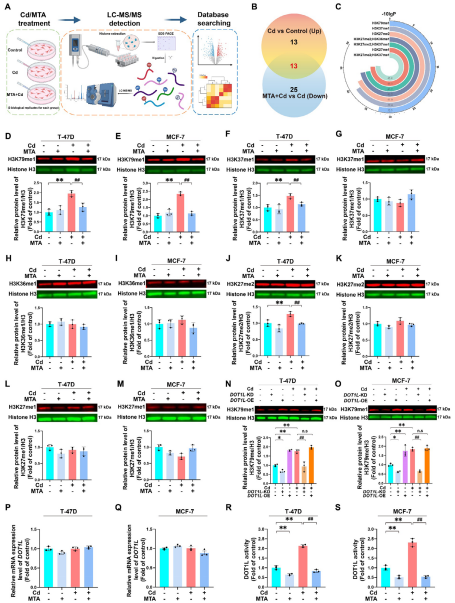
图3 镉诱导的MTA蛋白缺失通过重新激活DOT1L在乳腺癌细胞中提升H3K79me1水平
4、PAK2蛋白是镉诱导H3K79me1的下游靶点
作者通过利用转录组学技术检测了PAK2敲低和过表达模型中的基因谱,发现镉处理显著增强了H3K79me1结合峰的富集程度。其中,1116个基因的H3K79me1结合峰同时受到镉和MTA的调控,这些基因在MAPK信号通路最显著富集。利用venn分析,作者找到PAK2和PLA2G4B两个候选基因在其启动子区域与H3K79me1有结合峰。RT-qPCR分析和免疫共沉淀实验结果都显示PAK2是H3K79me1在乳腺癌模型中的保守下游靶标。
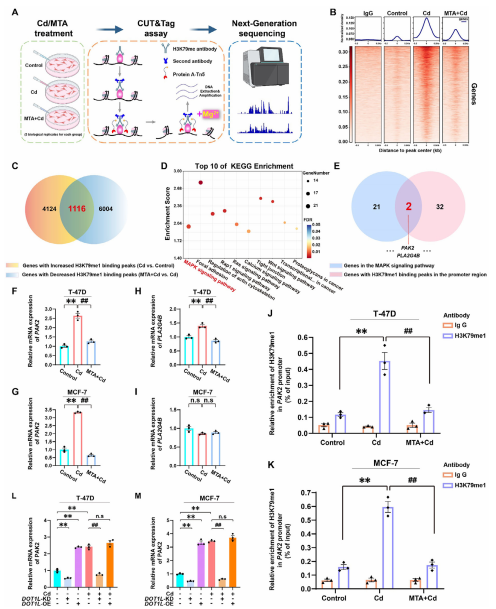
图4 PAK2蛋白是镉诱导H3K79me1的下游靶点
5、PAK2过表达消除了MTA介导的抑制镉诱导的自噬通量损伤和细胞进展
作者探讨了PAK2在镉诱导的乳腺癌细胞自噬流阻滞中的作用。研究数据表明,镉暴露显著提升了PAK2蛋白的表达水平,而MTA治疗能有效抑制这种镉诱导的上调现象。功能实验和药理抑制试验均证实了证实了PAK2在镉促癌效应中的关键作用。总之,这些结果将PAK2确立为镉诱导的H3K79me1修饰的下游介质,通过增加BC细胞的增殖、迁移和侵袭能力来协调自噬阻滞并促进恶性进展。
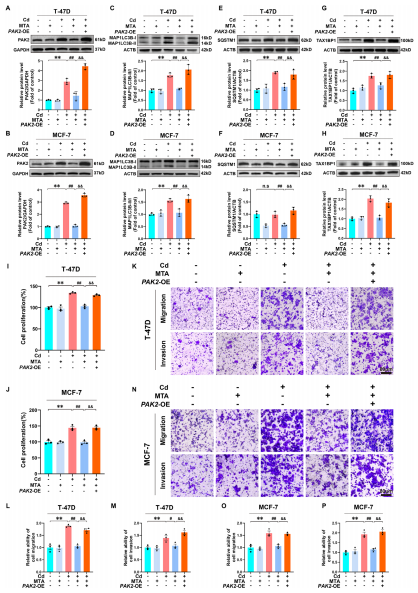
图5 PAK2过表达可消除MTA介导的镉诱导自噬流损伤及乳腺癌细胞增殖抑制
6、MTA的补充,抑制了Cd诱导维持MMTV-ErbB2小鼠H3K79me1去甲基化介导的自噬对乳腺肿瘤进展和转移的影响
MMTV-ErbB2小鼠是经典的乳腺肿瘤动物模型,作者建立的动物模型小鼠在延长潜伏期后自发发展为乳腺肿瘤。为了确定MTA代谢的恢复是否拮抗了镉暴露在体内的效应,作者对MMTV-ErbB2小鼠进行了多种治疗方案。从18周龄到28周龄小鼠,实验检测到可触及的乳腺肿瘤,并发现腹腔注射MTA显著延迟了镉暴露促进的乳腺肿瘤的早期发病均能有效抑制肿瘤体积的加速增长。作者收集了乳腺肿瘤组织检测H3K79me1水平的体内变化,与对照组相比,镉暴露导致乳腺肿瘤组织H3K79me1水平和Pak2转录水平显著升高,即MTA联合治疗能显著降低H3K79me1和Pak2的表达水平。与透射电镜观察结果一致。本次研究结果揭示了MTA代谢重编程在镉介导的自噬流障碍及乳腺癌体内进展中的作用机制。
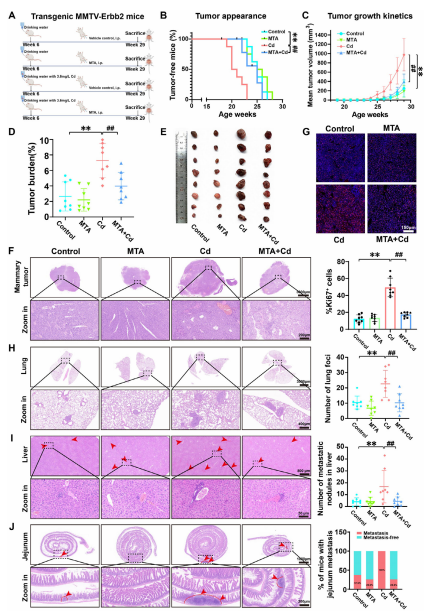
图6 MTA补充剂可缓解镉诱导的MMTV-ErbB2小鼠乳腺肿瘤进展与转移
本研究首次证实:
i)在镉诱导的乳腺癌恶性转化过程中,MTA代谢重编程在表观遗传自噬轴中发挥核心调控作用;
ii) 镉诱导的MTA缺失会特异性降低DOT1L甲基转移酶活性,并提升PAK2启动子区域的H3K79me1修饰水平,从而促进PAK2表达,这一过程正是阻断自噬通量、推动乳腺癌进展的关键机制;
iii) MTA水平与乳腺癌分期呈负相关,充分印证了MTA缺失在乳腺癌进展中的临床重要性。
综合研究数据不仅揭示了镉诱导乳腺癌进展的代谢与表观遗传调控机制,更为全面评估镉暴露相关的生态健康风险提供了全新视角。
本研究利用代谢双平台+iTRAQ蛋白组学等多种组学技术,从分子层面详细阐述了MTA药物治疗镉诱导乳腺癌的机制。
原文链接:DOI: 10.1002/advs.202500941






