胰腺癌(PDAC)被誉为“癌中之王”,其5年生存率低于12%,早期几乎无症状,现有标志物CA19-9对早期病变不敏感。临床90 %的PDAC被认为起源于胰腺上皮内瘤变(PanIN),然而,PanIN 阶段究竟发生了哪些分子事件、这些事件如何驱动后续恶性进展,仍待进一步研究。传统bulk组学因基质污染,难以精准捕捉PanIN特异性事件。本研究采用空间蛋白质组学,从FFPE样本中纯化PanIN组织,揭示代谢重编程早于癌变发生,并锁定关键转录因子SP1。
2025年8月,南京鼓楼医院胰腺与代谢外科仇毓东&程浩&闫超团队联合南京大学、江苏分子医学实验室,
在Advanced Science(IF=14.1)在线发表题为“SP1-Mediated Glycolytic Reprogramming Promotes Tumorigenesis and Progression in Pancreatic Cancer”的重磅研究。该研究通过空间蛋白质组学,首次在5例PanIN微病变中系统描绘代谢重编程图谱,锁定转录因子SP1在PanIN阶段即显著上调,并通过激活PFKFB4驱动糖酵解重编程,促进PDAC发生与进展;并通过转基因KPC小鼠、PDO/PDOX模型及同位素示踪完成机制与转化验证。
【欧易生物为本研究提供空间蛋白质组学技术服务】

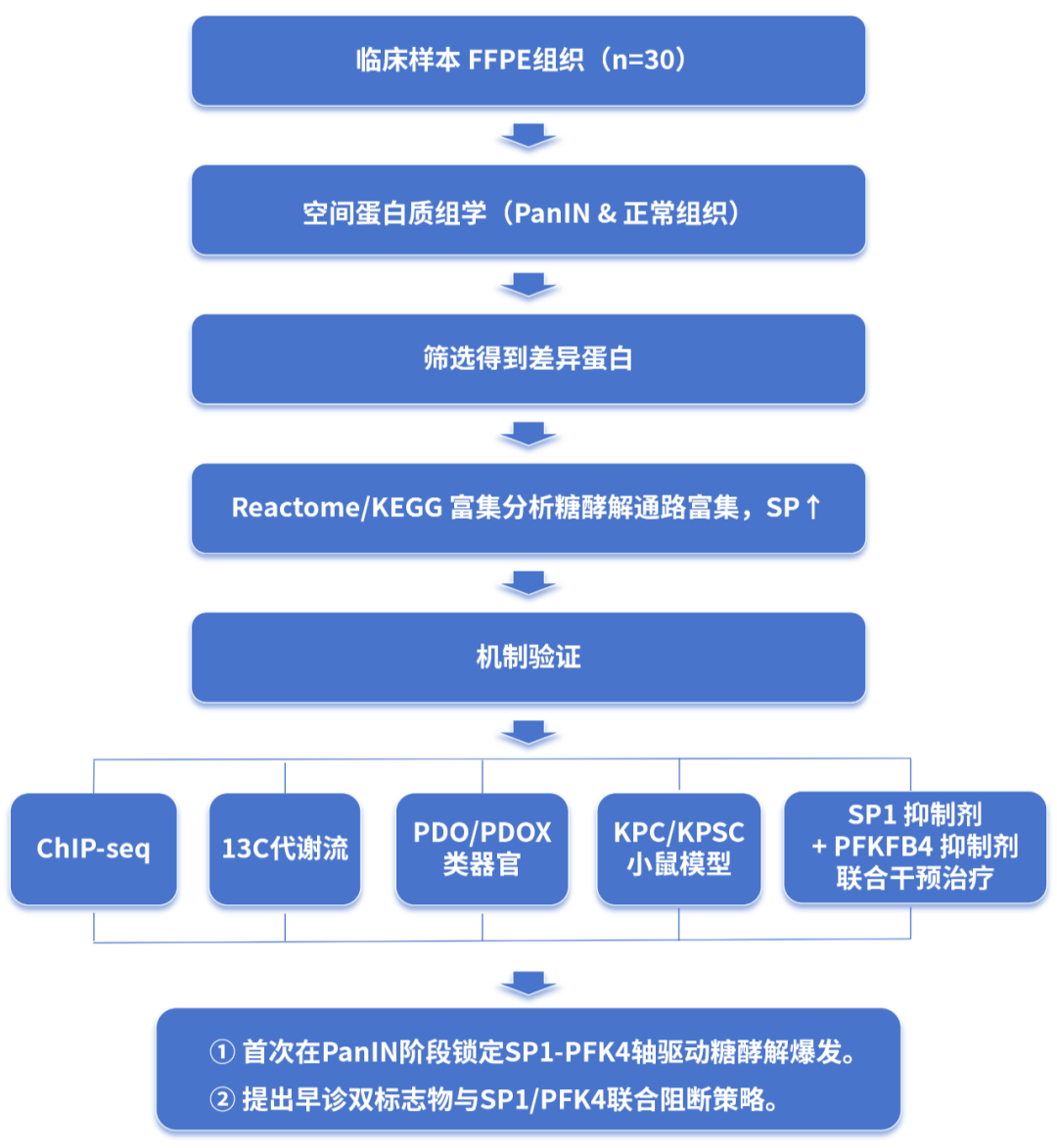
1. 人源标本:5例PanIN + 配对正常胰腺FFPE
2. 验证队列:20例PanIN IHC、40例PDAC TMA
3. 动物模型:KrasLSL-G12D/+;Trp53LSL-R172H/+;Pdx1-Cre (KPC)与Sp1条件敲除(KPSC)小鼠
4. 类器官/细胞系:13株PDAC细胞系、3例PDO、PDO-PDOX、CDX裸鼠模型
1. 激光捕获显微切割(LCM):0.1 mm²级病灶精准取材
2. 4D-DIA蛋白质组:timsTOF Pro2,>2600差异蛋白,深度覆盖低丰度转录因子
3. ChIP-seq:SP1全基因组结合图谱
4. Stable-isotope tracing:13C6-Glucose示踪糖酵解通量
5. Seahorse XF:实时ECAR/OCR评估代谢表型
6. 多重免疫荧光&IHC:空间验证关键蛋白表达
1. 基于空间蛋白质组学揭示了胰腺上皮内瘤变(PanIN)中的代谢重塑
在确认PanIN 阶段即出现“糖酵解爆发”的过程中,作者首先利用LCM从5名 PDAC 患者 FFPE 切片中精确切取PanIN及配对正常胰腺组织(图1A),随后进行timsTOF Pro2 4D-DIA蛋白组检测,共鉴定2600个差异蛋白,其中PanIN中2203个上调、397个下调;Reactome与KEGG富集一致显示糖酵解通路显著激活(图1B-C),热图进一步展示HK2、PFKL、LDHA等关键糖酵解酶显著升高(图1D)。为在更大样本中验证,研究者对20例PanIN与配对正常胰腺进行IHC,证实HK2、PFKL、LDHA蛋白表达显著增高,而脂质代谢酶 CD36、ACSL4 及氨基酸代谢酶 GLS、GLUD1/2 显著下降(图 1E-L)。

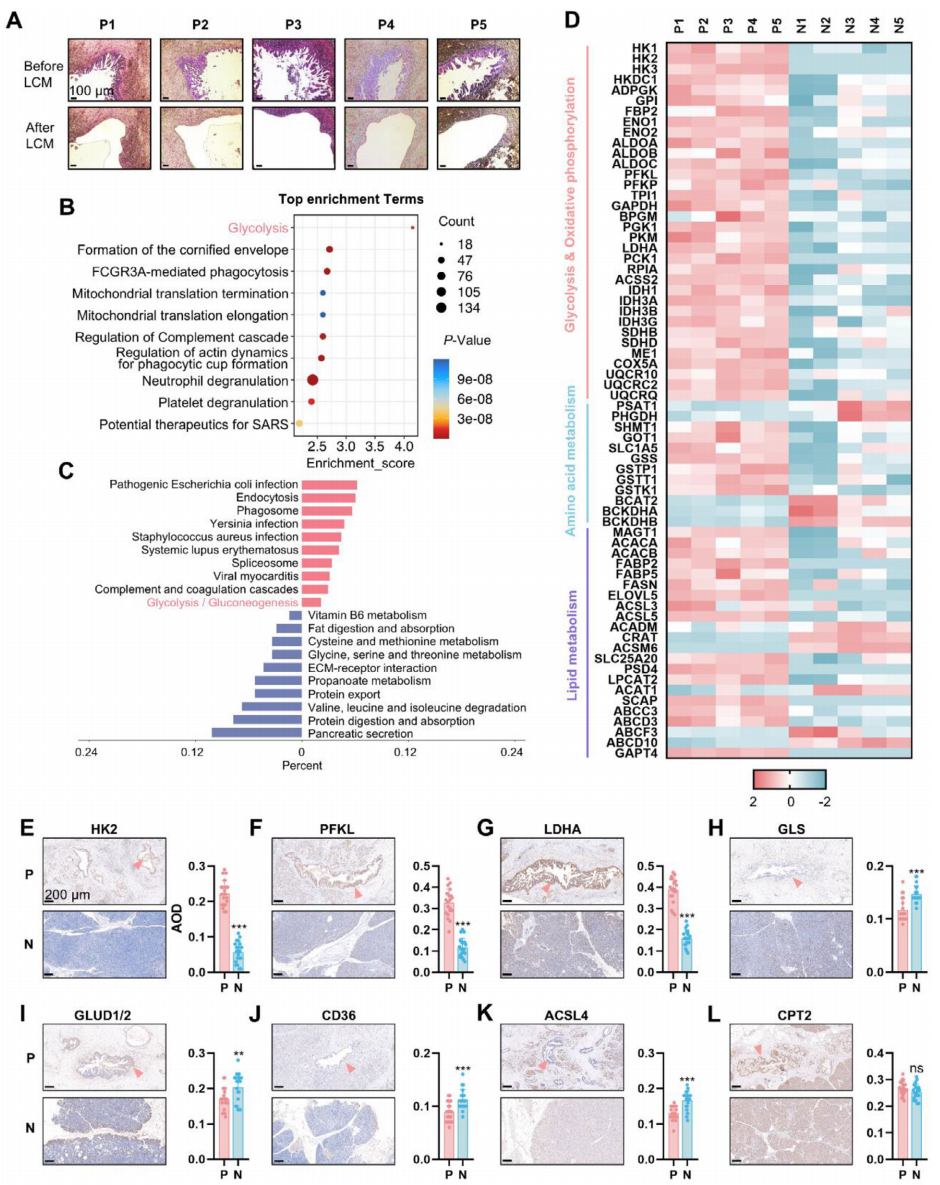
图1
2. PanINs和PDACs中SP1的上调与患者预后不良相关
为了挖掘驱动上述代谢重编程的上游转录因子,作者将差异蛋白中的转录因子与代谢酶进行Sankey网络分析,锁定 SP1、KLF4 等5个核心调控节点(图 2A);其中SP1位列 PanIN 中8个最显著上调转录因子之一(图 2B)。TRRUST数据库显示SP1与PDAC三大驱动基因MYC、TP53、SMAD4共享大量靶基因(图2C)。公共数据库GEPIA进一步证实SP1在PDAC组织中高表达(图2D),且Kaplan-Meier曲线表明SP1高表达患者总生存期显著缩短(图2E)。IHC结果显示22例PanIN(图2F-G)及40例PDAC组织芯片(图2H-I)均呈现SP1核内高表达,且SP1与MYC表达呈正相关(图2J)。
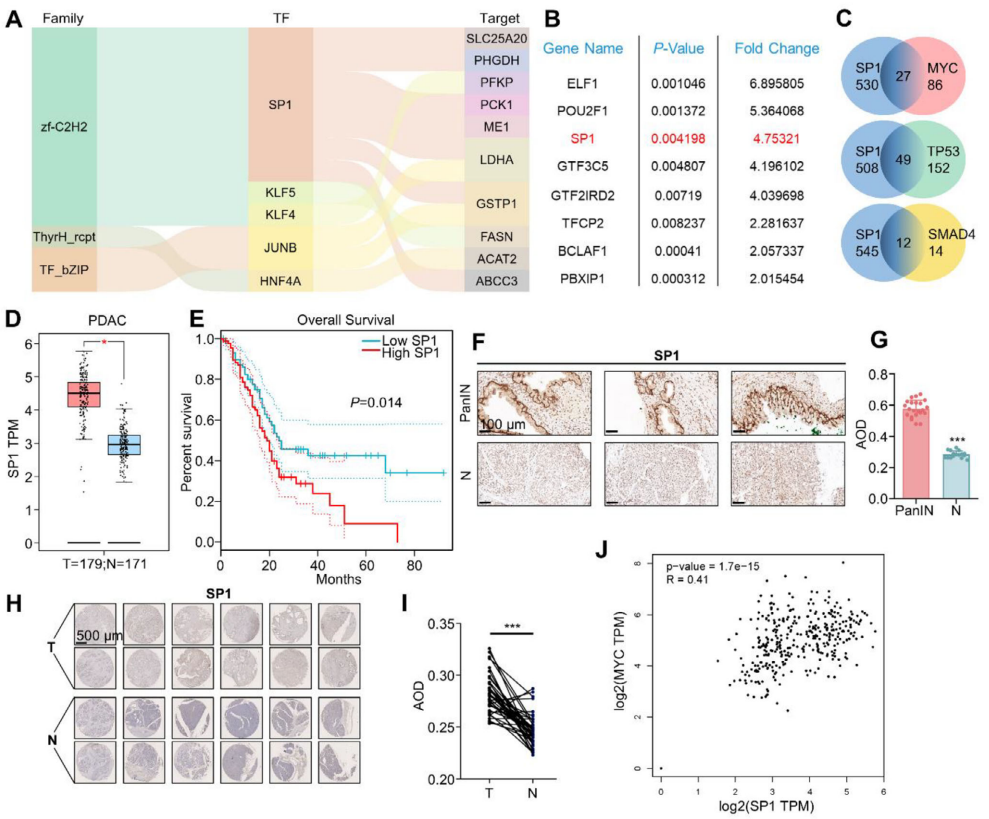
图2
3. SP1促进PDAC肿瘤生长
为功能验证SP1促瘤作用,作者首先在3DPDO模型中加入SP1抑制剂TA或MIT,可见类器官生长受抑(图3A);WesternBlot证实SP1及其下游VEGFA蛋白随药物剂量依赖性下降(图3B-C)。将PDO进行NCG小鼠原位移植建立PDOX模型后,口服TA或腹腔注射MIT均显著抑制肿瘤体积与重量(图3D-E),IHC显示SP1、Ki67表达同步下降(图3F)。在13株PDAC细胞系中,FG与HPAF-II的SP1蛋白水平较高(图3G),shRNA敲低SP1后细胞增殖及克隆形成显著受抑(图3H-L),裸鼠原位移植同样证实SP1缺失明显减小肿瘤重量(图3M-P)。
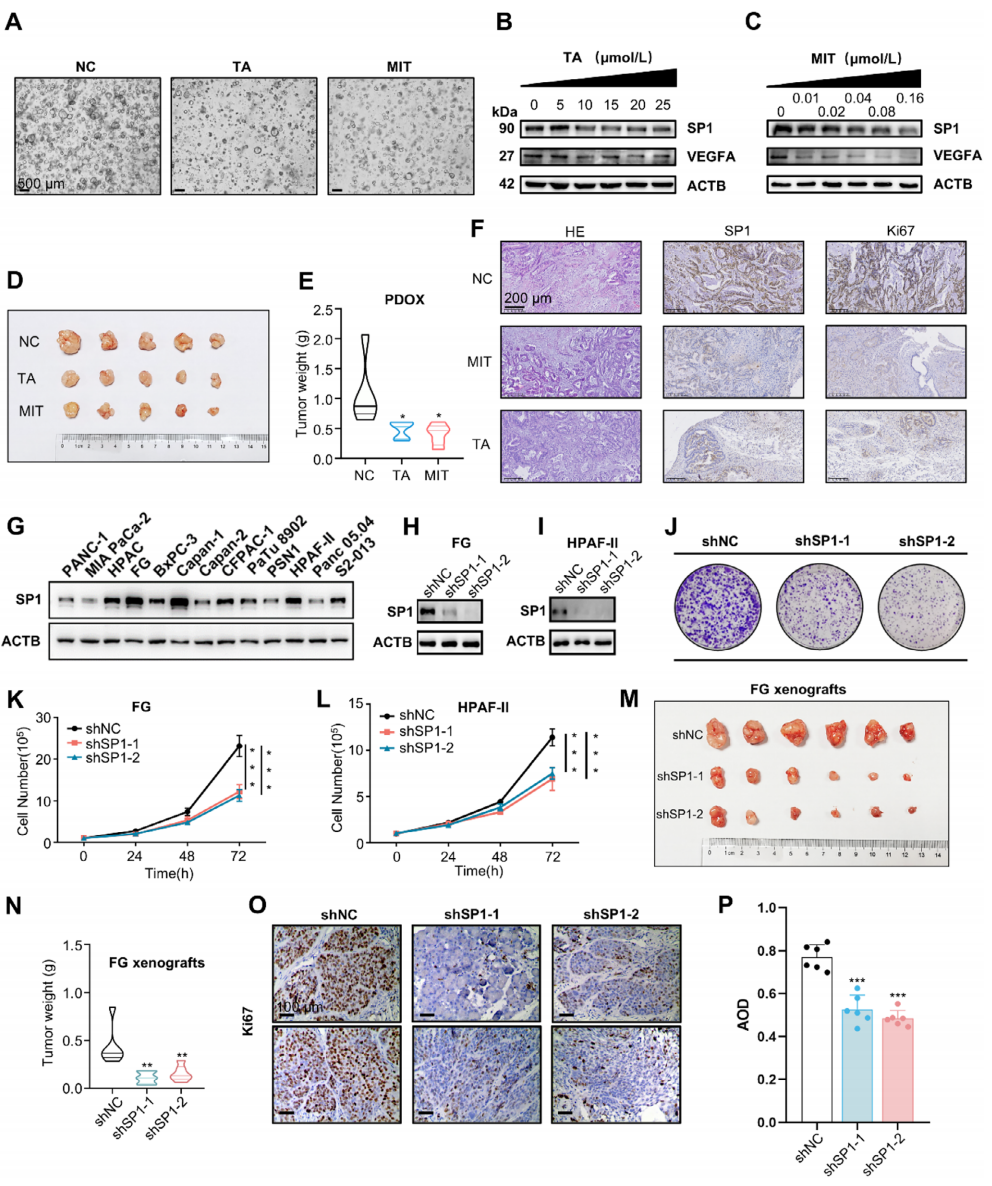
图3
4. SP1基因敲除抑制KrasLSL-G12D/+、Trp53LSL-R172H/+和Pdx1-Cre(KPC)小鼠的PDAC肿瘤形成
为在体内遗传学水平验证SP1的作用,作者通过将Sp1LoxP/LoxP小鼠与KPC小鼠杂交得到KPSC条件敲除模型(图4A)。多色免疫荧光显示KPSC胰腺中CK19阳性区域、α-SMA阳性CAF区域及Vimentin表达均随时间显著低于KPC对照(图4B-E)。AlcianBlue、Ki67、SiriusRed染色依次表明KPSC小鼠黏液分泌减少(图4F,J)、增殖指数降低(图4G,K)及纤维化减轻(图4H,L)。代谢酶IHC显示KPSC胰腺中HK2、PFKL、LDHA表达下调(图4I)。生存曲线显示SP1缺失显著延长KPC小鼠总生存期(图4M)。
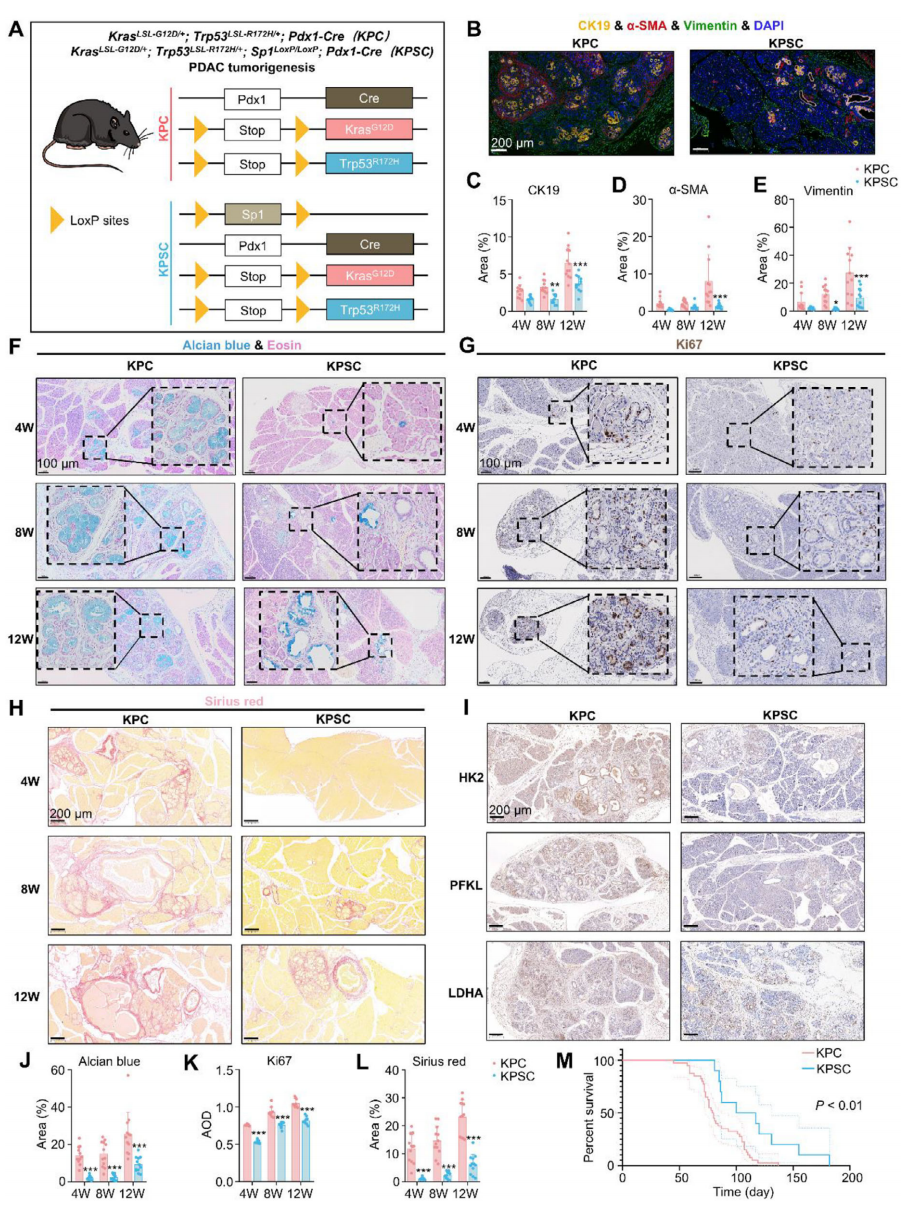
图4
5. SP1调节PDAC细胞有氧糖酵解
为解析SP1如何调控糖酵解,作者在FG细胞中进行ChIP-seq鉴定SP1全基因组结合位点(图5A),并与SP1敲低后的RNA-seq差异基因取交集,获得677个潜在靶基因(图5C);Wikipathways与KEGG分析均显著富集糖酵解通路(图5D),热图显示关键糖酵解酶表达受SP1正调控(图5E)。Seahorse实验表明SP1敲低显著降低ECAR与ATP生成率,而OCR无明显变化(图5F-H)。13C6-葡萄糖同位素示踪进一步证实SP1缺失导致糖酵解中间产物F-1,6-BP等下降,而TCA循环中间产物代偿性升高(图5I)。
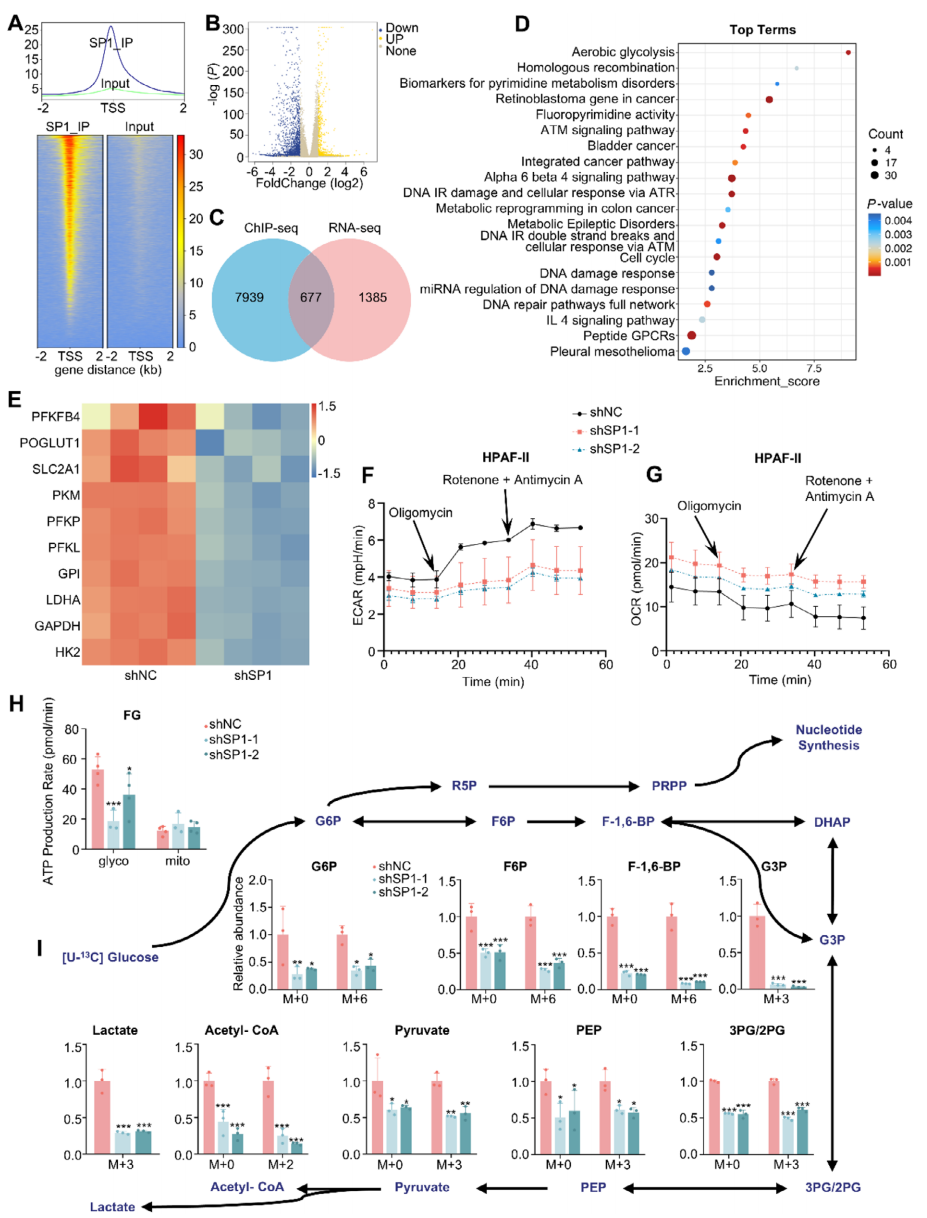
图5
6. SP1转录激活PDAC细胞中的PFKFB4
在明确SP1通过转录激活PFKFB4的机制研究中,RT-qPCR显示SP1敲低后PFKFB4 mRNA下降最显著(图6A),且F-1,6-BP含量同步减少(图6B)。Western Blot证实SP1缺失降低PFKFB4蛋白水平(图6D)。双荧光素酶报告基因实验表明SP1可增强PFKFB4启动子活性,且活性区定位于−1300~−1000nt(图6E-H);突变分析进一步将关键结合位点锁定在−1230~−1221nt与−1203~−1193nt(图6I-J)。ChIP-qPCR最终验证SP1直接结合PFKFB4启动子(图6K)。
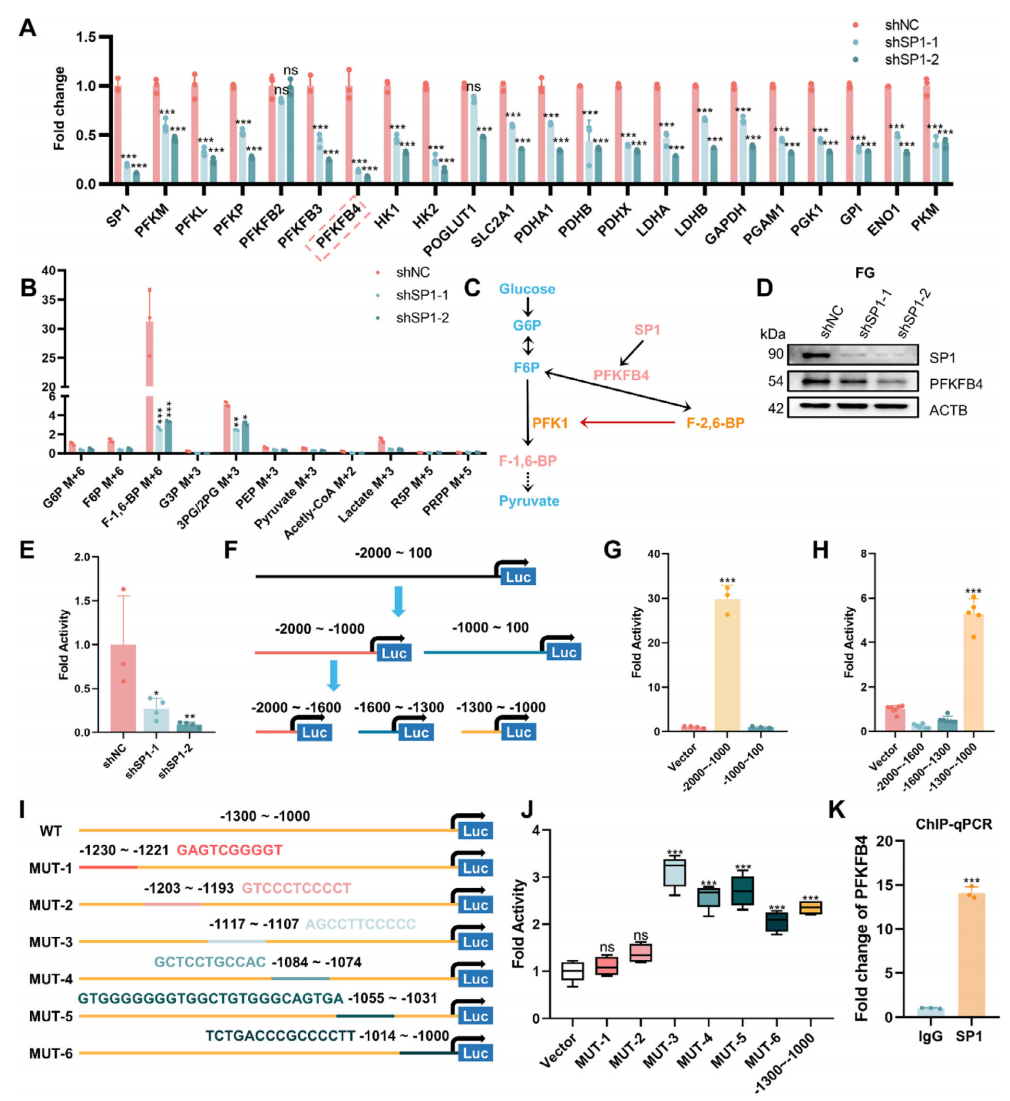
图6
7. SP1通过激活PFKFB4调节PDAC细胞的有氧糖酵解
为证明PFKFB4是SP1介导糖酵解及增殖的关键下游,作者在FG细胞中分别敲低/过表达PFKFB4(图7A-C)。代谢检测显示PFKFB4缺失同样降低F-1,6-BP与F-2,6-BP水平,而过表达PFKFB4可挽救SP1敲低导致的代谢抑制(图7D-E)。Seahorse结果一致表明PFKFB4过表达恢复SP1缺失细胞的ECAR(图7F-H)。体外增殖与克隆形成实验进一步证实PFKFB4过表达可逆转SP1敲低造成的生长抑制(图7I-J)。在FG-luc原位移植模型中,PFKFB4过表达同样逆转SP1缺失导致的肿瘤生长受阻(图7K-N)。临床样本IHC显示75例PanIN中SP1与PFKFB4同步高表达(图7O-R)。
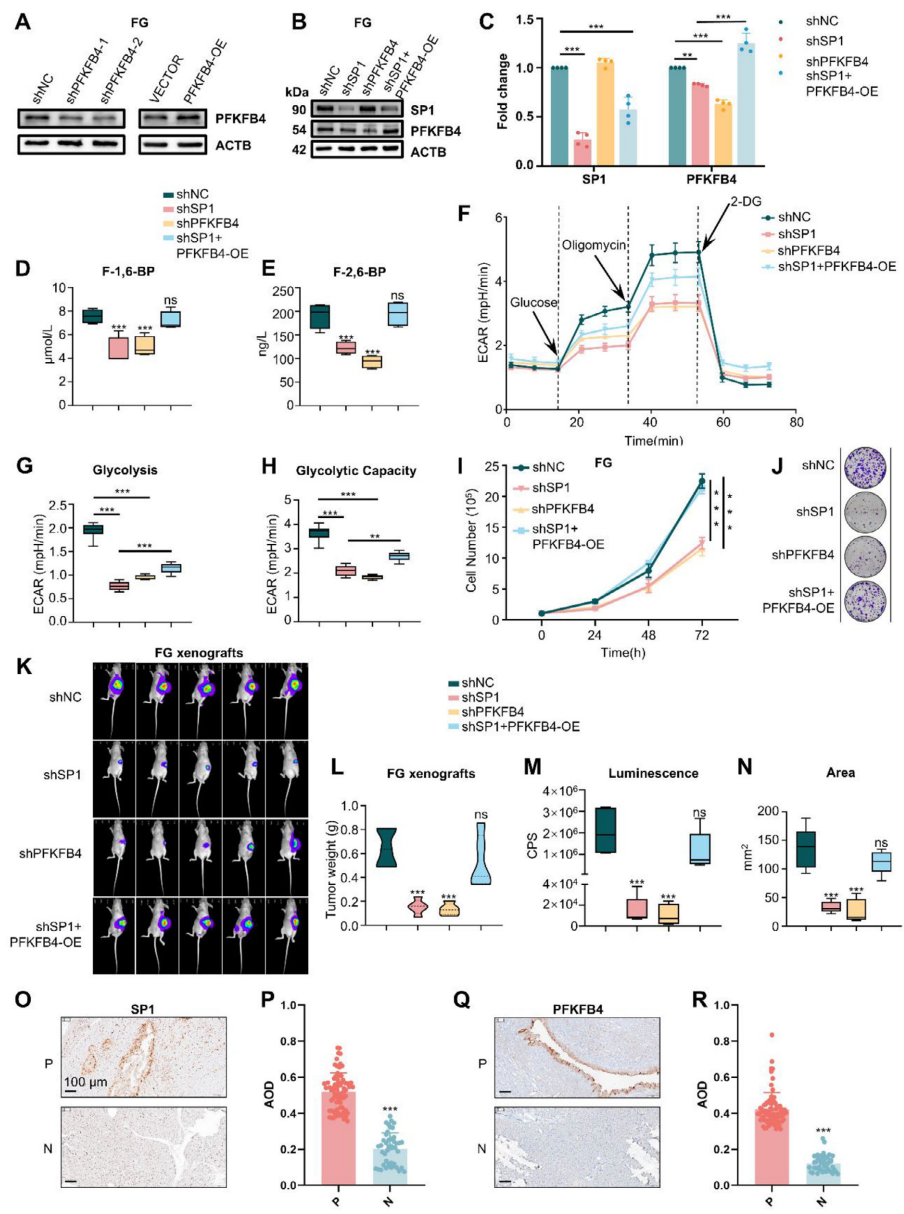
图7
8. SP1抑制剂TA与PFKFB4抑制剂5MPN单药及联合疗效
最后,作者在FG原位移植模型中评估SP1抑制剂TA与PFKFB4抑制剂5MPN的单药及联合疗效。结果显示单药即可显著抑制肿瘤重量,半剂量联用效果最佳且对小鼠体重无明显影响(图8A-D)。机制示意图总结SP1通过直接激活PFKFB4转录,增强PFK-1活性,加速糖酵解通量,从而推动胰腺癌发生与进展(图8E)。
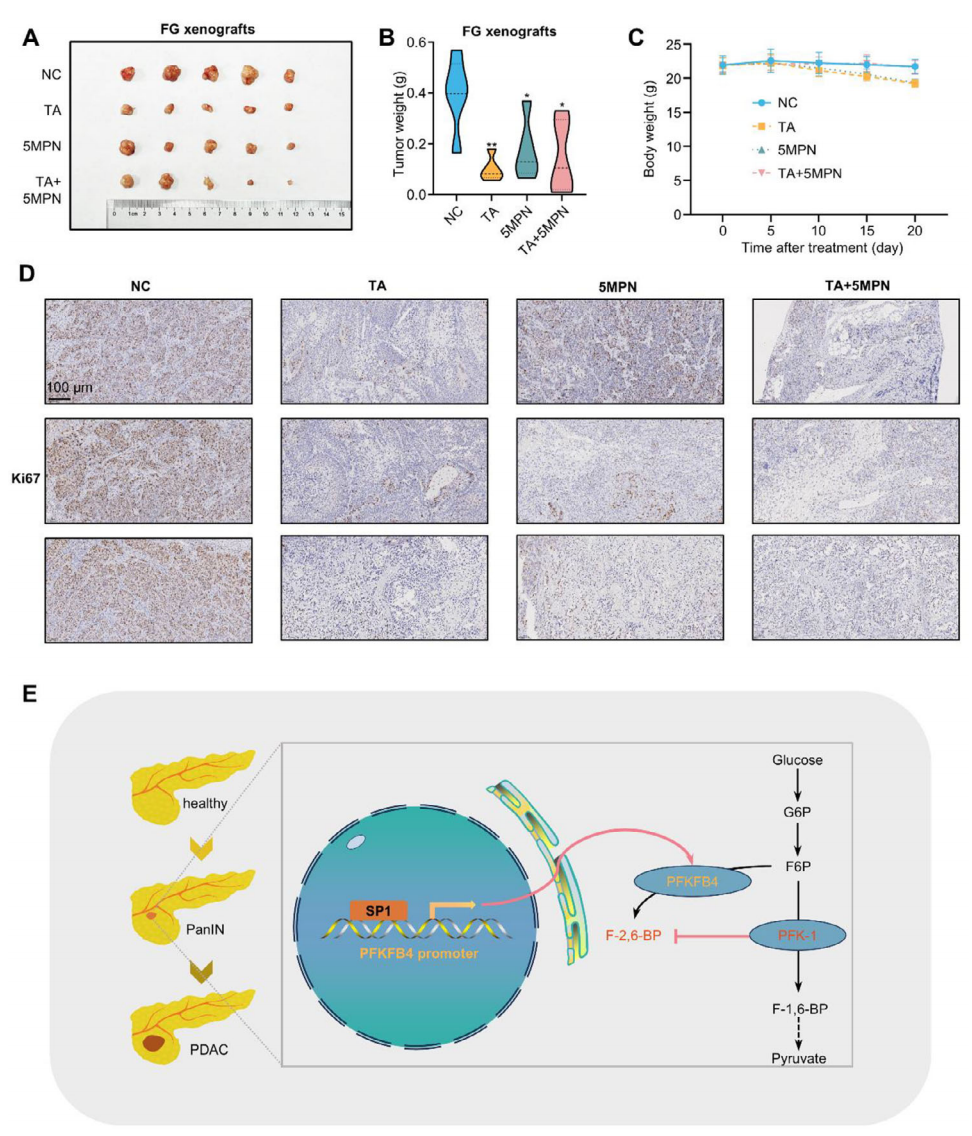
图8
本研究以空间蛋白质组学为核心,首次在人源PanIN水平证实:SP1-PFKFB4轴介导的糖酵解重编程是胰腺癌“极早期”驱动事件。靶向该轴不仅能延缓甚至阻断PanIN向PDAC演进,还为临床提供了可转化的早诊标志物(SP1/PFKFB4)及联合干预策略。
1. 技术创新:首次实现PanIN微病变空间蛋白质组学研究,突破FFPE样本低丰度限制。
2. 临床价值:SP1/PFKFB4双重抑制剂已进入动物验证阶段,为胰腺癌“早筛+早治”提供候选方案。
3. 组学应用:多组学研究交叉验证,确保机制链完整闭环。
4. 适用研究:若正在开展肿瘤早筛标志物、代谢重编程或转录调控研究,可参考本研究的“空间蛋白质组学”策略,以微量临床样本撬动大发现!
【参考文献】
Hang, H., Yu, M., Zhu, L., Tang, N., Fu, X., Cai, Z., Yan, M., Chen, Y., Yang, L., Wu, J., Tang, J., Xie, Y., Li, Q., Fu, X., Mao, L., Chen, J., Meng, F., Kong, B., Han, X., Yan, C., Cheng, H. (2025). SP1-Mediated Glycolytic Reprogramming Promotes Tumorigenesis and Progression in Pancreatic Cancer. Advanced science (Weinheim, Baden-Wurttemberg, Germany), e10071. Advance online publication. https://doi.org/10.1002/advs.202510071






