2025年7月21日,中山大学第五附属医院陈明远教授、中国科学院数学与系统科学研究院张世华教授等团队合作,在Nature Genetics (IF=29)上发表题为”Single-cell and spatial transcriptomics reveal mechanisms of radioresistance and immune escape in recurrent nasopharyngeal carcinoma”的论文,该研究通过单细胞与空间转录组技术,首次揭示rNPC中MCAM⁺成纤维细胞驱动的放疗抵抗机制及胶原蛋白IV介导的免疫排斥微环境,为突破复发性鼻咽癌的治疗瓶颈提供了初步的靶点和策略。欧易生物提供了空间转录组测序的技术服务。

发表期刊:Nature Genetics
影响因子:29
涉及的欧易生物服务产品:空间转录组测序
研究背景
鼻咽癌(NPC)是一种在东南亚地区高发的头颈部恶性肿瘤,其复发和放疗抵抗是治疗中的主要挑战。尽管免疫检查点抑制剂在某些患者中显示出疗效,但整体响应率仍不理想。近年来,scRNA-seq和空间转录组学技术的发展为研究肿瘤微环境的异质性提供了强有力的工具。这些技术能够揭示不同细胞类型之间的相互作用及其在肿瘤进展和治疗抵抗中的功能。然而,目前对NPC复发(rNPC)的肿瘤微环境(TME)研究仍然有限,特别是在放疗抵抗和免疫逃逸机制方面。因此,深入理解NPC的TME及其在放疗抵抗和免疫逃逸中的作用,对于开发新的治疗策略至关重要。
研究内容
这篇文章通过单细胞和空间转录组学技术,深入研究了复发鼻咽癌(rNPC)中放疗抵抗和免疫逃逸的机制。研究团队收集了24名患者的39个肿瘤样本,包括11个pNPC和13个rNPC样本,进行了详细的细胞组成和微环境差异分析。研究设计包括scRNA-seq、空间转录组学、全外显子组测序(WES)以及免疫组织化学(IHC)染色验证,并利用多个验证队列进行预后分析。研究结果表明,rNPC中MCAM⁺癌症相关成纤维细胞(CAFs)显著富集,并通过COL4-ITGA2-FAK-AKT轴促进肿瘤放疗抵抗。此外,COL4抑制了T细胞的浸润,导致免疫逃逸,rNPC中CD8⁺ ZNF683⁺T细胞比例增加,但其细胞毒性较低,且三级淋巴结构显著减少。本研究结果为开发新的治疗策略提供了重要的理论基础,有望改善rNPC患者的预后。
技术路线
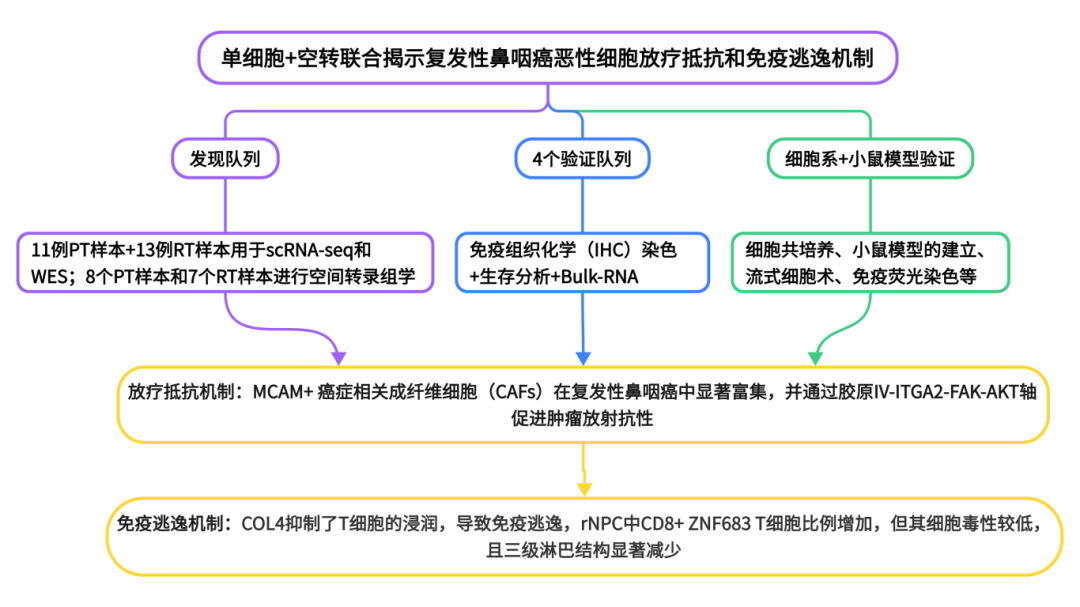
研究结果
Result 1 pNPC和rNPC肿瘤生态系统的分析
为了解析原发性鼻咽癌(pNPC)和复发性鼻咽癌(rNPC)之间的肿瘤生态系统差异,作者收集了11例初治pNPC患者(PT样本)和13例rNPC患者(RT样本)的肿瘤标本进行scRNA-seq和全外显子组测序(WES),并收集了相应的8个PT样本和7个RT样本进行空间转录组学分析。此外,作者还纳入了4个验证队列来确认发现队列中的差异并进行预后分析,队列1:40例配对PT和RT患者进行免疫组织化学(IHC)染色;队列2:来自中山大学肿瘤防治中心回顾性队列的86例接受根治性放疗的pNPC患者;队列3:52例接受PD-1抑制剂和抗VEGFR抗体治疗的复发或转移性鼻咽癌患者进行IHC染色;队列4:先前发表中报告的88个PT样本中的批量RNA测序数据用于验证和预后分析(图1a)。
构建了原发性和复发性鼻咽癌的全局肿瘤生态系统图谱,共鉴定出多种主要细胞类型,包括免疫细胞、基质细胞和恶性细胞等(图1b-1d)。与pNPC相比,rNPC呈现独特的免疫生态系统,B细胞比例减少,而成纤维细胞、中性粒细胞和内皮细胞比例增加(图1g),且病灶中的大多数非免疫细胞是恶性细胞(图1e-1f)。
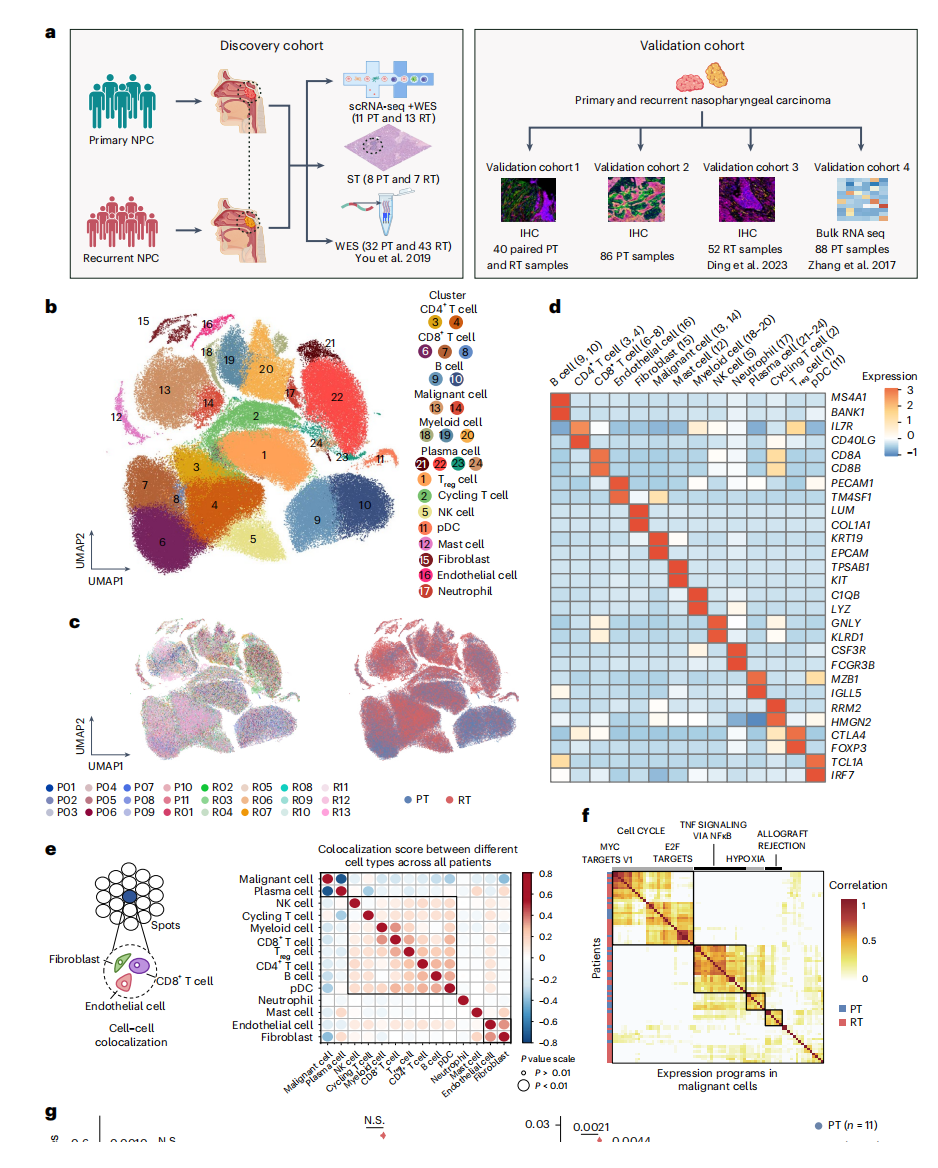
图1 pNPC和rNPC肿瘤微环境的scRNA-seq与空间表达谱分析
Result 2 放疗抵抗和免疫逃逸是rNPC细胞的双重特征
作者针对肿瘤细胞进行组间差异分析,结果显示PT上调基因富集于细胞周期通路,而RT上调基因富集于免疫应答通路,且RT样本展现出更高的免疫炎症和癌症信号,如NF-κB、PI3K-AKT、MAPK和P53通路(图2a-2b)。放疗抗性细胞系的bulk-RNA测序结果也证明RT的放疗抗性与NF-κB、MAPK和PI3K-AKT通路的上调相关(图2c)。此外,RT还体现出更强的免疫逃逸特征,在与免疫逃逸相关的基因中,RT样本的恶性细胞中 CD47 和 HLA-A/HLA-B/HLA-C 表达增加(图2e)。关于肿瘤的抗原性,PT和RT样本之间肿瘤抗原性(包括TMB、TNB和CNV)无显著变化,RT的肿瘤异质性显著低于PT样本(图2f)。关于免疫原性,RT样本中VCAM1的表达更高,而TNFRSF14、CD276、LGALS9和CD274在PT样本中的表达显著增加(图2g)。综上,RT具有高放疗抗性和免疫逃逸的能力,这些能力不依赖于免疫原性和抗原性降低的特定方式存在。
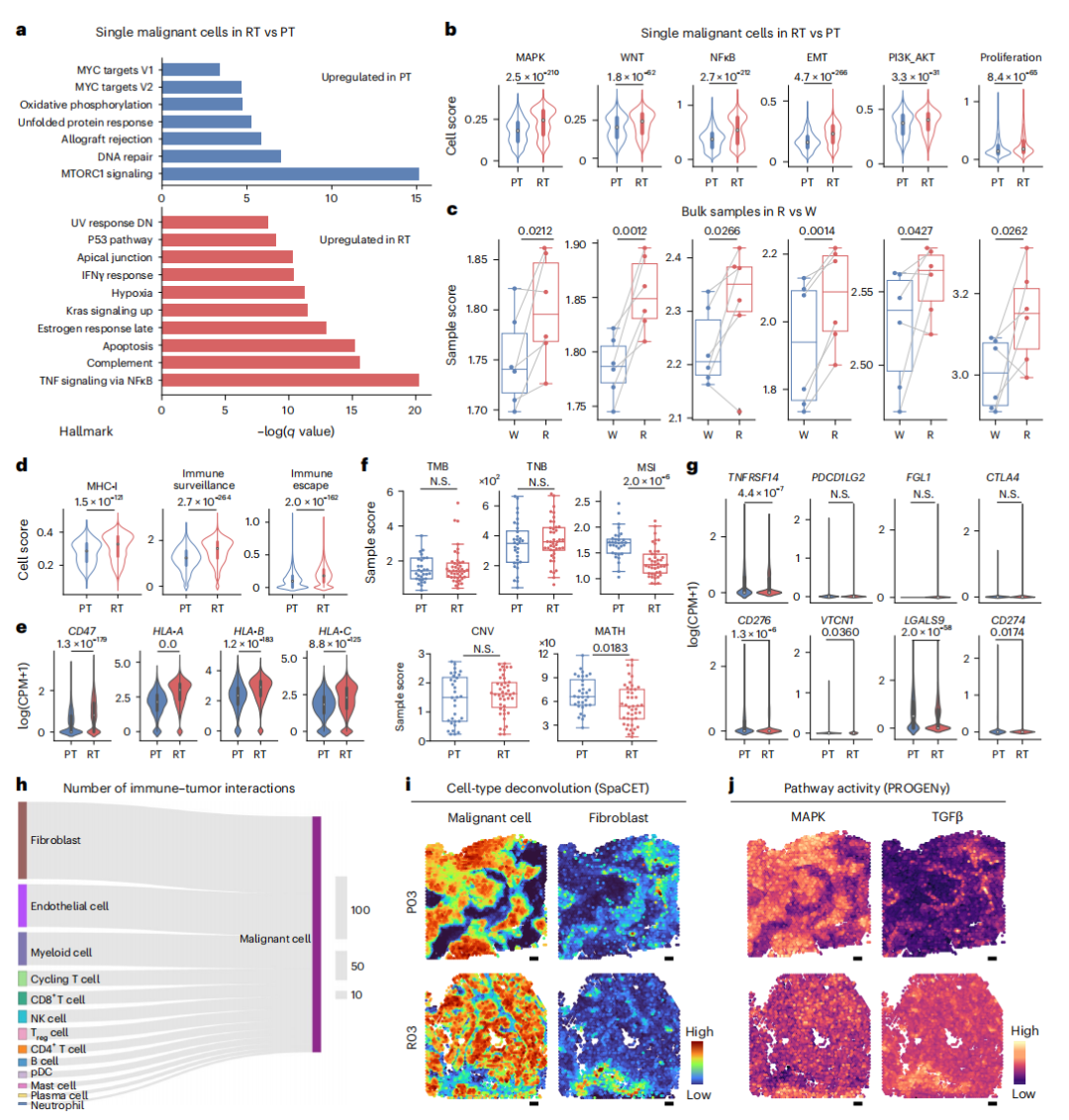
图2 PT与RT样本中恶性细胞的特征及其对肿瘤生态系统的影响
Result 3 MCAMmCAFs促进rNPC细胞的放疗抗性
除了癌症相关通路的自我激活外,TME也可能促进rNPC恶性细胞放疗抗性的发展,细胞通讯分析结果显示,成纤维细胞与恶性细胞的相互作用数量最多(图2h-2j )。通过对成纤维细胞(CAF)进行单细胞聚类分析,识别出四个亚群(图3a-3c),其中MCAM⁺mCAFs在复发性肿瘤(RT)中的比例显著高于原发性肿瘤(PT)(图3d)。该结果经多色免疫荧光技术证实,RT样本中可检测到大量ACTA2和MCAM双阳性成纤维细胞(图3e-f)。流式细胞分析进一步量化显示,RT样本MCAM⁺mCAFs占比中位数高达58.4%,约为PT样本(6.275%)的9倍(图3g)。临床预后分析表明,MCAM⁺mCAFs比例升高与更差的局部区域无复发生存率(LRRFS)和总体生存率显著相关(图3h-i)。
空间转录组分析揭示CAF MCAM亚群较其他CAF亚型显著贴近恶性细胞(P=0.0015),且毗邻CAF MCAM的恶性细胞表现出更强的肿瘤干性特征。从批量CAFs中分离的MCAM⁺mCAFs,并经Western blot验证其纯度(图3j)。当与 MCAM⁺mCAFs共培养时,C666和TWO3鼻咽癌细胞系减弱了γH2AX焦点吸收(图3k),且克隆数量增加,细胞凋亡减弱(图3m)。NCG小鼠皮下共注射模型进一步证实:与MCAM⁺mCAFs共注射的肿瘤在放疗后表现出更强的生长持续性(图3n-p)和凋亡抗性(图3q)。
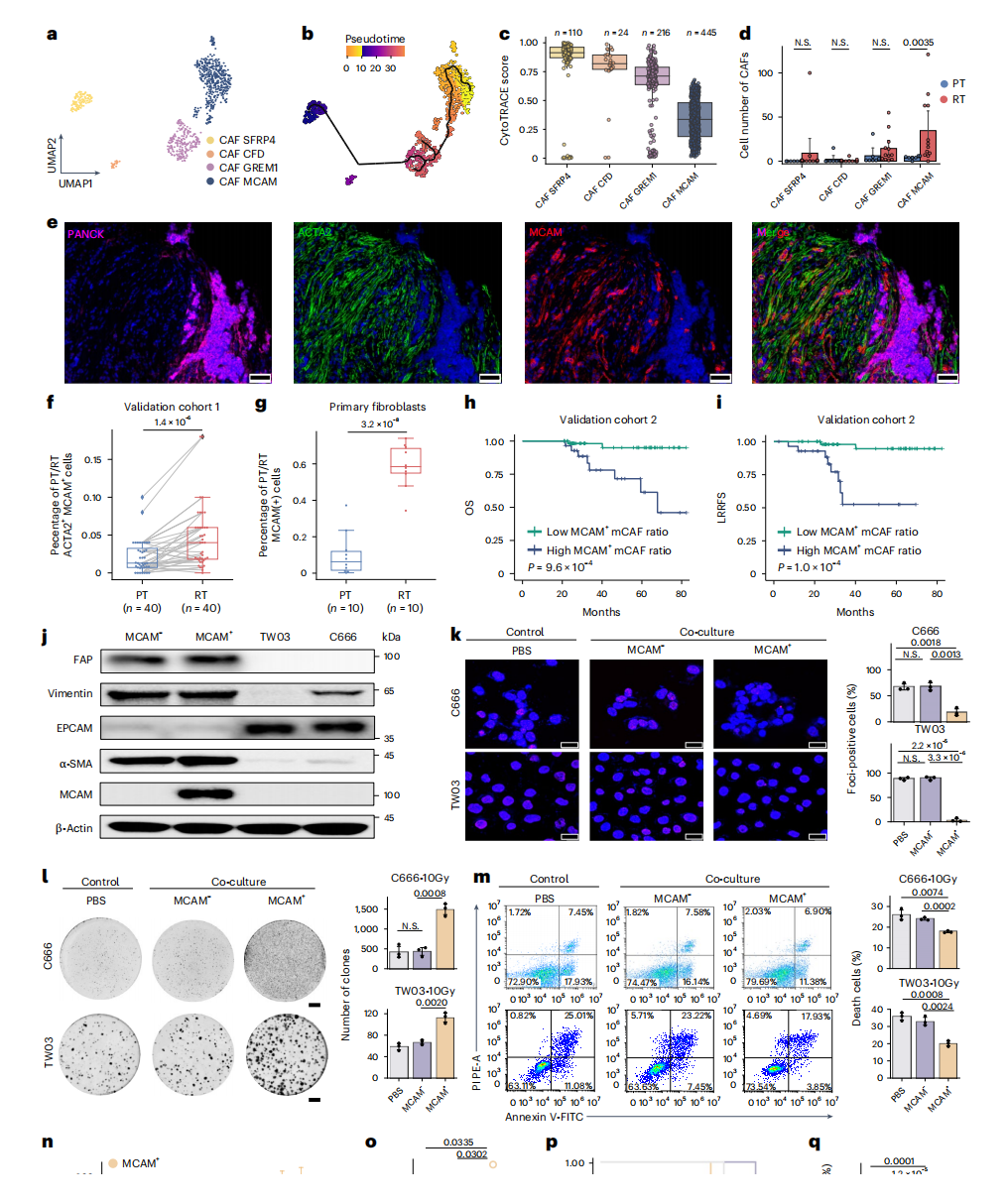
图3 在rNPC中检测到MCAM⁺mCAFs,这些细胞可增强鼻咽癌肿瘤细胞的放射抗性。
Result 4 MCAM⁺ mCAFs 通过COL4-ITGA2-FAK-AKT轴促进放疗抗性
作者通过对在MCAM⁺mCAFs中差异显著的基因进行网络分析,确定ACTA2、COL4A2、ITGA1及COL4A1为潜在的关键枢纽基因,其中分泌蛋白编码基因COL4A1、COL4A2、PDGFA与IGFBP7在单细胞与Bulk-RNA测序数据集均显著富集(图4a-b)。COL4A1和COL4A2编码IV型胶原的α1和α2链,作者发现IV型胶原蛋白在蛋白水平上在MCAM⁺mCAFs中表达上调(图4c,d)。体外实验表明,IV型胶原处理鼻咽癌细胞后,鼻咽癌细胞的放疗抗性显著提高(图4e-h )。整合素是常见的胶原受体,细胞通讯分析表明,恶性细胞与MCAM⁺mCAFs通过COL4A1/2-ITGA2、ITGB1 和 COL4A1/2-ITGA3_ITGB1轴的串扰增强(图4i)。体外实验验证表明,当在C666和TWO3细胞中敲低ITGA2时,显著降低了外源处理IV型胶原诱导的放疗抗性(图4j-4k )。体内实验也表明,ITGA2 KD的肿瘤细胞即使在与MCAM⁺mCAFs共注射并在晚期接受辐照时,其成瘤能力也较弱,且肿瘤细胞凋亡显著增加(图4l-o)。先前的研究表明,胶原主要通过结合整合素激活下游的PI3K-AKT信号通路并发挥其生物学效应,经体内实验验证,当PI3K-AKT通路被抑制时,MCAM⁺mCAFs的促瘤作用显著减弱(图4p-4s)。综上,MCAM⁺mCAFs通过分泌IV型胶原激活肿瘤细胞表面受体ITGA2介导放疗抗性。
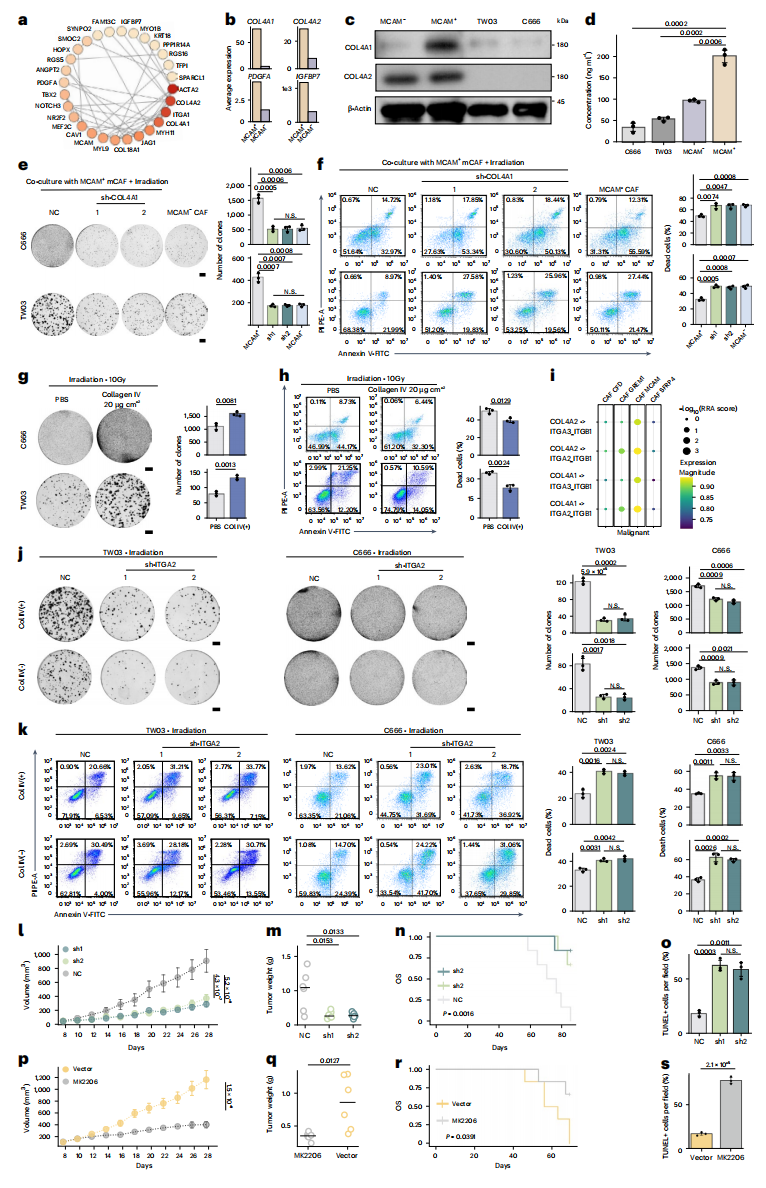
图4 MCAM⁺mCAFs通过COL4-ITGA2-FAK- AKT通路协同增强鼻咽癌肿瘤细胞的放疗抗性
Result 5 胶原IV与鼻咽癌中T细胞抑制和免疫逃逸相关
先前研究表明,胶原可以调节白细胞向肿瘤的浸润,作者研究发现高表达的IV型胶原确实与更少的T细胞浸润相关(图5a),高水平的IV型胶原表达与T细胞浸润呈负相关(图5c),且与较差的总生存期(P=0.031)和更差的局部无复发生存率(LRRFS)(P=0.036)相关(图5d-5e)。一致地,更高的COL4A1转录水平与T细胞相关基因的较低表达显著相关(图5g),且与显著更差的的无进展生存期相关(图5f)。人源化小鼠模型中,与共注射MCAM⁺mCAFs或PBS对照相比,当共注射COL4A1敲除(KO)的MCAM⁺mCAFs时,肿瘤细胞成瘤能力较弱(图5h-5j )。此外,在COL4A1 KO组和载体(vector)组中,MCAM和α-SMA的表达均高于PBS组,而载体组中的IV型胶原表达高于COL4A1 KO组和PBS组(图5k-5l)。在免疫荧光染色和流式细胞术分析中,载体组中CD4⁺和CD8⁺T细胞的比例显著低于COL4A1 KO组和PBS组(图5m,)。此外更高的IV型胶原评分与CD4⁺ T细胞(r=-0.523, P=0.026)和CD8+T细胞(r= -0.752, P=0.0003)的浸润降低显著相关(图5n)。综上所述,IV型胶原通过显著抑制T细胞浸润,介导鼻咽癌免疫逃逸,导致患者生存预后恶化。

图5 鼻咽癌患者瘤内IV型胶原水平与T细胞抑制及免疫逃逸相关
Result 6 复发性鼻咽癌中存在具有弱细胞毒性的ZNF683⁺CD8⁺T细胞
在比较原发(PT)和复发(RT)鼻咽癌样本的TME差异时,作者发现rNPC中CD8⁺ZNF683⁺T细胞和CD8⁺PNRSR⁺T细胞的丰度显著高于pNPC(图6b)。通过Monocle 3的拟时序分析揭示了CD8⁺T细胞的分化轨迹:该过程起始于CD8⁺TCF7⁺T细胞,经历以CD8⁺FOSB⁺和CD8⁺ITM2C⁺为特征的中间细胞毒性状态,最终分化为两个终末亚群——CD8⁺TIGIT⁺的耗竭性T细胞与CD8⁺ZNF683⁺的记忆性T细胞(图6c)。在此分化过程中,细胞毒性和耗竭特征评分同步升高(图6d)。值得注意的是,初始CD8⁺TCF7⁺细胞主要分布于CD8⁺ ZNF683⁺细胞比例较低的原发肿瘤中,而CD8⁺ZNF683⁺细胞则在复发肿瘤中富集并呈现组织驻留特征(图6c-6e)。进一步分析表明,PT和RT样本间T细胞耗竭评分无统计学差异,但复发肿瘤中T细胞的共刺激功能显著减弱(图6f-6g)。在临床验证队列1中,RT样本的CD8⁺ZNF683⁺细胞比例显著升高(图6h-6i)。队列2的生存分析显示,该细胞高比例患者的总生存期(OS)和局部无复发生存期(LRRFS)显著缩短(图6j)。为解析其功能特性,研究者分离肿瘤浸润的CD8⁺ZNF683⁺和CD8⁺ZNF683⁻细胞群,通过流式细胞术检测细胞毒性标志物颗粒酶B(GZMB)的表达。结果显示CD8⁺ZNF683⁺细胞的GZMB表达显著降低,证实其细胞毒性功能减弱(图6k)。
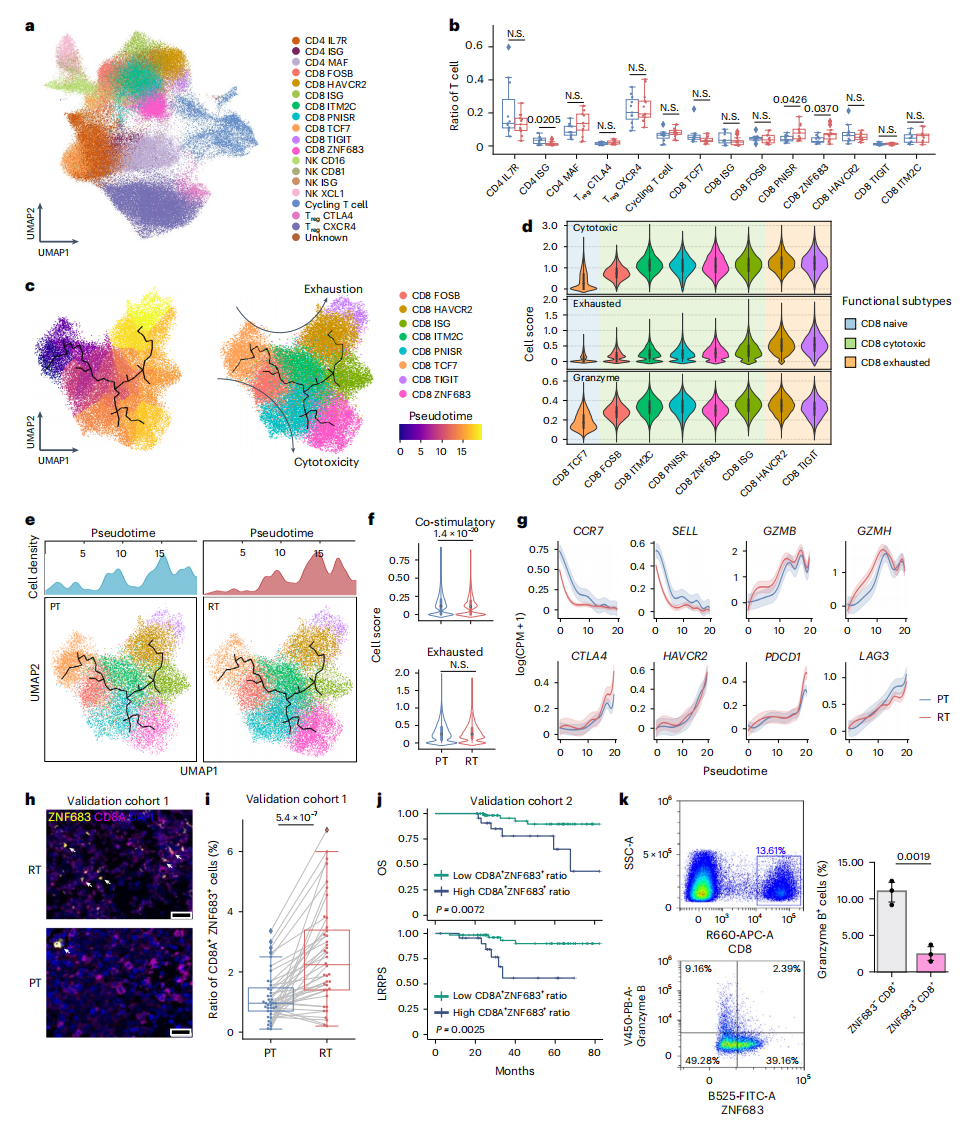
图6 CD8⁺T细胞在rNPC中保持弱细胞毒性的记忆表型
Result 7 复发性鼻咽癌中三级淋巴结构减少
作者先前观察到B细胞在复发性鼻咽癌中的比例显著减少,通过降维聚类分析,将B细胞分为五个亚群,其中,记忆B细胞在复发性鼻咽癌中的比例显著减少,而 B IGHM细胞的比例增加(图7a- 7e)。空间转录组学进一步揭示,pNPC中的CD4⁺T细胞、CD8⁺T细胞、调节性T细胞和循环T细胞普遍更靠近B细胞(图7f)。组织学检测显,pNPC样本中肿瘤相关淋巴结构(TLS)阳性率达62.5%(5/8),而rNPC样本未见TLS阳性(0/7)(图7g),且TLS内观察到CD20+B细胞与T细胞亚群及滤泡树突状细胞共定位(图7h)。在验证队列中进一步证实,PT样本中的TLS密度高于RT样本(图7i),较高的TLS密度与显著更好的生存结局相关(图7j-7k),TLS状态为阴性的患者在接受抗 VEGFR 和PD-1抑制剂治疗后,无进展生存期结果更差(图7l)。

图7 rNPC中TLSs的含量显著降低
Result 8 CD47-SIRPα相互作用抑制复发性鼻咽癌中的抗原呈递
作者进一步在髓系谱系中鉴定出11个亚群,包括5个巨噬细胞亚群,1个单核细胞亚群,4个树突状细胞亚群和一个活跃增殖细胞亚群(图8a-8b)。单核细胞 FCN1表现出FCN1、VCAN、S100A8和S100A9的高表达,且在复发性鼻咽癌中的比例高于原发性鼻咽癌(图8c-8d)。多色免疫荧光染色验证了RT样本与PT样本相比,单核细胞 FCN1的丰度增加(图8e-8f)。 基于空间转录组学分析显示,与原发性鼻咽癌相比,髓系细胞在复发性鼻咽癌中明显更靠近肿瘤细胞,并表现出更显著的相互作用对(图8g)。细胞通讯表明,rNPC中恶性细胞与髓系细胞通过CD47- SIRPα 存在更密切的相互作用(图8h)。此外,在RT样本中,靠近CD47阳性恶性细胞的髓系spots显示出显著更高的 SIRPα 表达水平(图8i)。多色IHC同时证实SIRPα⁺CD1C⁺树突细胞定位于CD47⁺复发恶性细胞周边(图8j)。
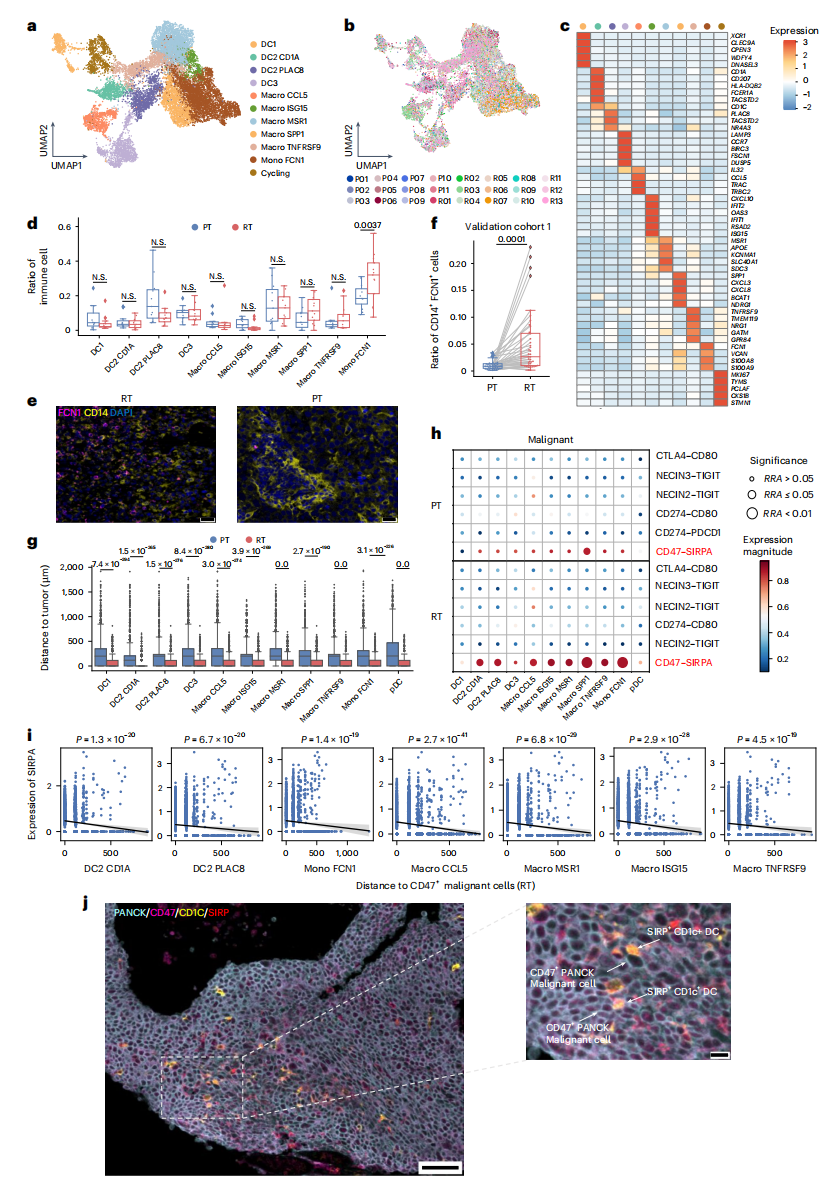
图8 SIRPα⁺髓系细胞聚集在CD47⁺恶性细胞附近,可能抑制rNPC中的抗原呈递
研究结论
本研究通过单细胞和空间转录组学技术,系统研究了复发鼻咽癌(rNPC)中放疗抵抗和免疫逃逸的分子机制。rNPC中MCAM⁺癌症相关成纤维细胞(CAFs)显著富集,并通过COL4-ITGA2-FAK-AKT轴促进放射抵抗。此外,COL4的高表达抑制了T细胞浸润,导致免疫逃逸,该研究为改善rNPC患者的预后提供了新的思路和方法。

参考文献:
You, R., Shen, Q., Lin, C. et al. Single-cell and spatial transcriptomics reveal mechanisms of radioresistance and immune escape in recurrent nasopharyngeal carcinoma. Nat Genet 57, 1950–1965 (2025). https://doi.org/10.1038/s41588-025-02253-8






