前言
2025年12月30日,中南大学湘雅医学院附属株洲医院肿瘤免疫代谢研究所(TIMI)李昱堃、南华大学第二附属医院临床研究所高安博等研究团队合作,在npj Digital Medicine杂志发表最新研究成果《Machine Learning-Enabled Spatial Multi-Omics Uncovers Lactate-Driven Targets and Tumor Microenvironmental Reprogramming in Cancer》。
本研究通过整合单细胞转录组、空间转录组、空间代谢组等多组学技术,结合TCGA生存数据与机器学习模型,系统解析了乳酸在肺腺癌中的空间异质性及细胞特异性调控作用。本研究从空间维度揭示了乳酸通过代谢—血管—免疫轴重塑肿瘤微环境的机制,研究为靶向乳酸信号及其下游通路提供了新的治疗策略与生物标志物。欧易生物提供了该项目的单细胞转录组、空间转录组和空间代谢组测序实验和分析工作,文章特别致谢欧易生物谭裕智、于俊浩、施淼、徐振宇和王恒允在分析中提供的帮助。

发表期刊:npj Digital Medicine
影响因子:15.1
发表年月:2025年12月
材料:高、低循环乳酸水平的LUAD手术样本分别做单细胞转录组、空间转录组、空间代谢组(n=3)
方法:10x Genomics单细胞转录组测序、10x空间转录组测序、空间代谢组
DOI:10.1038/s41746-025-02286-7.
研究背景
肺癌是全球癌症相关死亡的主要原因,其中肺腺癌(LUAD)是最常见的非小细胞肺癌亚型。尽管早期诊断和靶向治疗已取得进展,但肿瘤异质性与治疗抵抗仍是临床面临的重大挑战。肿瘤微环境(TME)的代谢重编程是肿瘤异质性的核心特征之一。乳酸,作为瓦博格效应的主要产物,传统上被视为代谢废物,现已被广泛认为是一种关键的信号分子和免疫代谢调节因子。在LUAD等实体瘤中,乳酸累积会形成酸性、免疫抑制的微环境,损害T细胞功能,促进M2型巨噬细胞极化,并通过HIF-1α等途径激活内皮细胞,驱动血管生成。然而,乳酸在肿瘤组织内的空间分布异质性及其对不同细胞类型的特异性影响机制仍不清楚。阐明乳酸如何时空特异性重塑TME,对于理解肿瘤进展和开发新的治疗策略至关重要。
研究内容
本研究根据患者血液乳酸水平将LUAD组织分为高乳酸组和低乳酸组,采用空间多组学整合策略,结合单细胞转录组测序、10x Visium空间转录组、质谱成像空间代谢组以及机器学习模型,深入探究了乳酸异质性在肺腺癌微环境中的作用。此外,多种机器学习模型(随机森林、弹性网络、SVM、ANN等)分析一致将成纤维细胞和内皮细胞识别为区分高/低乳酸状态的最重要特征,并构建出能有效预测患者生存风险的乳酸相关基因模块。
本研究系统描绘了乳酸通过驱动代谢重编程、血管生成和免疫抑制,在空间上重塑LUAD微环境的全景图谱,为靶向乳酸信号轴的治疗策略提供了新靶点和预后工具。
技术路线
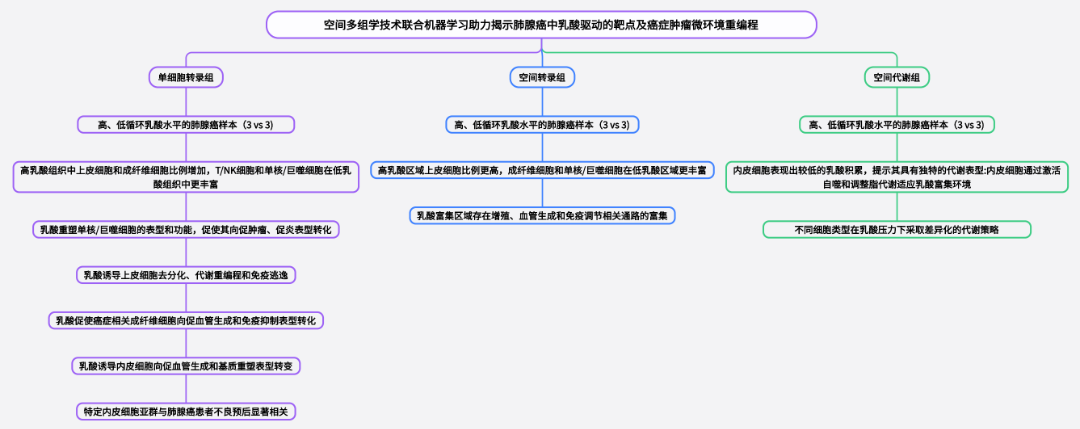
研究结果
Result 1 单细胞转录组学分析揭示肺腺癌与乳酸水平相关的独特细胞及分子特征
本研究通过整合单细胞转录组测序、空间转录组学和空间代谢组学技术,对高乳酸和低乳酸肺腺癌(LUAD)样本进行系统解析(图1A)。通过单细胞RNA测序分析发现高乳酸组织中上皮细胞和成纤维细胞比例增加,而T/NK细胞和单核/巨噬细胞则更多富集于低乳酸组(图1E)。细胞组间差异分析显示,高乳酸T/NK细胞中应激反应基因表达上调,而抗原呈递相关基因表达下降,提示乳酸可能抑制T细胞的免疫监视功能(图1F-H)。高乳酸内皮细胞中血管生成相关通路(如淋巴管发育、血管生成)激活,且与上皮细胞之间的通讯关系增强。
综上,乳酸通过调控细胞组成、增强促血管生成信号和抑制免疫细胞功能,塑造了一个支持肿瘤进展的微环境。
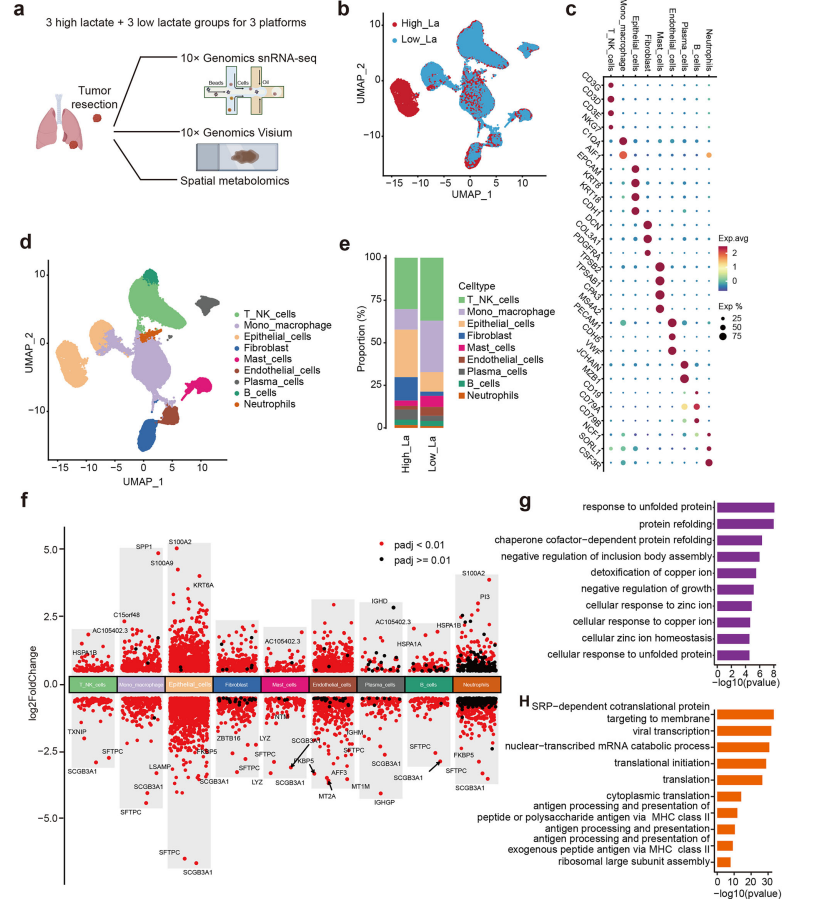
图1.单细胞转录组学分析揭示肺腺癌与乳酸水平相关的独特细胞及分子特征
Result 2 乳酸驱动单核细胞/巨噬细胞亚型转录与功能重编程
单核细胞与巨噬细胞是肿瘤微环境中免疫稳态和炎症的核心调节因子,通过单细胞转录组分析发现高乳酸单核/巨噬细胞中炎症反应、细胞周期和吞噬相关通路显著激活,而组织结构维持和细菌应答通路则受到抑制(图2A,B)。亚群聚类分析识别出一个在高乳酸条件下显著富集的巨噬细胞亚群-CLUSTER5,该亚群高表达促肿瘤基因,功能富集显示其参与糖酵解和免疫调节(图2C-G)。拟时序分析进一步表明,高乳酸条件改变了该亚群的分化路径(图2H,I)。细胞通讯分析揭示SPP1信号通路在高乳酸样本中显著增强,而EGF通路则在低乳酸样本中占主导(图2J)。
以上结果说明,乳酸不仅重塑巨噬细胞的转录状态,还通过调节其与其他细胞的相互作用,推动其向促肿瘤、促炎症表型转化。
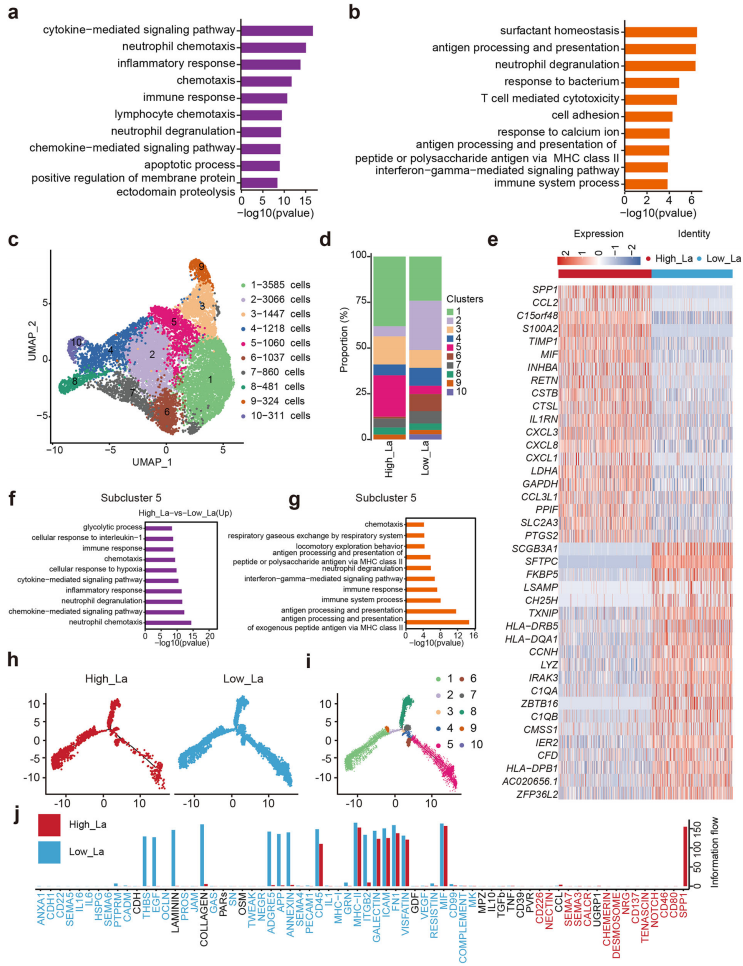
图2. 乳酸驱动单核细胞/巨噬细胞亚型转录与功能重编程
Result 3 乳酸诱导上皮细胞去分化、代谢重编程和免疫逃逸
基因功能富集分析显示,高乳酸上皮细胞中内质网应激、蛋白质合成和病毒转录等分泌和应激相关通路上调,而肺泡分化和线粒体呼吸功能相关基因表达下降,提示上皮细胞发生去分化并转向糖酵解代谢(图3A,B)。亚群分析识别出一个在高乳酸富集的上皮亚群-CLUSTER5,表达应激和代谢适应基因,该亚群中肺泡分化标记物下调,抗原呈递功能受损。拟时序结果显示其在高乳酸组中表现出与低乳酸组不同的发育路径。细胞间通讯分析进一步发现,高乳酸条件下上皮细胞通过SPP1、CD99、THBS等通路增强与周围细胞的相互作用,促进细胞黏附和免疫调节。
这些发现表明,乳酸通过诱导上皮细胞去分化、代谢重编程和增强基质交互,从而促进肿瘤进展并增强治疗耐药性。
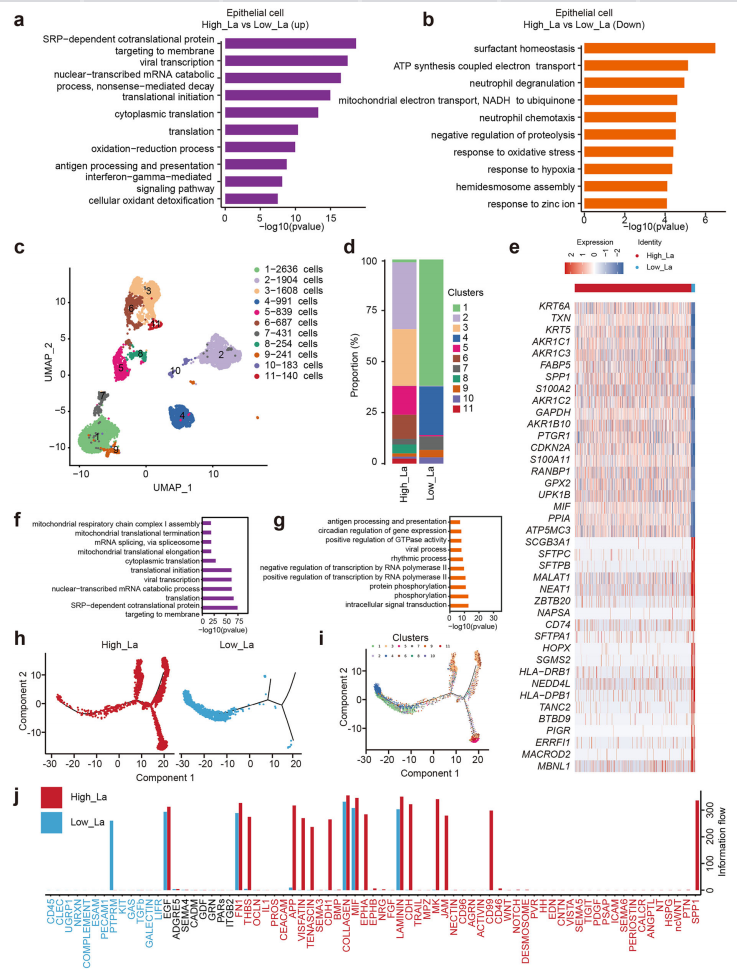
图3. 乳酸诱导上皮细胞去分化、代谢重编程和免疫逃逸
Result 4 高乳酸肿瘤微环境中成纤维细胞的表型转变
乳酸在肿瘤微环境中能显著改变癌症相关成纤维细胞(CAFs)的功能状态。差异分析表明,高乳酸来源的成纤维细胞中细胞黏附、肿瘤坏死因子应答和NF-κB信号通路上调,而抗原呈递和细胞外基质组织相关基因表达下降(图4A,B)。亚群分析揭示一个在高乳酸样本中显著富集的成纤维细胞亚群-CLUSTER1,其特征是促血管生成和基质重塑基因的高表达,同时钙离子转运和氧应激反应通路受到抑制(图4C-G)。细胞通讯网络分析进一步显示,高乳酸环境成纤维细胞通过SPP1、THBS、NOTCH等信号通路增强了其对内皮细胞和免疫细胞的调控作用(图4H)。
这些结果表明,乳酸水平升高会促使成纤维细胞功能从免疫调节和结构维持转向促肿瘤发生、促血管生成及基质重塑的表型,从而可能促进肿瘤进展并增强对免疫监视的抵抗能力。
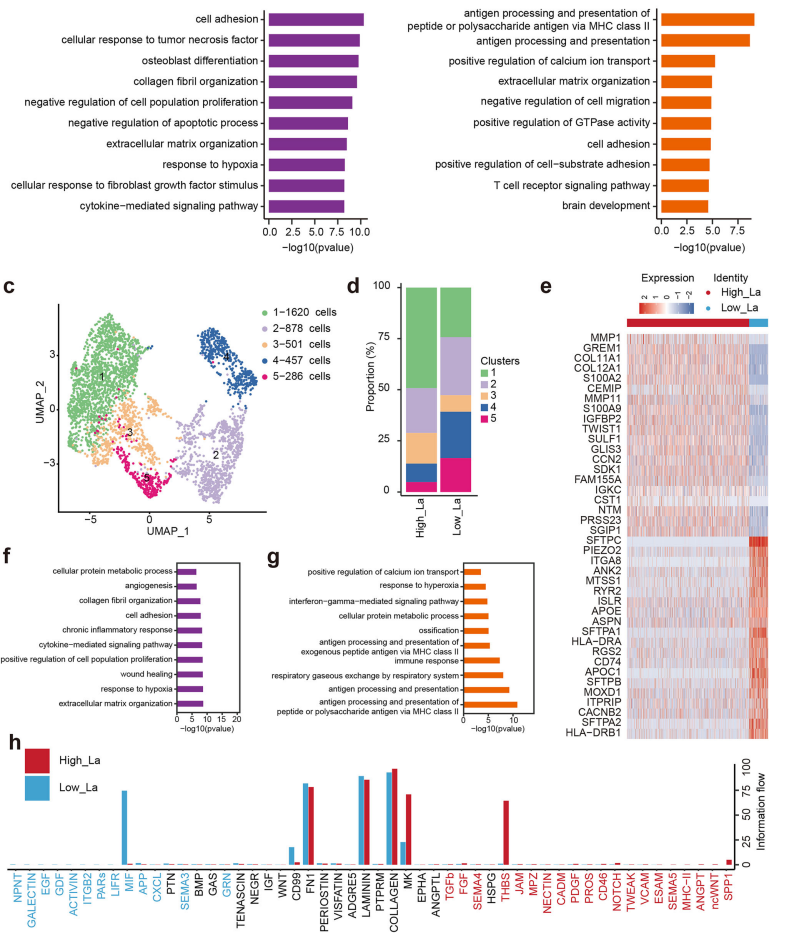
图4. 高乳酸肿瘤微环境中成纤维细胞的表型转变
Result 5 乳酸诱导内皮细胞向促血管生成和基质重塑表型转变
通过单细胞亚群分析得到13个内皮细胞亚群,其中CLUSTER1在高乳酸样本中显著富集,表达促血管生成基因和应激应答基因,功能富集显示其参与血管生成和细胞外基质重塑(图5A)。拟时序分析进一步揭示内皮细胞在高乳酸条件下向血管生成谱系分化。细胞通讯显示VEGF、NOTCH、EPHA等通路在高乳酸样本中增强。
综上,肿瘤微环境中乳酸的积累会促使内皮细胞重编程为促血管生成和重塑状态,可能促进肿瘤进展和免疫逃逸。
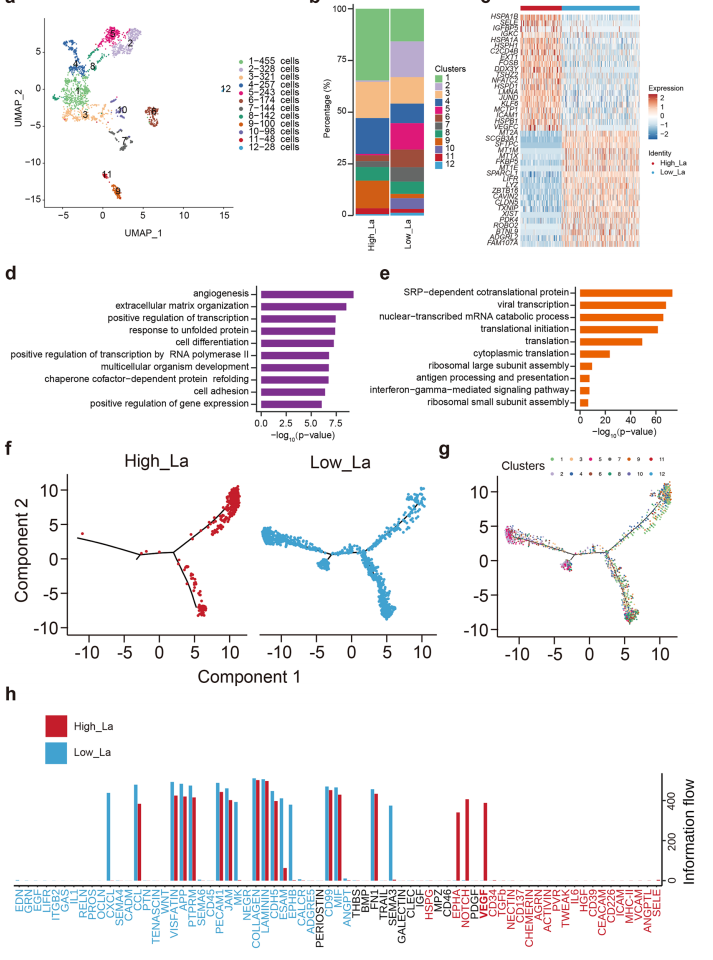
图5. 乳酸诱导内皮细胞向促血管生成和基质重塑表型转变
Result 6 空间多组学整合揭示肺腺癌富集的细胞类型特异性响应及代谢动态
通过整合空间转录组学和空间代谢组学数据,本研究系统解析了乳酸在肺腺癌组织中的细胞类型特异性和代谢异质性。空间图谱显示,高乳酸区域上皮细胞比例较高,而成纤维细胞和单核/巨噬细胞更多分布于低乳酸区域。不同细胞类型在高乳酸条件下表达谱发生特异性变化,如上皮细胞去分化、巨噬细胞促炎化、成纤维细胞促血管化。空间亚群分析识别出多个乳酸敏感的细胞亚群,这些亚群在高乳酸样本中显著扩张并富集到血管生成、细胞周期和炎症相关通路(图6)。
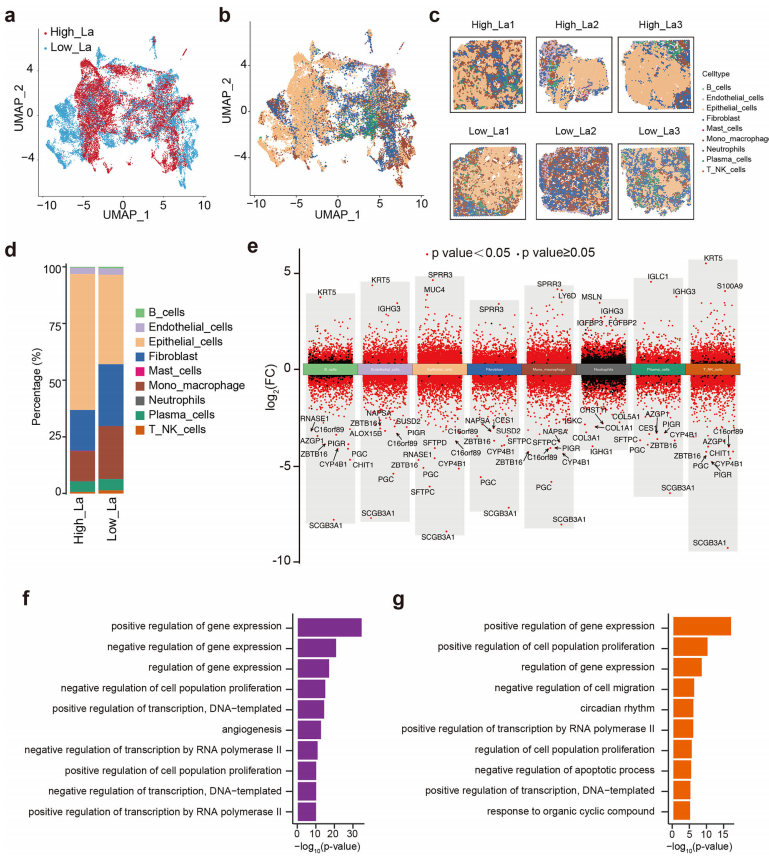
图6. 空间转录组图谱揭示乳酸富集肺腺癌组织中的细胞类型特异性响应
代谢成像分析确认高乳酸组整体乳酸水平显著高于低乳酸组,且乳酸分布呈现明显的空间梯度。有趣的是,尽管高乳酸组中多数细胞类型乳酸含量升高,内皮细胞却表现出较低的乳酸积累,提示其具有独特的代谢表型。丙酮酸分析进一步揭示,低乳酸组整体丙酮酸水平较高,而高乳酸组中免疫细胞和上皮细胞的丙酮酸含量下降,成纤维细胞则呈现升高趋势,反映不同细胞类型在乳酸压力下采取差异化的代谢策略。内皮细胞特异性代谢谱分析发现,高乳酸条件下自噬相关代谢物上调,而胆碱代谢和突触相关代谢物下调,提示内皮细胞通过激活自噬和调整脂代谢适应乳酸富集环境(图7)。
这些发现揭示了乳酸在肿瘤微环境中调控代谢重编程的空间复杂性和细胞类型特异性。
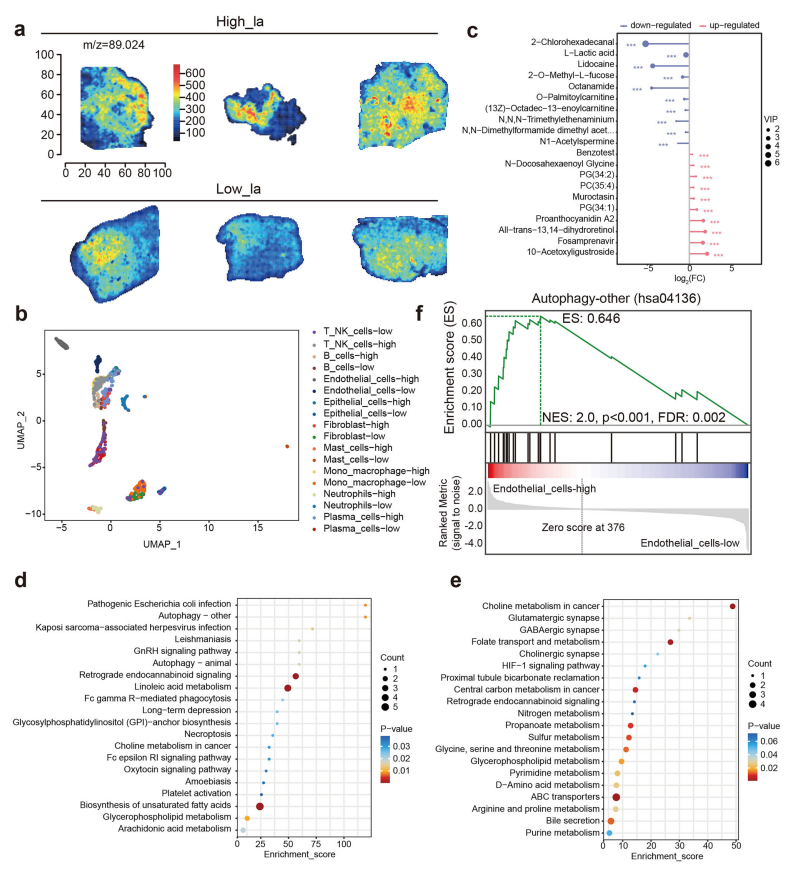
图7. 空间多组学整合揭示肺腺癌中乳酸相关的代谢动态
Result 7 特定内皮细胞亚群与肺腺癌患者不良预后显著相关
结合单细胞转录组数据和TCGA临床队列,本研究深入探讨了不同内皮细胞亚群在肺腺癌预后中的意义。生存分析显示,内皮细胞亚群1和亚群9的富集与患者总生存期显著缩短相关,其中亚群9的预后关联尤为强烈(图8A,B)。基因功能分析表明,亚群1高表达血管生成和细胞黏附相关基因,低表达氧化还原和脂代谢通路基因;亚群9则富集未折叠蛋白应答和热应激基因,下调翻译起始和抗原呈递通路。这些转录特征提示,高乳酸诱导的内皮亚群倾向于促血管生成、应激适应和免疫调节表型(图8C,D)。免疫荧光实验进一步验证,高乳酸肺腺癌组织中内皮标记物FN1、ENG和MMP2表达增强,血管密度显著升高。
综合表明,乳酸通过促进促血管生成和应激适应内皮亚群的扩张,加剧肿瘤进展和不良预后,为内皮靶向治疗提供了潜在切入点。
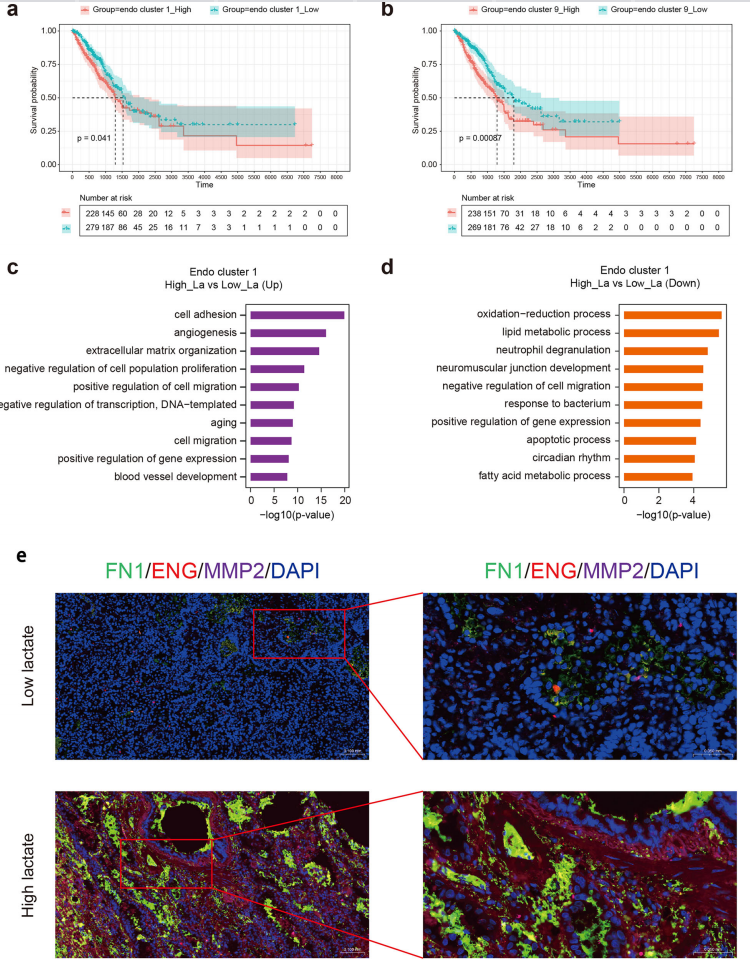
图8. 特定内皮细胞亚群与肺腺癌患者不良预后显著相关
研究结论
1. 乳酸诱导内皮细胞发生促血管生成和应激适应的转录重编程,并与不良预后显著相关。
2. 乳酸通过调节肿瘤相关巨噬细胞和成纤维细胞的功能状态,促进免疫抑制和基质重塑。
3. 空间多组学揭示乳酸富集区域表现出协调的代谢和转录重编程,特征为血管生成、代谢转换和免疫抑制。
4. 机器学习模型一致识别成纤维细胞和内皮细胞是乳酸富集状态的核心决定因素,并构建出具有预后预测能力的基因模块。
参考文献:
Tan Y, Tan W, Liang Y, Long Y, Chen S, Hu Q, Ou Y, Fu J, Chen H, Ren F, Ye J, Zhou Q, Li S, He X, Wang Q, Shen Y, Lu H, Wu D, Gao A, Chen X, Li Y. Machine learning-enabled spatial multi-omics uncovers lactate-driven targets and tumor microenvironmental reprogramming in cancer. NPJ Digit Med. 2025 Dec 30. doi: 10.1038/s41746-025-02286-7. Epub ahead of print. PMID: 41469480.






