前言
免疫球蛋白超家族成员9(IGSF9)已被报道可结合T细胞表面未知蛋白,并抑制T细胞增殖与活化,促进肿瘤免疫逃逸。肿瘤相关巨噬细胞(TAMs)作为肿瘤浸润免疫细胞中最丰富的群体,在形成免疫抑制性肿瘤微环境过程中发挥关键作用。但IGSF9是否也与TAMs结合,会不会影响TAMs功能,以及如何促进肿瘤免疫微环境形成?其具体机制尚未明确。
近日,滨州医学院李尊岭教授团队在Journal for Immunotherapy of Cancer发表的最新研究“Tumor-associated macrophages educated by IGF9 exhibit a senescence-associated secretory phenotype to promote tumor immune escape”,揭示了IGSF9通过与TMUB1互作,激活IL-6/STAT3通路,进而诱导肿瘤相关巨噬细胞进入衰老状态,促进肿瘤免疫逃逸的新机制。
欧易生物在本项目中提供了膜体系酵母文库构建与筛选服务。

文库与诱饵
酵母文库:人_PBMC
诱饵蛋白:IGSF9
筛选方法:酵母双杂交(膜体系)
验证方法:免疫荧光成像(共定位)/Co-IP/GST-pull down等
研究结果
1. 衰老样巨噬细胞在IGSF9高表达的肺癌组织中增多
通过分析肺癌单细胞及空间转录组数据(GSE189487),发现在IGSF9高表达的肿瘤区域(如TD1和TD2样本),肿瘤相关巨噬细胞(TAMs)表现出显著升高的衰老评分(图1)。这些TAMs不仅富集了典型的衰老相关基因(如CDKN2A, CDKN2B),还高表达多种免疫抑制标志物(如ARG2, CD163, IDO1)。基因集富集分析(GSEA)显示,这些衰老样TAMs中IL-6/JAK/STAT3等促肿瘤和免疫抑制通路被显著激活。空间邻近性分析进一步揭示,衰老样TAMs在空间位置上更接近IGSF9⁺的肿瘤细胞,而与效应CD8⁺ T细胞则距离较远。这些结果从空间和单细胞层面证实了IGSF9表达与TAMs衰老及免疫抑制表型的强相关性。
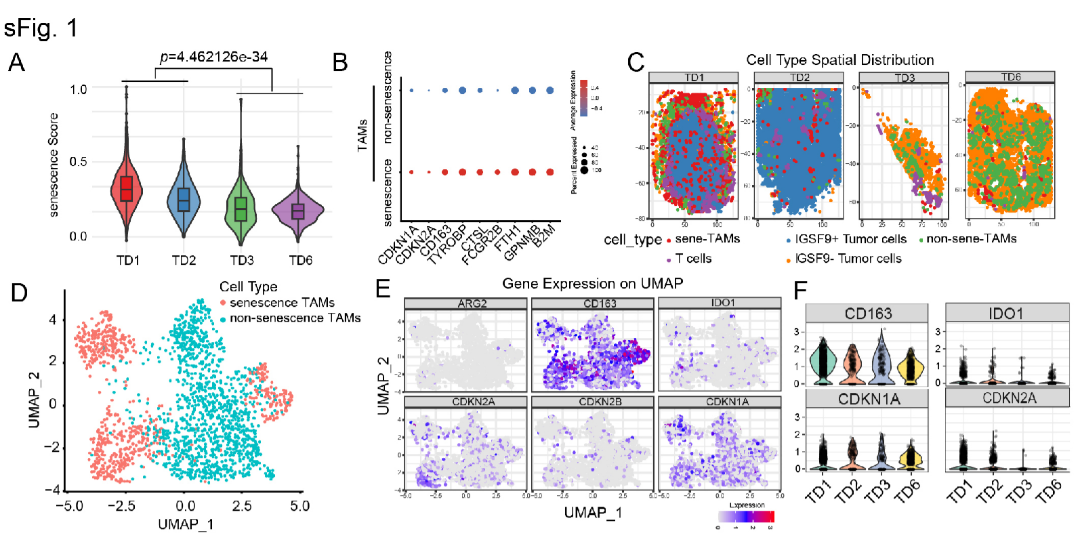
图1.肿瘤中衰老性与非衰老性TAMs的空间定位与UMAP图
2. IGSF9与巨噬细胞结合并驱动其向免疫抑制与衰老状态转化
通过流式细胞术发现,IGSF9的胞外域(ECD)能特异性结合人及小鼠的单核/巨噬细胞,且与患者来源细胞的结合更强。功能上,这种结合导致巨噬细胞表面关键的免疫激活分子(CD86, MHC-II)下调,而抑制性分子(PD-L1)上调,并显著抑制T细胞增殖。转录组分析揭示了其分子机制:IGSF9处理广泛上调了巨噬细胞中免疫抑制相关基因(如IL10, TGFB1)和衰老相关基因(如CDKN1A)的表达(图2A)。通路富集分析表明,IL-6/JAK/STAT3、IL-10、TGF-β等促进免疫抑制与衰老的信号通路被显著激活,而细胞周期通路则受到抑制(图2)。qPCR进一步验证了衰老与细胞周期调控基因的表达改变(图2H)。这些研究结果表明,经IGSF9诱导的巨噬细胞会向免疫抑制和衰老表型发生显著极化,从而促进抑制性肿瘤微环境的形成。
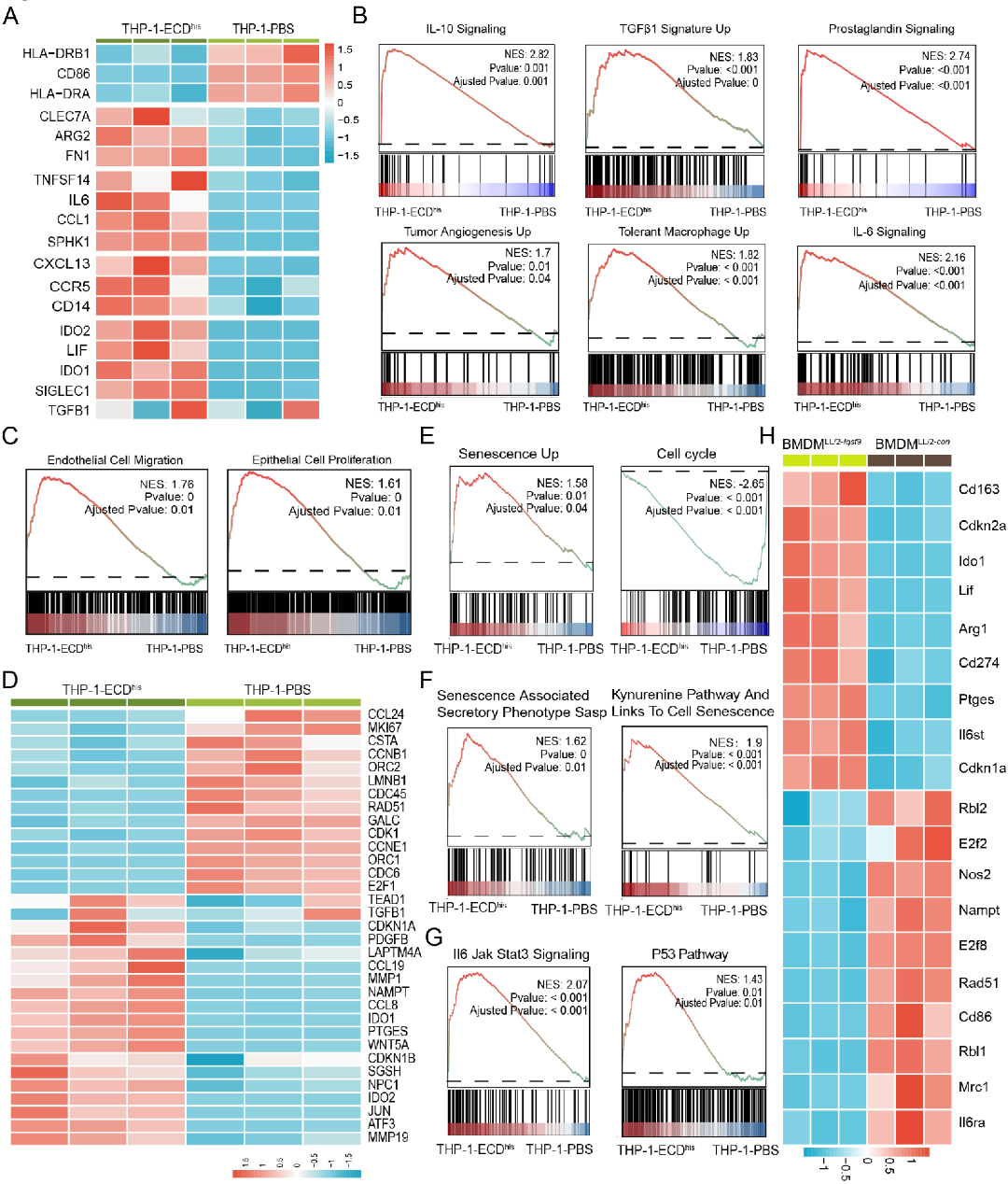
图2. IGSF9- ECD上调了免疫抑制基因和衰老基因的表达水平
3. IGSF9通过损害细胞功能并激活IL-6/STAT3通路诱导巨噬细胞衰老
通过免疫成像、细胞流式及活细胞成像技术等研究发现,IGSF9处理的巨噬细胞吞噬能力显著下降,细胞骨架紊乱,细胞迁移速度减慢,表现出“懒散”的运动模式。在表型与机制层面,这些细胞同时呈现出典型的衰老特征:细胞体积增大、SA-β-gal活性升高、增殖标志物Ki67减少、而衰老标志物P21/P53显著增加(图3A-E)。免疫荧光显示衰老相关因子(P53, P21, HMGB1)上调,DNA修复/核纤层蛋白(RAD51, LaminB1)下调(图3F-H)。这些功能衰退与衰老表型的背后,是IL-6/STAT3信号通路的强力激活,表现为STAT3磷酸化(p-STAT3)水平显著升高(图3I-K)。关键性验证实验表明,使用中和性抗IL-6抗体可以同时逆转IGSF9诱导的p-STAT3升高、P21表达增加以及CD86hiMHC-IIhi巨噬细胞比例的下降(图3L-N)。这共同证明,IGSF9通过激活IL-6/STAT3这一核心通路,促进巨噬细胞衰老。
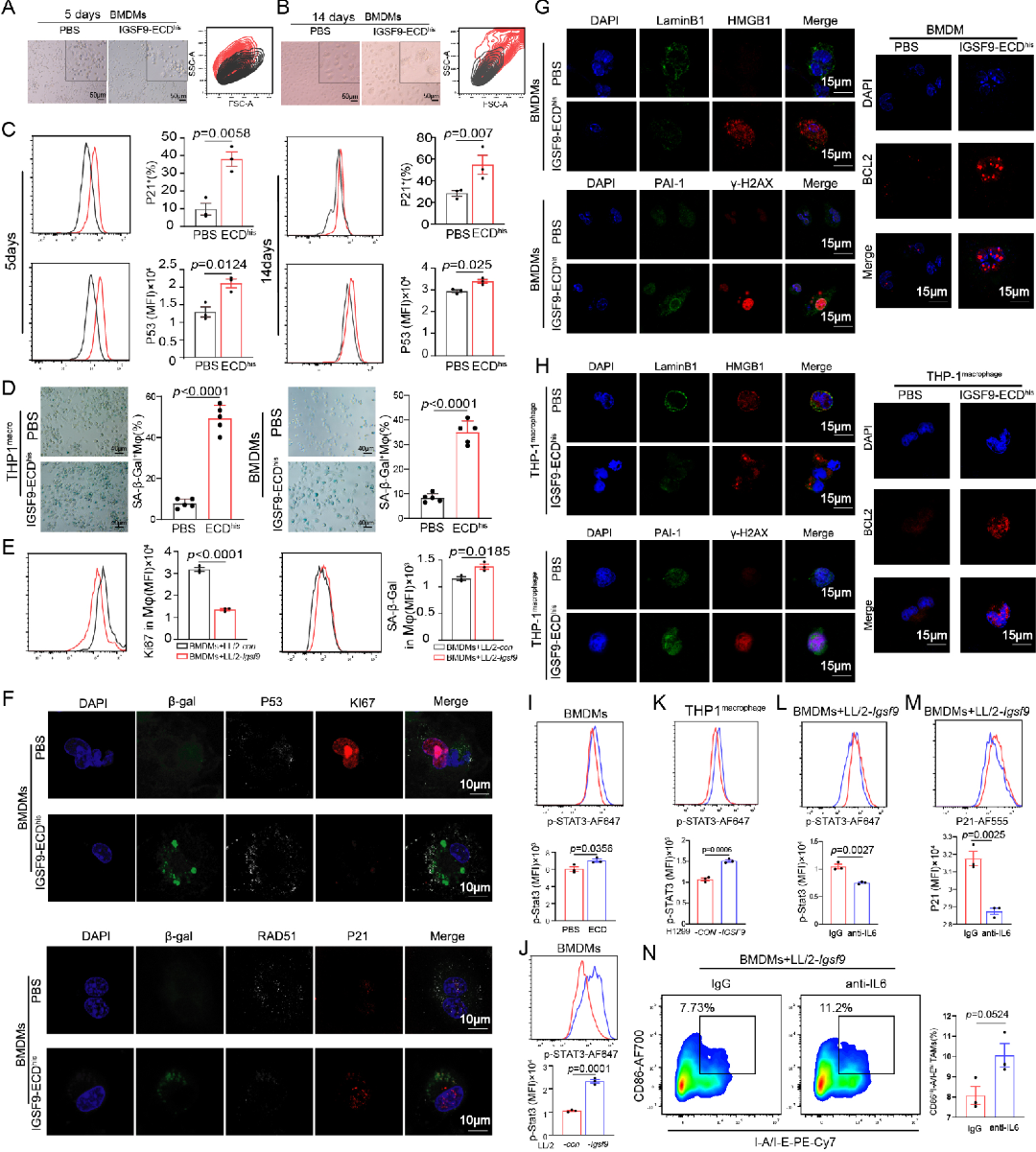
图3. IGSF9通过IL-6/JAK/STAT3信号通路促进巨噬细胞衰老
4. IGSF9通过与TMUB1互作激活IL-6/STAT3信号通路并诱导巨噬细胞衰老
为阐明IGSF9巨噬细胞表面的相互作用受体蛋白。研究以IGSF9为诱饵,采用膜系统酵母双杂交筛选技术,从人PBMC cDNA文库中鉴定出跨膜泛素样结构域蛋白1(TMUB1)为候选互作蛋白(图 4A-B)。流式细胞术显示TMUB1在多种髓系细胞系(U-937, THP-1, MV4-11)高表达,并能与IGSF9-ECD结合(图 4C)。免疫荧光实验证实了IGSF9与TMUB1在细胞内的共定位(图 4D-F)。通过免疫共沉淀(Co-IP)和GST pull-down实验,在体外和细胞膜蛋白提取物中均验证了IGSF9与TMUB1之间存在直接的物理相互作用(图 4G-H)。功能上,在U-937细胞中过表达TMUB1能增强IGSF9对IL-6/p-STAT3通路的激活;反之,利用siRNA敲低THP-1或U-937细胞中的TMUB1,则显著削弱了IGSF9诱导的IL-6分泌和STAT3磷酸化(图 4I-J)。这些结果首次确定TMUB1是巨噬细胞表面介导IGSF9信号传导的功能性受体。
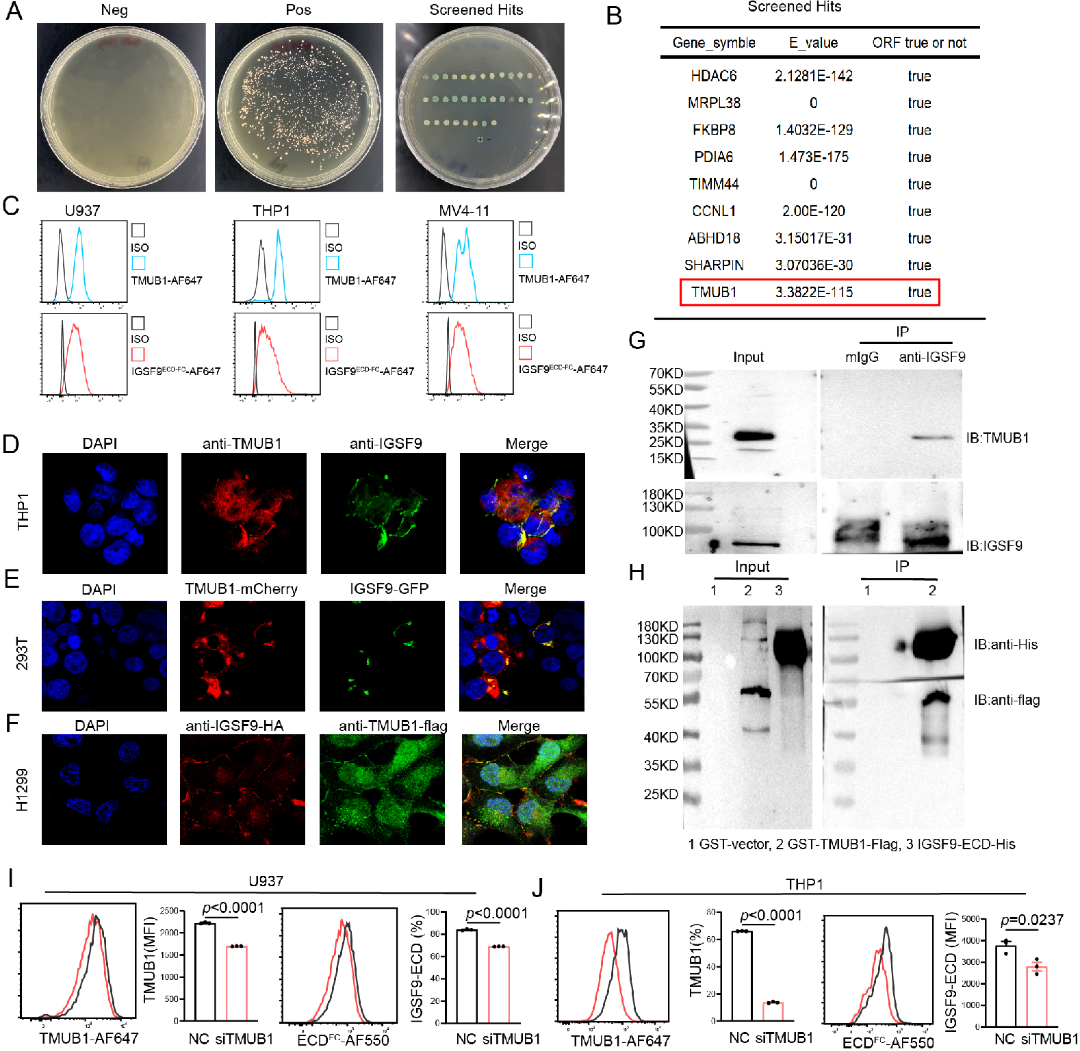
图4.IGSF9与巨噬细胞上的TMUB1互作
5.IGSF9诱导TAMs衰老的促瘤功能验证与靶向治疗潜力
本研究通过一系列体内实验、治疗干预及临床样本分析,系统验证了IGSF9-TAMs衰老轴的促瘤功能及其转化价值。首先,在多种小鼠模型中证实了其体内功能:在免疫健全小鼠中,接种LL/2-Igsf9肿瘤细胞后,肿瘤生长更快,肿瘤微环境(TME)内F4/80⁺ TAMs比例增加;在缺乏T细胞的NSG小鼠中,此效应依然存在,说明该效应不依赖于适应性免疫,且清除巨噬细胞可逆转促瘤效应,这直接证明TAMs为IGSF9促瘤作用的关键执行者。
治疗干预表明,抗IGSF9抗体能逆转TAMs的衰老与抑制状态,重塑TME免疫组成(增加CD8⁺ T细胞、减少Treg),从而抑制肿瘤生长。最后,临床样本分析证实,在非小细胞肺癌(NSCLC)患者中,IGSF9的表达与TAMs内衰老标志物P21和IL-6的水平呈显著正相关,为该轴的临床相关性提供了直接证据。
研究结论
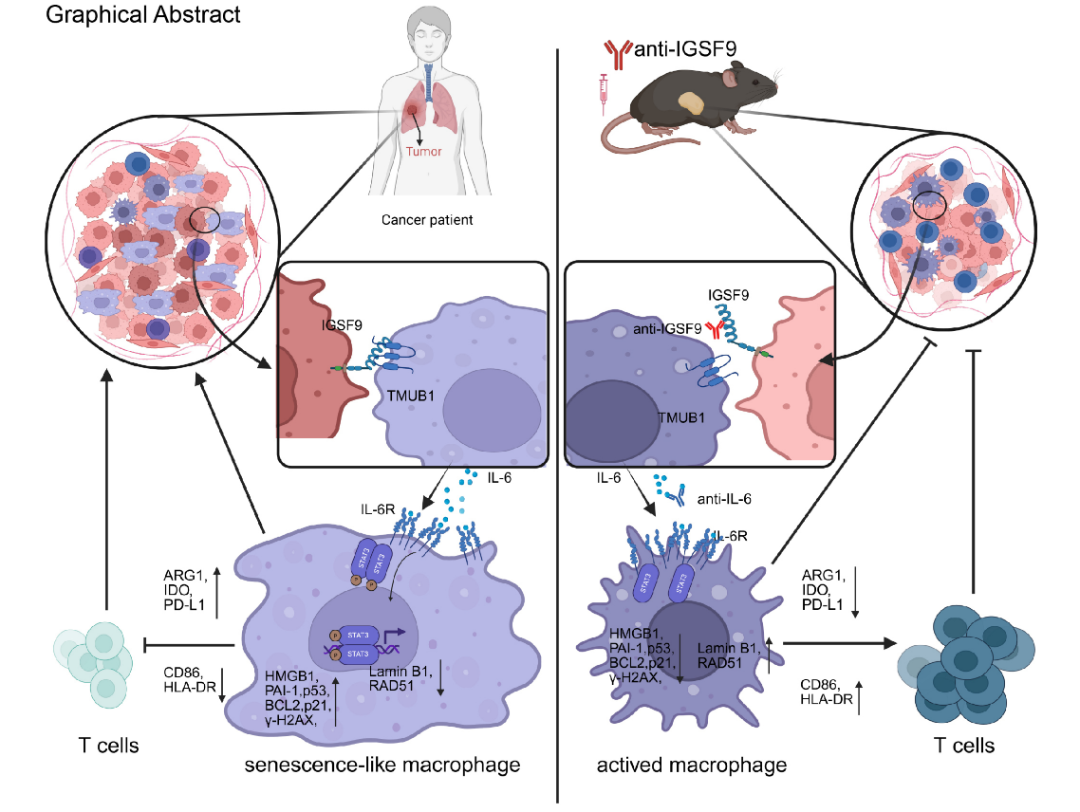
本研究通过对临床肺癌单细胞及空间转录组数据分析发现IGSF9与肿瘤相关巨噬细胞(TAMs)衰老相关。通过膜体系酵母双杂交筛选人PBMC文库,鉴定出TMUB1为IGSF9在TAMs上的结合蛋白,并证实该结合激活IL-6/STAT3信号通路,诱导肿瘤相关巨噬细胞(TAMs)衰老,并表达免疫抑制表型,从而促进肿瘤免疫逃逸。动物模型中抗IGSF9抗体可逆转TAMs衰老、恢复T细胞功能并抑制肿瘤生长。临床样本证实IGSF9与TAMs衰老正相关。该发现为靶向IGSF9/TMUB1轴的肿瘤免疫治疗提供了新策略。
原文链接:https://doi.org/10.1136/jitc-2025-012889
滨州医学院张加深博士和孟宪会博士为论文共同第一作者,李尊岭教授为论文通讯作者。研究工作得到了国家自然科学基金、山东省自然科学基金等项目的资助。






