前言
2026年1月10日,中国科学技术大学生命科学与医学部杨振业团队在期刊Molecular Cancer上发表研究论文。阐明了肿瘤相关巨噬细胞(TAMs)通过激活NOTCH2-JAG1邻分泌信号,促进肿瘤细胞在紫杉醇等抗有丝分裂药物诱导的分裂阻滞期后存活,从而介导化疗耐药的作用机制。研究通过分裂阻滞期肿瘤细胞的翻译组测序,筛选到在该阶段发生翻译上调的关键靶点NOTCH2,并进一步结合活细胞成像、单细胞转录组测序、基因敲降/敲除及肿瘤–巨噬细胞共培养等方法,系统解析了TAMs–肿瘤细胞通过 NOTCH2–JAG1轴介导耐药的分子机制。上述发现已在多种卵巢癌异种移植、同种移植及患者来源移植(PDX)模型和临床样本中得到验证,为阐明肿瘤微环境介导的紫杉醇耐药机制及优化联合治疗策略提供了重要理论依据和实验支撑。

发表期刊:《Molecular Cancer》
影响因子:33.9
涉及的欧易生物服务产品:单细胞转录组测序
研究背景
抗有丝分裂类化疗药物,尤其是紫杉类药物,仍是一线治疗卵巢癌、乳腺癌和肺癌等多种实体瘤的核心药物,但其疗效常因原发性或继发性耐药而受限,相关分子机制尚未明确。研究表明,紫杉类药物通过破坏纺锤体组装并持续激活纺锤体检查点,诱导肿瘤细胞发生有丝分裂期阻滞,而多数细胞并不在分裂期内死亡,而是通过异常分裂或有丝分裂滑脱(mitotic slippage)存活下来,这是耐药形成的重要基础。然而,分裂阻滞后肿瘤细胞命运选择的关键调控机制仍不清楚。
此外,紫杉醇耐药的形成既涉及肿瘤细胞自身的内在调控,也受到肿瘤微环境(tumor microenvironment,TME)的显著影响。其中,肿瘤相关巨噬细胞(tumor-associated macrophages,TAMs)作为TME中最丰富的免疫细胞,常极化为促肿瘤的M2型,可通过旁分泌或细胞间直接接触等方式调控肿瘤化疗耐药,是介导紫杉醇耐药的重要外在因素,但其通过细胞间直接接触的邻分泌信号发挥作用的具体机制仍不明确。
NOTCH信号通路是进化保守的细胞间通讯通路,其异常激活与肿瘤多药耐药密切相关。JAG1作为NOTCH通路的核心配体、NOTCH2作为重要受体,二者介导的邻分泌信号在TAMs-肿瘤细胞相互作用中的功能及其在紫杉醇耐药中的调控机制尚未深入解析,且现有针对TAMs或NOTCH通路的干预策略仍存在特异性不足、临床转化效果有限等问题。基于此,深入探究TAMs是否及如何通过激活NOTCH2–JAG1邻分泌信号调控紫杉醇耐药,对于阐明TME介导化疗耐药的新机制并优化紫杉醇联合治疗策略具有重要意义。
技术路线
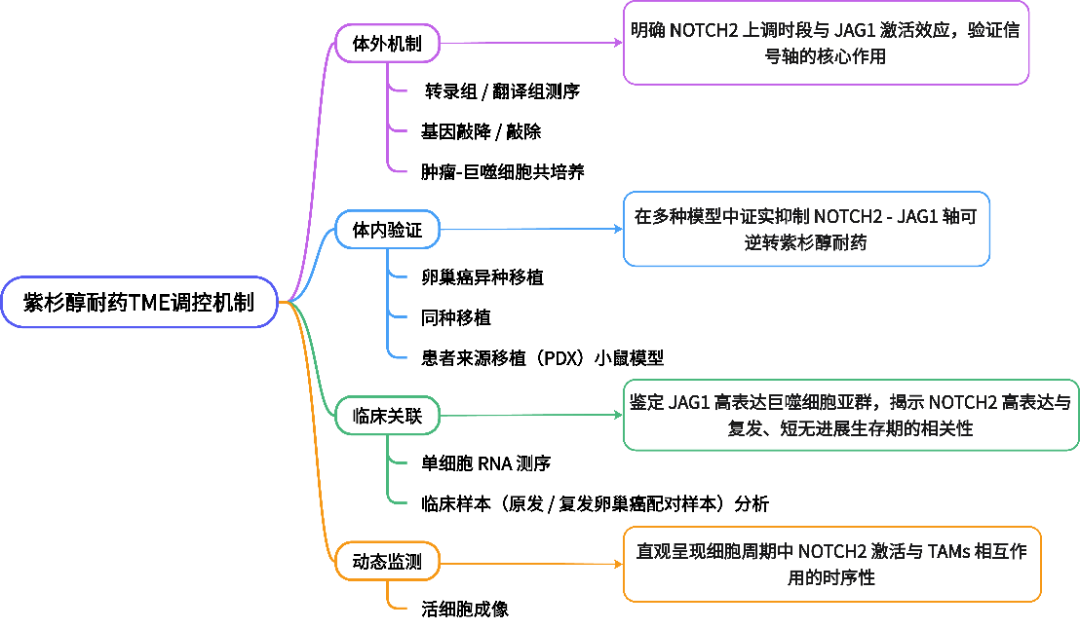
研究内容
本研究围绕肿瘤相关巨噬细胞(TAMs)调控肿瘤对紫杉醇耐药的分子机制展开系统探索,通过体外细胞共培养模型、体内荷瘤小鼠模型及临床肿瘤样本分析,证实TAMs与肿瘤细胞的直接接触可激活NOTCH2-JAG1邻分泌信号通路,具体表现为TAMs在紫杉醇刺激下高表达NOTCH 配体JAG1,其与肿瘤细胞表面的NOTCH2受体结合后,触发受体切割释放胞内域(NICD2),进而入核调控下游耐药相关基因(如BCL-2、ABCB1等)的转录,增强肿瘤细胞的抗凋亡能力和药物外排功能,最终导致紫杉醇化疗敏感性降低;进一步研究发现,该信号轴可通过正反馈循环(激活的NOTCH2信号反过来促进肿瘤细胞分泌趋化因子招募更多TAMs浸润,并诱导其M2型极化及JAG1持续表达)放大耐药效应,而特异性敲低TAMs中的JAG1、肿瘤细胞中的 NOTCH2,或使用NOTCH通路抑制剂(如DAPT)均可有效阻断该信号传导,逆转肿瘤对紫杉醇的耐药性,同时临床样本验证显示,高TAMs浸润、JAG1高表达及NOTCH2激活的肿瘤患者,紫杉醇化疗疗效更差、预后不良,上述研究明确了TAMs介导紫杉醇耐药的新机制,为临床开发靶向NOTCH2-JAG1邻分泌信号的联合治疗策略提供了实验依据和理论支撑。
研究结论
一、紫杉醇诱导NOTCH2翻译上调,且与卵巢癌患者耐药相关
1. 紫杉醇处理后,肿瘤细胞在有丝分裂停滞期(pM) 通过细胞质多聚腺苷酸化选择性上调 NOTCH2 蛋白(而非mRNA),且该上调在细胞退出有丝分裂进入G1期后仍持续存在。
2. 临床样本显示:卵巢癌患者化疗后复发肿瘤中NOTCH2表达显著高于初治肿瘤;NOTCH2高表达患者的无进展生存期(PFS)显著缩短,提示NOTCH2可作为紫杉醇耐药的预后标志物。
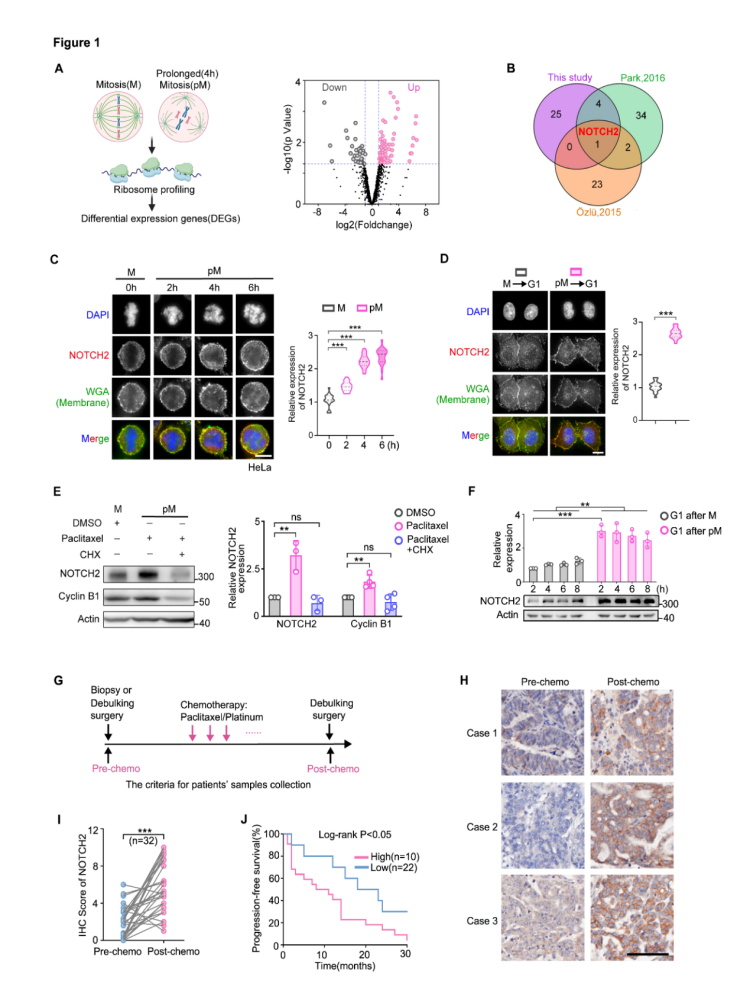
图1 紫杉醇诱导 NOTCH2 翻译上调且与卵巢癌患者耐药及不良预后相关
二、NOTCH2通过多聚腺苷酸化翻译上调,且JAG1激活其信号促进肿瘤细胞存活
1. NOTCH2 mRNA的3'UTR含8个细胞质多聚腺苷酸化元件(CPE)和5个多聚腺苷酸化六核苷酸(PH),可结合CPEB蛋白并在有丝分裂期发生多聚腺苷酸化,从而增强翻译(类似已知的有丝分裂翻译调控基因 CCNB1)。
2. 巨噬细胞高表达的NOTCH配体JAG1可激活肿瘤细胞的NOTCH2信号(促进NOTCH2核转位),显著降低紫杉醇诱导的G1期肿瘤细胞死亡;敲除NOTCH2可完全阻断该保护作用。
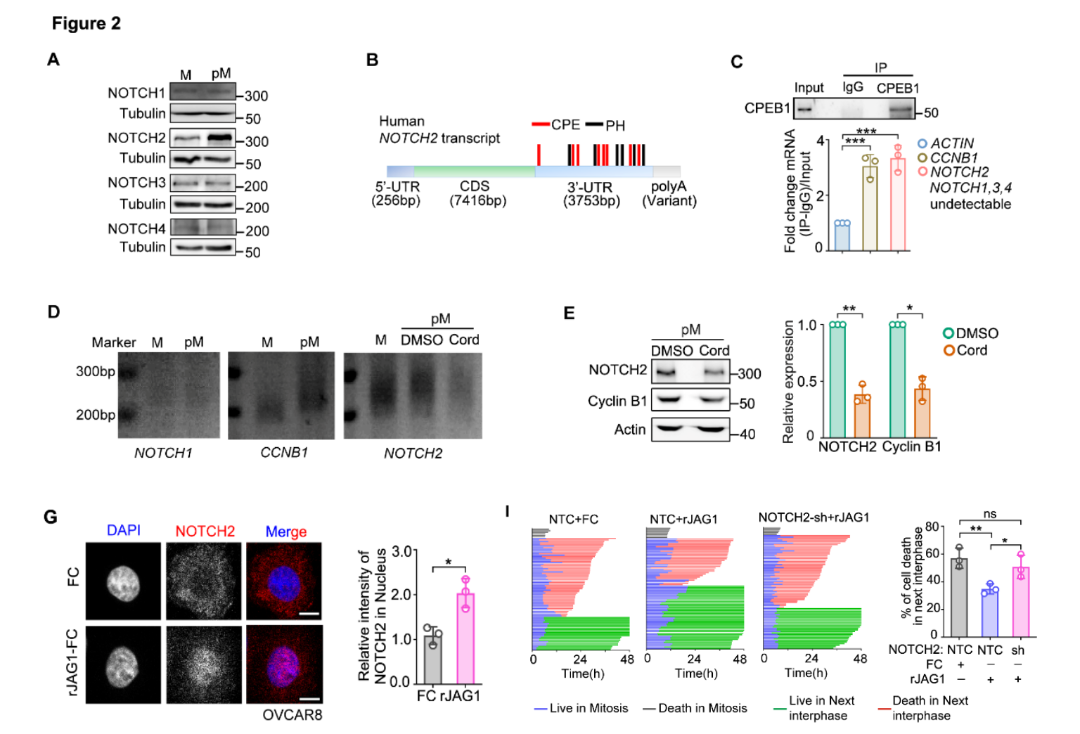
图2 多聚腺苷酸化增强 NOTCH2 翻译,JAG1 激活其信号减少紫杉醇诱导的肿瘤细胞死亡
三、巨噬细胞JAG1是NOTCH2的主要激活者,且形成正反馈loop增强耐药
1. 临床卵巢癌腹水样本中,CD68⁺巨噬细胞的JAG1表达显著高于肿瘤细胞(流式分析显示93.59% JAG1⁺细胞为巨噬细胞)。
2. 体外共培养实验:M2型巨噬细胞(TAMs主要亚型)通过JAG1激活肿瘤细胞NOTCH2,降低紫杉醇诱导的肿瘤细胞凋亡;敲除巨噬细胞JAG1或肿瘤细胞NOTCH2可逆转该效应。
3. 体内巨噬细胞耗竭实验:在ID8卵巢癌小鼠模型中,用氯膦酸脂质体耗竭巨噬细胞后,紫杉醇对肿瘤的抑制作用显著增强,且NOTCH2敲除不再进一步提升敏感性,证明巨噬细胞是NOTCH2-JAG1信号的核心上游激活者。
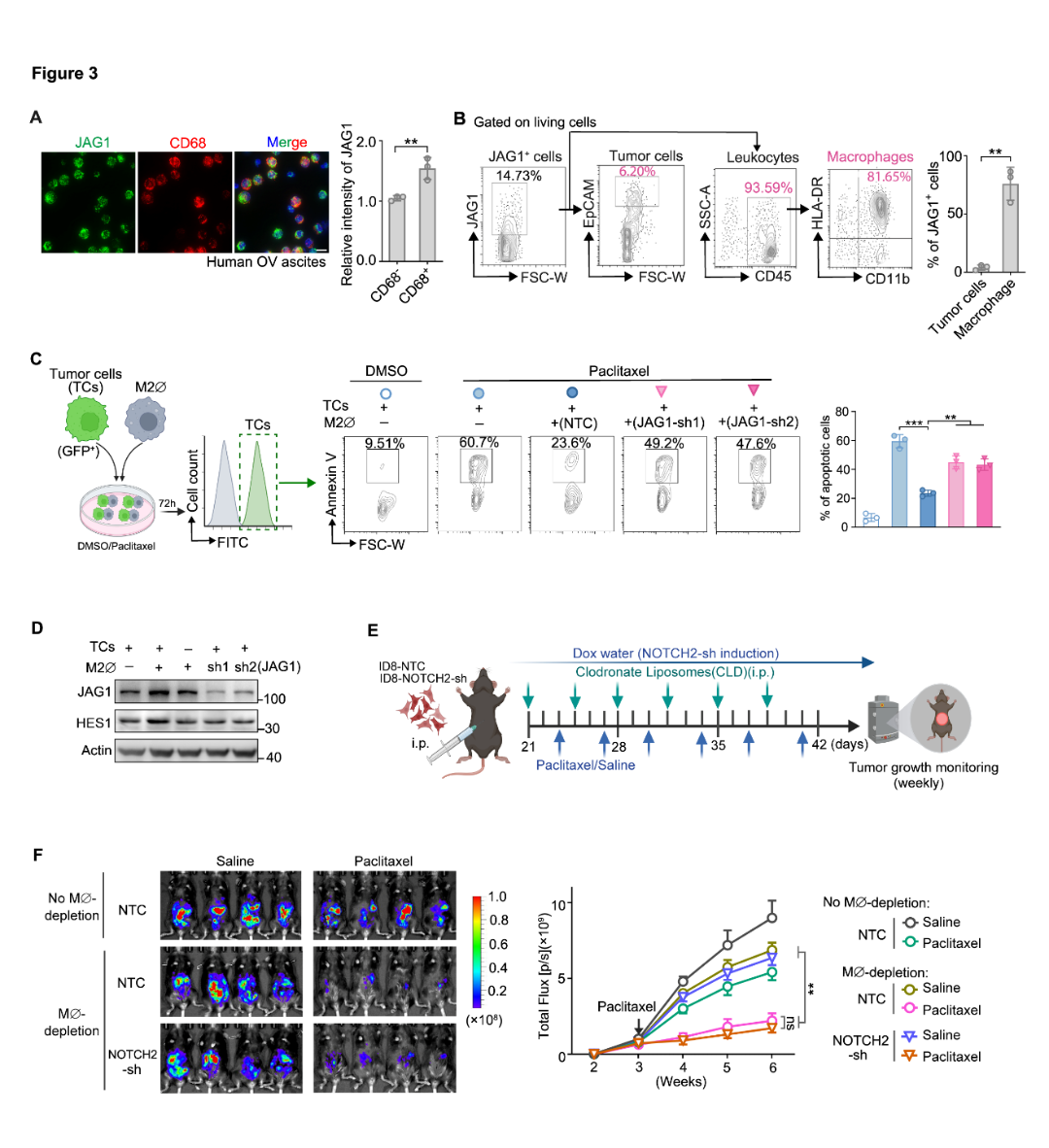
图3 巨噬细胞JAG1激活 NOTCH2,是体内紫杉醇耐药的关键因素
四、NOTCH2激活下游促生存通路并招募巨噬细胞,形成正反馈loop
1. NOTCH2激活后,通过转录调控上调CSF1和IL-1β(两种巨噬细胞趋化因子),促进M2型巨噬细胞向肿瘤微环境招募。
2. 转录组分析显示:NOTCH2敲除后,肿瘤细胞的PI3K-AKT、MAPK等促生存通路显著下调,同时细胞因子-受体相互作用通路富集降低,证明NOTCH2兼具“增强肿瘤细胞自身存活”和“重塑微环境招募巨噬细胞”的双重作用,形成“NOTCH2激活→CSF1/IL-1β释放→巨噬细胞招募→JAG1进一步激活 NOTCH2”的正反馈 loop。
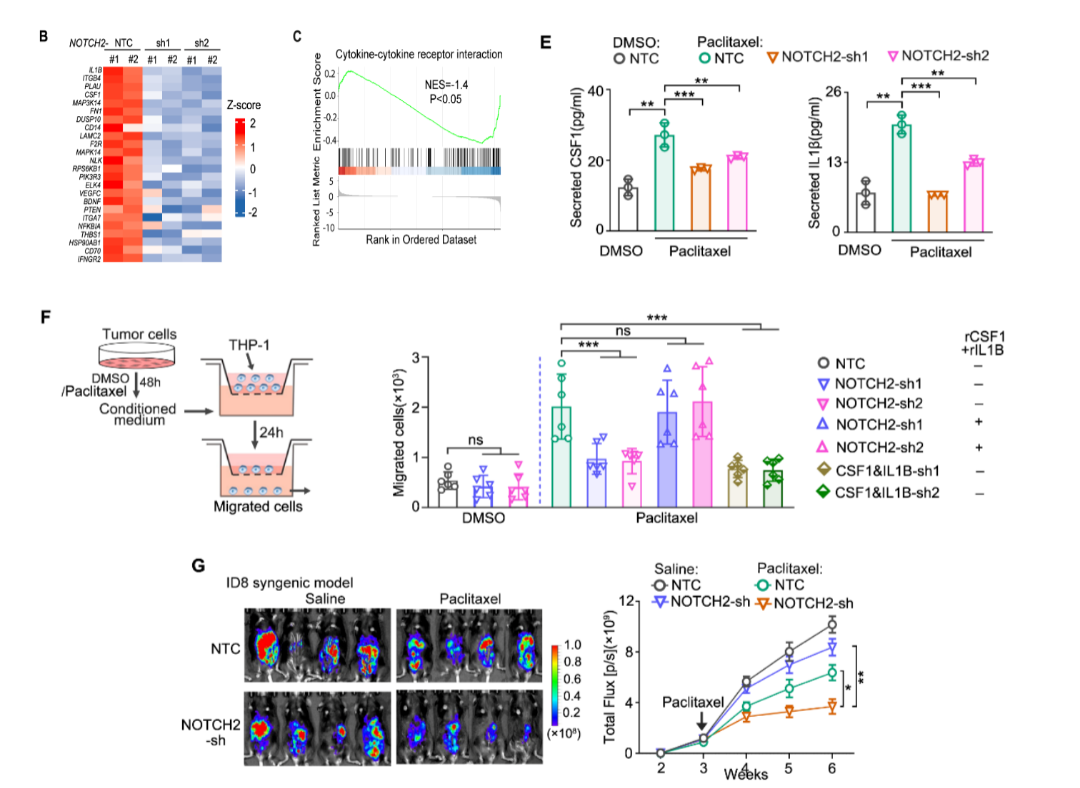
图4 NOTCH2 通过促生存通路及 CSF1/IL-1β 招募巨噬细胞增强耐药
五、NOTCH抑制剂(GSI)联合紫杉醇可逆转耐药,且在PDX模型中验证
1. 采用泛NOTCH抑制剂RO4929097(γ-分泌酶抑制剂,GSI) 阻断NOTCH2激活:在OVCAR8异种移植、ID8同系移植(包括p53敲除模型)中,GSI+紫杉醇联合治疗显著抑制肿瘤生长,且效果优于单药;同时减少肿瘤微环境中JAG1高表达的巨噬细胞亚型。
2. 患者来源异种移植(PDX)模型:取自紫杉醇耐药患者的肿瘤组织构建PDX模型,GSI+紫杉醇联合治疗显著抑制肿瘤生长,证明该策略的临床转化潜力。
3. 单细胞RNA测序(scRNA-seq):ID8-p53⁻/⁻模型腹水细胞测序显示,紫杉醇处理富集“JAG1 高表达巨噬细胞亚型(C1)”,该亚型高表达促肿瘤基因(如Hmox1、Fabp5);而GSI+紫杉醇联合治疗可显著减少该亚型,证明NOTCH抑制可靶向清除促耐药巨噬细胞。
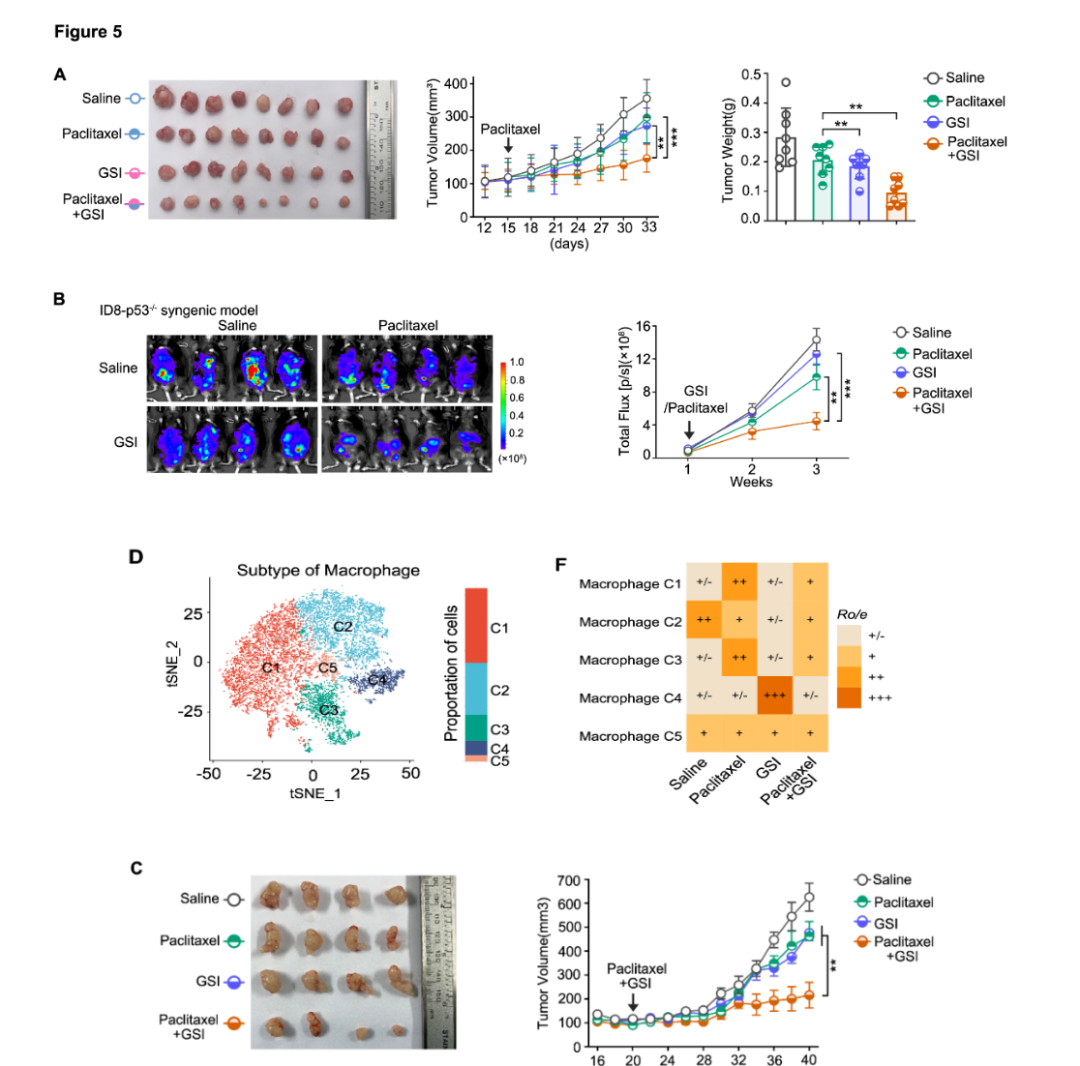
图5 NOTCH抑制剂联合紫杉醇在多种小鼠模型中逆转耐药并靶向JAG1⁺巨噬细胞
研究结论
1. 核心结论
1)全新耐药机制:首次发现紫杉醇通过“细胞质多聚腺苷酸化”上调NOTCH2翻译,且肿瘤细胞与巨噬细胞通过NOTCH2-JAG1邻分泌信号形成正反馈loop,是紫杉醇耐药的关键机制。
2)生物标志物价值:NOTCH2高表达可作为卵巢癌患者紫杉醇耐药的预后标志物,指导临床用药选择。
3)治疗策略:NOTCH 抑制剂(如 GSI)联合紫杉醇可特异性阻断肿瘤-巨噬细胞相互作用,逆转耐药,尤其在NOTCH2阳性肿瘤中潜力显著。
2. 临床意义
1)解决临床痛点:针对卵巢癌紫杉醇耐药的“无药可用”困境,提供了“靶向NOTCH2-JAG1信号轴” 的全新方向,且PDX模型验证了临床转化可行性。
2)精准治疗优势:相比“广谱巨噬细胞耗竭”(可能影响正常免疫功能),靶向NOTCH2-JAG1信号可特异性清除促耐药巨噬细胞,降低治疗毒性。
3)药物研发启示:目前尚无NOTCH2特异性抑制剂,本研究为开发NOTCH2单抗或小分子抑制剂提供了明确的靶点验证,且提示“JAG1中和抗体”也可能成为联合治疗选项。
参考文献:
Jones LO, Willms RJ, Xu X, Graham RDV, Eklund M, Shin M, Foley E. Single-cell resolution of the adult zebrafish intestine under conventional conditions and in response to an acute Vibrio cholerae infection. Cell Rep. 2023 Nov 28;42(11):113407.
doi: 10.1016/j.celrep.2023.113407. Epub 2023 Nov 9. PMID: 37948182.






