前言
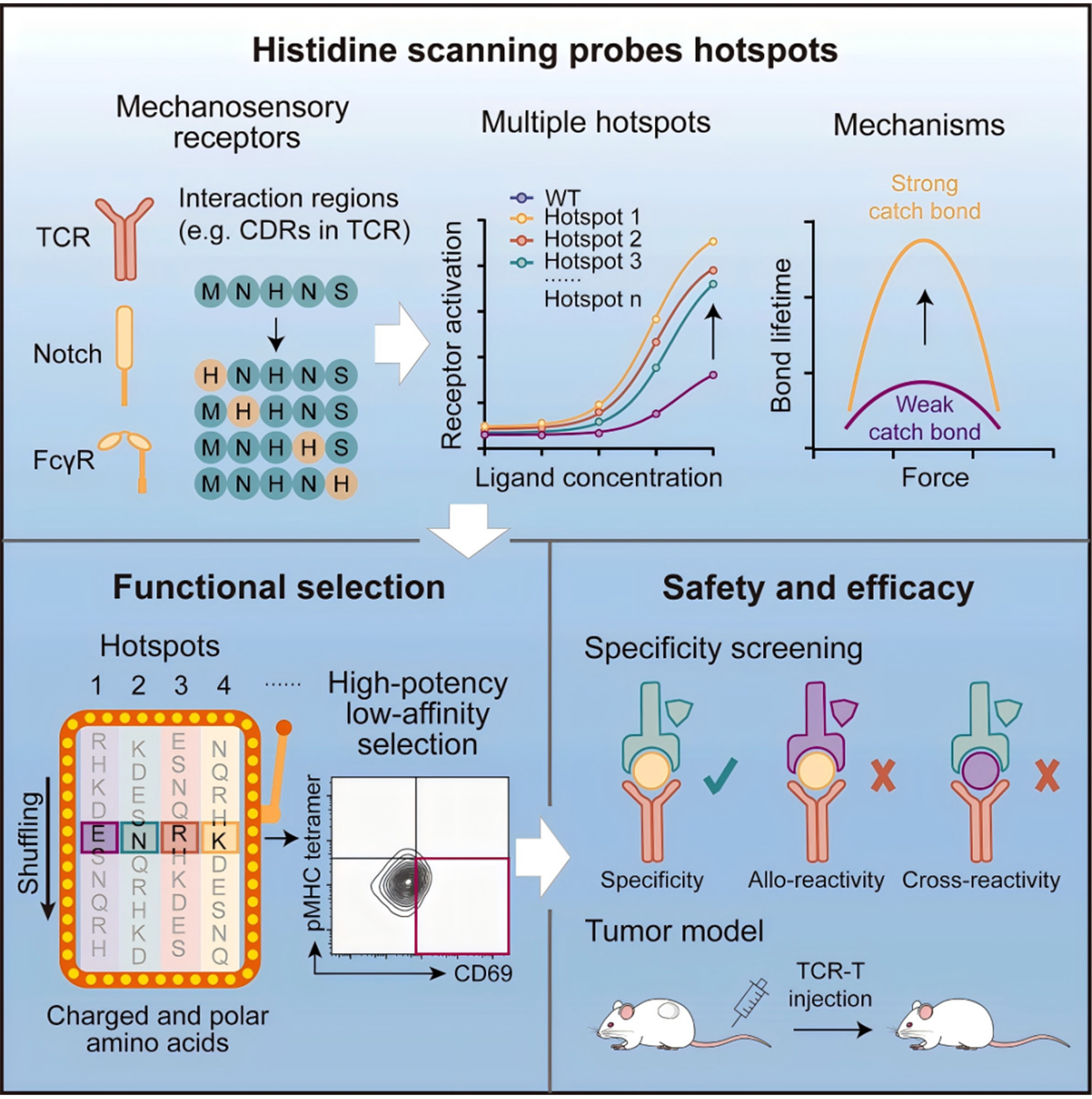
2026年2月19日,中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)赵祥研究员团队联合多家单位在《Cell》上发表题为“Tuning the sensitivity of mechanosensory receptors through histidine scanning”的文章,该研究提出组氨酸扫描(histidine scanning)技术,通过单组氨酸突变筛选T细胞受体(TCR)互补决定区(CDR区)热点,增强其与pMHC的逆锁键(catch bond)形成,提升信号强度且不引发脱靶毒性。该改造技术无需借助TCR-pMHC的三维结构即可设计低亲和力高活性TCR库,显著改善TCR-T治疗的安全性与疗效,还可推广至DLL4-Notch、Fc-FcR等其他机械敏感受体,为免疫治疗提供通用新策略。欧易生物提供了单细胞转录组测序(scRNA-seq)的服务。

发表期刊:Cell
影响因子:42.5
涉及欧易生物的服务产品:单细胞转录组测序(scRNA-seq)
研究背景
T细胞受体(TCR)-T细胞疗法对实体瘤具有疗效,但鉴定针对肿瘤抗原的高效、特异性TCR仍面临挑战。传统的亲和力成熟方法虽能增强TCR与pMHC的结合强度,却可能引发致命的脱靶毒性。近年研究发现,TCR作为一种机械感受受体,其与pMHC在受力下形成的“逆锁键”对信号传导和抗原辨别至关重要,且逆锁键的强度与TCR信号效能密切相关,而非单纯取决于三维结合亲和力。然而,逆锁键的具体形成机制及其在解决TCR-T疗法安全性问题上的潜力尚不明确。此外,现有的逆锁键改造工程方法依赖于已知的TCR-pMHC复合物晶体结构来设计突变文库,限制了其广泛应用。因此,迫切需要一种不依赖结构信息的通用策略,以安全地增强TCR的敏感性。
研究内容
本研究首先运用组氨酸扫描技术,对TCR的互补决定区进行系统性单点突变,成功识别出多个能显著增强TCR激活信号的热点,并验证了该方法在TCR55、MAGE-A3特异性TCR等多种TCR中的广泛适用性。机制研究表明,组氨酸通过促进氢键和盐桥的形成来增强逆锁键,从而强化TCR信号传导。基于识别的热点构建随机化TCR文库并进行功能筛选,获得了信号强度与逆锁键水平均优于野生型的TCR变体。安全性评估显示,这些变体保持了精细特异性,未引入新的脱靶毒性。在体内肿瘤模型中,工程化后的TCR-T细胞展现出更优的治疗效果,且未引起脱靶或靶上脱瘤毒性。最后,研究将组氨酸扫描成功应用于DLL4-Notch和Fc-FcR等其他机械感受受体系统,证明了其作为通用工程化平台的潜力。
技术路线
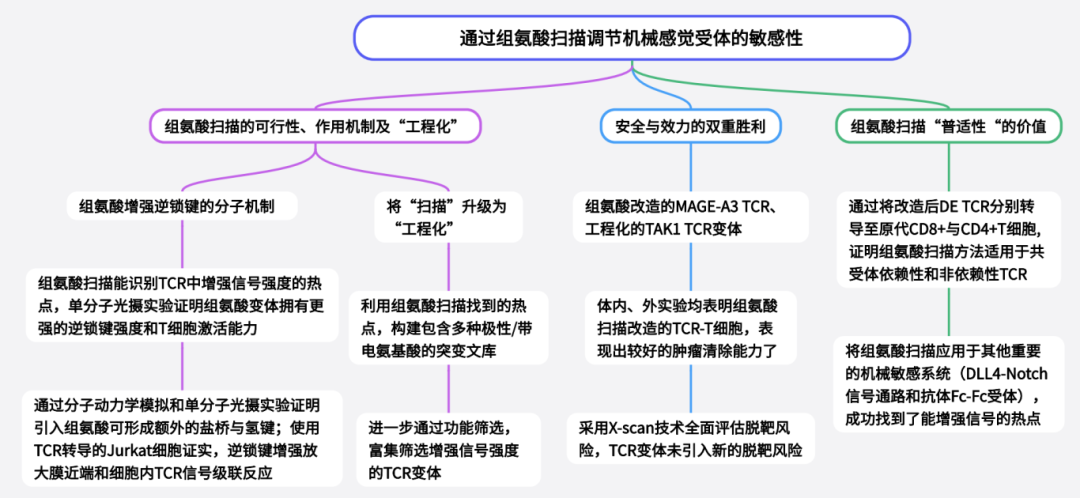
研究结果
Result 1 组氨酸扫描识别用于调节TCR敏感性的热点
基于晶体结构的文库设计方法曾被用于构建特异性TCR的逆锁键,从而生成多种TCR变体,与其他带电或极性氨基酸相比,组氨酸突变是最常引入的(图1A)。本研究中作者提出了一种组氨酸扫描方法,即通过单个组氨酸突变,扫描TCR的α链和β链的互补决定区(CDR),以识别形成逆锁键的热点(图1B)。作者首先对HLA-B35-HIVpol特异性TCR55的CDR进行了组氨酸扫描,识别出九个热点,单个组氨酸修饰即可显著增强TCR激活(图1C, 1D)。随后,在肿瘤抗原特异性MAGE WT TCR(其亲和力极低且临床高亲和力变体存在交叉反应毒性)中识别出十个能显著增强TCR激活的热点,且所有单点突变体均未引发对HLA-A1-肌联蛋白的交叉反应(图1E, 1F)。证明了组氨酸扫描技术在微调TCR敏感性方面的普适性与安全性。
为定量表征这些热点的功能,作者开发了基于光镊的逆锁键检测方法。功能性验证表明,在TCR55中,α-E55H变体比先前已知的α-A98H变体具有更强的T细胞激活能力(图1G)及更高的逆锁键强度(图1H)。在MAGE TCR中,双突变体α-D28H & β-F51H则表,现出与已知的高功能变体94a-14 TCR相当的激活水平(图1I)和逆锁键水平(图1J)。此外,作者还将分析扩展至另外五个缺乏TCR-pMHC复合物的结构数据的TCR(小鼠OT-I、Pmel、TRP2 TCR,HLA-A*02:01-MAGEA4 TCR,HLA-A*11:01-EBV -LMP2A TCR),均成功识别约10个增强信号强度的热点。这些结果证实了组氨酸扫描及时在设计功能性TCR变体中的有效性与普适性。
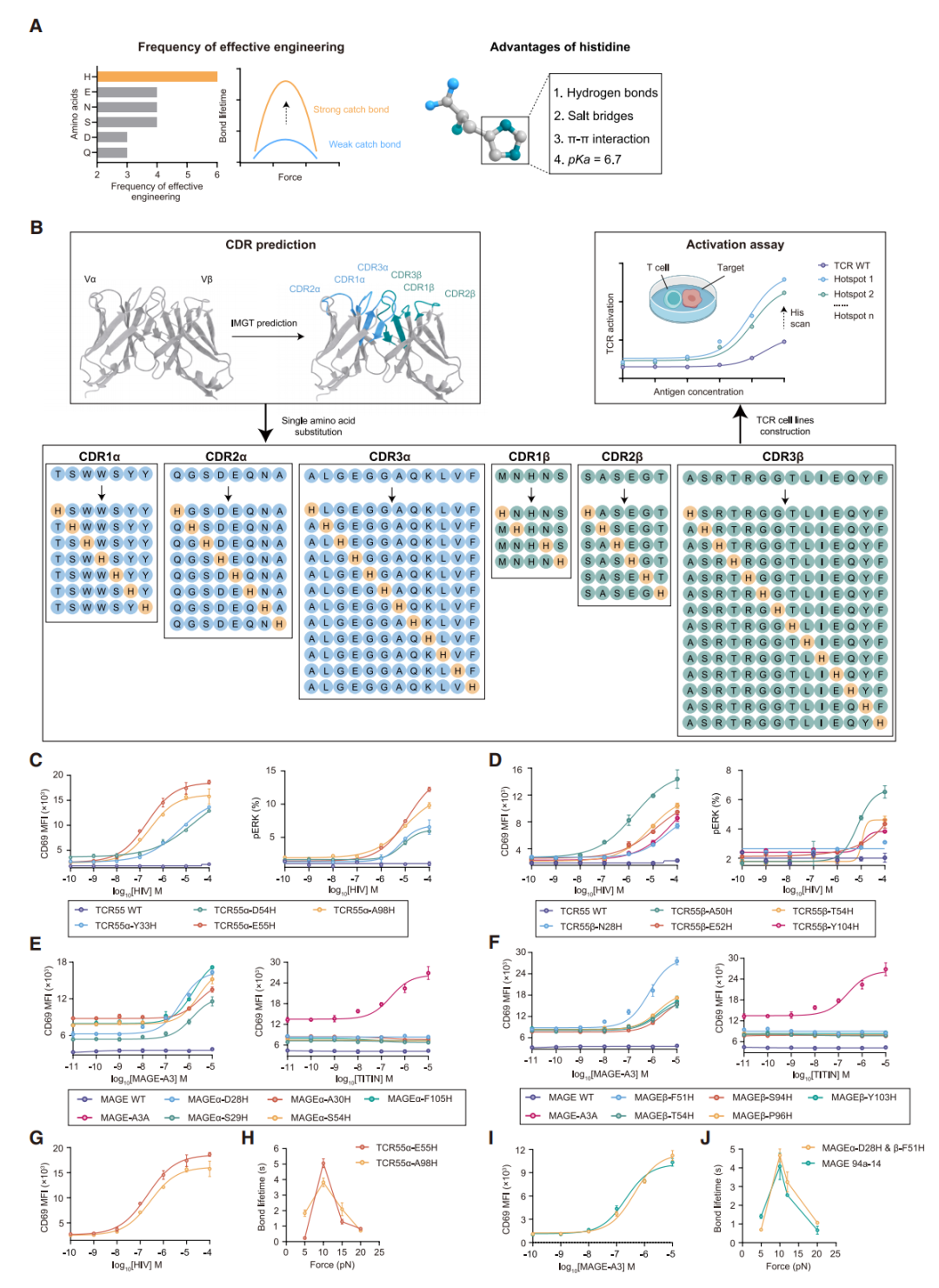
图1 组氨酸扫描示意图及TCR55或MAGE-A3特异性TCR的组氨酸扫描
Result 2 组氨酸通过细胞外、膜近端和细胞内机制调节TCR敏感性
作者进一步探究了组氨酸增强逆锁键的分子机制(图2A)。以TCR55-HLA-B35-HIVpol复合物为模型,通过分子动力学模拟分析了TCR从pMHC解离过程中相互作用的动态变化。结果显示,在±x和±y方向的剪切力下,组氨酸突变体TCR55α-E55H和TCR55α-A98H比野生型(WT)形成了更多瞬时的氢键与盐桥相互作用(图2B)。重点分析相互作用形成最多的+x方向发现,WT TCR在解离时原有相互作用会逐渐被取代(图2C);而引入组氨酸突变后,突变残基在剪切早期即积极参与初始相互作用形成,进而促进更多稳定相互作用的产生(图2C),有效补偿了解离过程中的相互作用损失,从而增强了逆锁键强度。
随后通过单分子光镊实验测量组氨酸修饰TCR变体与HLA-A1-MAGE-A3的逆锁键,发现其键寿命随力增加而延长的典型逆锁键特征,峰值键寿命出现在10-12 pN范围内(图2D)。尽管三维亲和力(3D KD)与TCR信号强度无直接关联(图2E),但峰值键寿命与TCR信号强度呈强正相关(图2F),这表明组氨酸扫描可以通过富集逆锁键来促进识别具有增强敏感性的组氨酸修饰TCR变体。
在细胞功能层面,使用TCR转导的Jurkat细胞证实,逆锁键增强导致免疫突触中磷酸化LCK的募集增加(图2G)。此外还放大下游信号级联,包括PLCγ1、ZAP70和ERK的磷酸化水平升高(图2H)。综上所述,在TCR CDR区特定热点引入组氨酸,可利用其侧链特性形成额外的盐桥与氢键,从而放大膜近端和细胞内TCR信号级联反应。
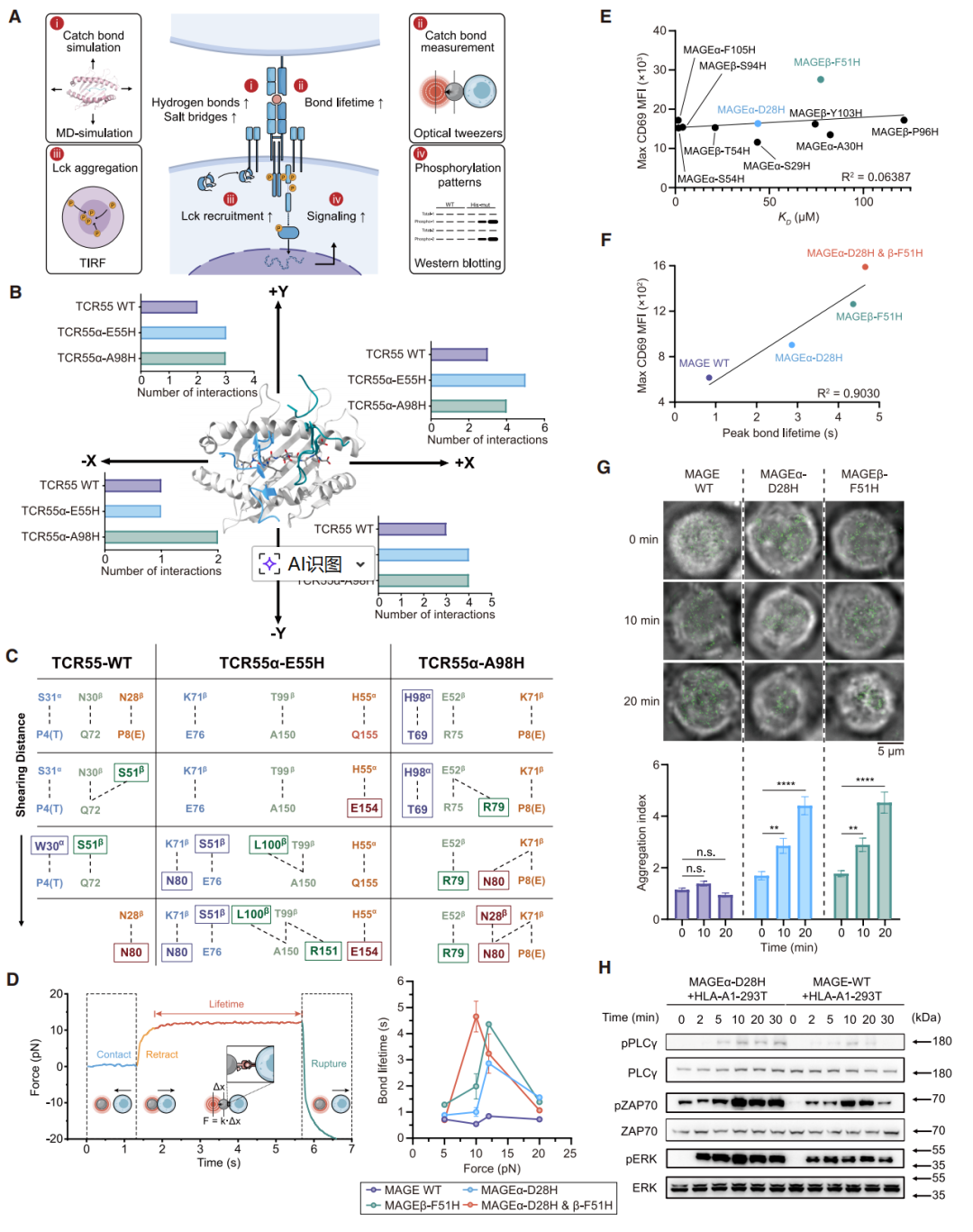
图2 组氨酸逆锁键形成的机理
Result 3 组氨酸扫描指导用于TCR通用工程改造的文库设计
为筛选具有更强逆锁键的TCR变体,作者提出先通过组氨酸扫描鉴定热点,再使用极性与带电氨基酸(包括组氨酸)对这些热点位置进行同时突变,旨在通过形成更多氢键与盐桥来协同增强逆锁键。作者以临床疗效有限的TAK1 TCR(靶向WT-1抗原)为模型,通过组氨酸扫描在其α链与β链上共鉴定出九个功能热点(图3B, 3C)。随后,将α链四个或β链五个热点同时随机化构建T细胞展示文库(图3D)。通过三轮功能选择,富集低四聚体结合(低亲和力)但高CD69表达(高效力)的克隆(图3E, 3G),最终获得了多个信号强度显著优于野生型TAK1 TCR的变体(图3F, 3H)。其中,TAK1-mut 8与TAK1-mut 10的信号强度甚至超过了最强的单点组氨酸突变体TAK1β-R28H(图3I)。尽管这些优选变体的三维亲和力与野生型相当或更低(图3J),且亲和力与信号强度无相关性(图3K),但它们均被改造出更高水平的逆锁键,且逆锁键强度与信号强度呈正相关(图3M)。该结果表明,组氨酸扫描可为TCR文库的设计提供指导,通过逆锁键富集筛选具有增强信号强度的TCR变体。
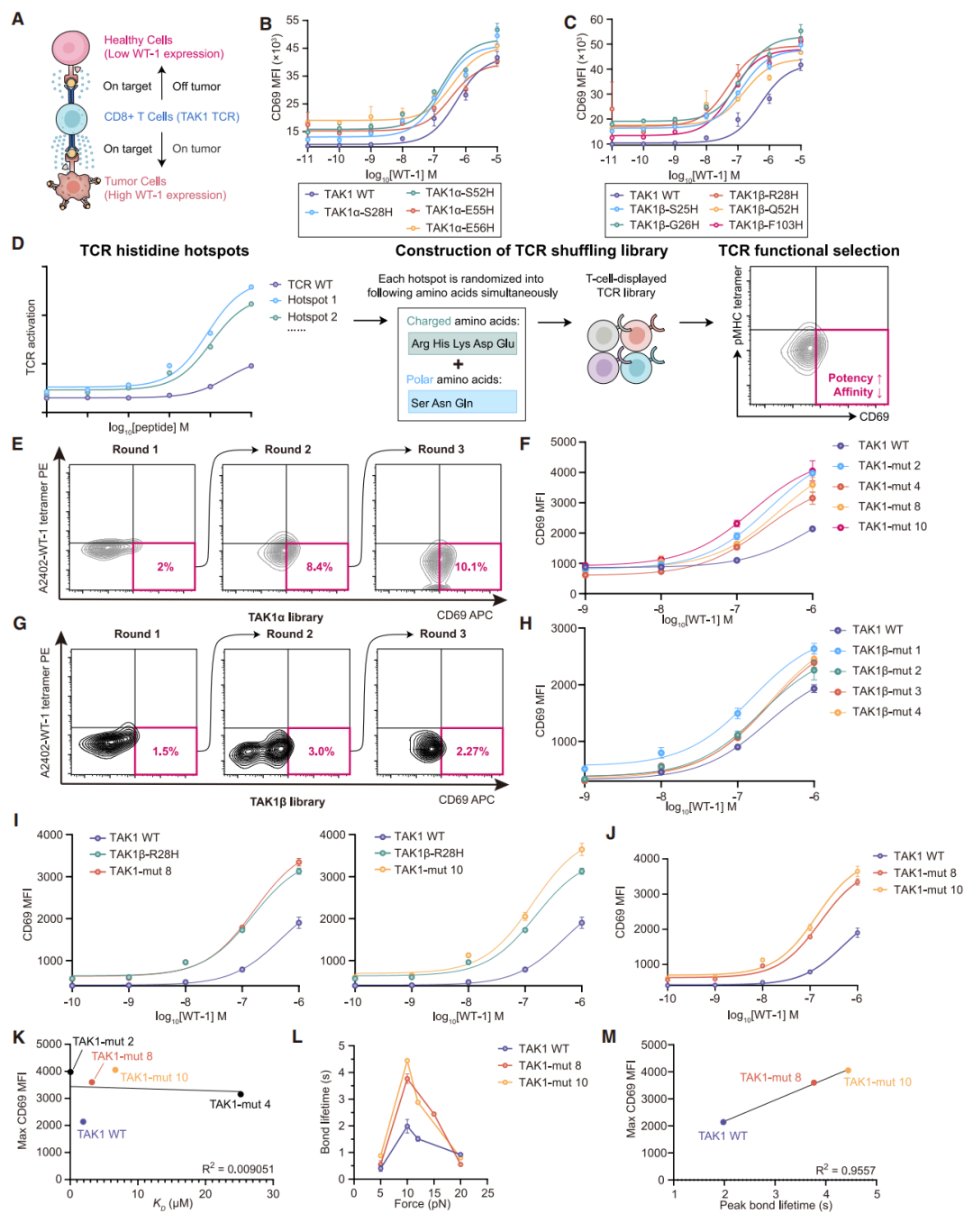
图3基于组氨酸扫描信息的文库功能筛选实现TAK1 TCR的逆锁键工程化
Result 4 组氨酸修饰改善TCR-T细胞疗法且无脱靶毒性
为检验通过组氨酸扫描改造的TCR-T细胞是否能有效清除特定肿瘤细胞,作者选择了信号最强的MAGE-A3特异性变体(MAGEα-D28H、MAGEβ-F51H及双突变体)进行测试。体外与表达内源性靶抗原的HCT116肿瘤细胞共培养时,改造后的TCR-T细胞相较于野生型(WT),其效应功能显著增强,表现为干扰素γ(IFN-γ)、肿瘤坏死因子(TNF)分泌(图4A-4D)、脱颗粒标志CD107a表达(图4E)及细胞毒性(图4F)均显著提升,同时共刺激受体CD137表达更高(图4G),而耗竭标志PD-1/TIM-3表达未进一步增加(图4H, I)。在HCT116荷瘤的免疫缺陷小鼠模型中,输注改造后的TCR-T细胞能有效抑制肿瘤生长、延缓进展并提高生存率(图4J-M),且肿瘤浸润T细胞中耗竭亚群比例与WT组相当(图4N)。表明组氨酸扫描改造的TCR-T细胞在不引起进一步耗竭的情况下,表现出改善的肿瘤清除能力。
为确保安全性,研究采用X-scan技术全面评估脱靶风险。信号热图分析显示,逆锁键改造的MAGEα-D28H & β-F51H TCR的抗原识别谱与WT高度相似,而临床出现毒性的高亲和力A3A TCR则表现出更广泛的氨基酸耐受性(图4O)。综上,研究证实通过组氨酸扫描获得的TCR变体在显著提升抗肿瘤效力的同时,并未引入新的脱靶风险,兼具强效性与安全性。
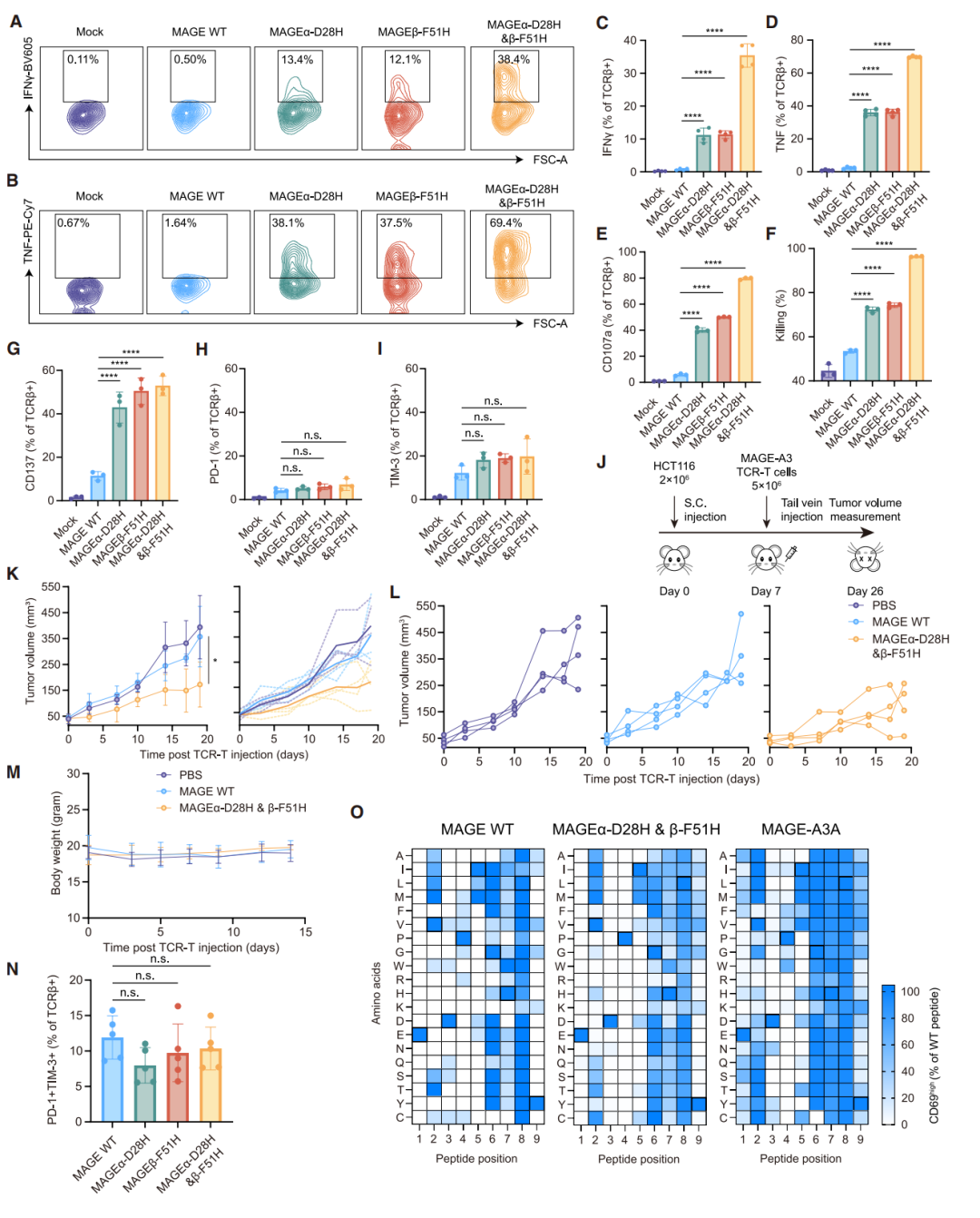
图4 逆锁-结合工程化MAGE-A3特异性TCR在体外和体内的功能与交叉反应性
Result 5 组氨酸扫描指导的文库产生了强效且具有最小靶上毒性的TCR-T细胞
作者进一步评估了基于组氨酸扫描指导的文库筛选出的优选TAK1 TCR变体(TAK1-mut 8与TAK1-mut 10)作为TCR-T疗法的效力与安全性。体外实验表明,相较于野生型(WT),转导TAK1变体的原代T细胞,其效应功能(IFN-γ、TNF、CD107a表达)与细胞毒性显著增强(图5A-D),共刺激标志CD137表达上调(图5E),而耗竭标志PD-1/TIM-3未见显著增加(图5F, G)。在K562荷瘤小鼠模型中,过继转移改造后的TCR-T细胞能有效延缓肿瘤进展并提高生存率(图5H-I )。单细胞RNA测序分析显示,肿瘤浸润的TAK1变体T细胞高表达细胞毒性效应分子(PRF1, GZMB)及趋化因子(CCL3, CCL4),但耗竭相关基因表达也相应升高(图S10A-D)。
随后通过X-scan全面评估脱靶风险,反应热图显示改造TCR的识别谱与WT相似(图5J)。针对过表达抗原可能引起的“靶上、脱肿瘤”毒性,研究建立了模拟健康组织(低抗原)与肿瘤组织(高抗原)的细胞模型(图5K)。结果显示,在高抗原环境下,TAK1变体的信号强度优于临床高亲和力变体T262;而在低抗原环境下,其反应性与WT相当,显著低于T262(图5L, M)。机制上,TAK1变体仅在高抗原刺激时才表现出更强的下游ERK磷酸化(图5N)。因此,在针对过表达抗原改造TCR时,逆锁键工程优于高亲和力成熟,因为它能最大限度地减少靶上、脱肿瘤毒性。
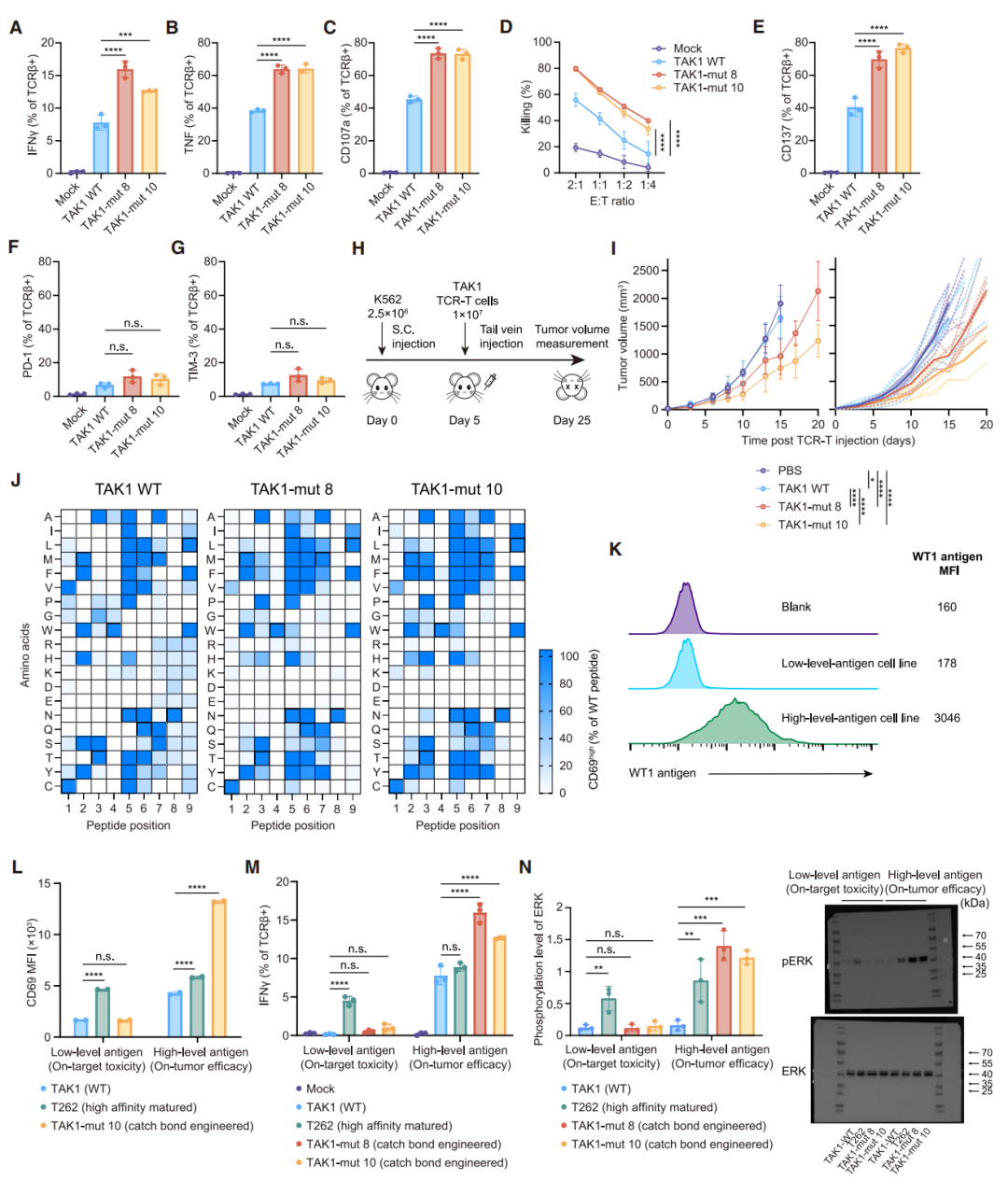
图5 逆锁-结合工程化TAK1变体在体外和体内的功能与交叉反应性
Result 6 组氨酸扫描调节受体依赖性和共受体非依赖性TCR信号的敏感性
为阐明共受体对逆锁键改造TCR功能的影响,本研究将野生型及改造后的TCR分别转导至原代CD8⁺与CD4⁺ T细胞中,并比较其激活水平。结果显示,TCR55α-E55H、MAGE WT TCR及其改造体MAGEα-D28H & β-F51H在CD8⁺ T细胞中的激活显著强于CD4⁺ T细胞,表明其功能发挥依赖于CD8共受体,属于共受体依赖性TCR。与之相反,TAK1 WT TCR及其优选变体TAK1-mut 8与TAK1-mut 10在CD8⁺和CD4⁺ T细胞中均能引发强烈的激活反应,表明其属于共受体非依赖性TCR(图6)。以上结果说明,组氨酸扫描方法适用于共受体依赖性和非依赖性TCR。
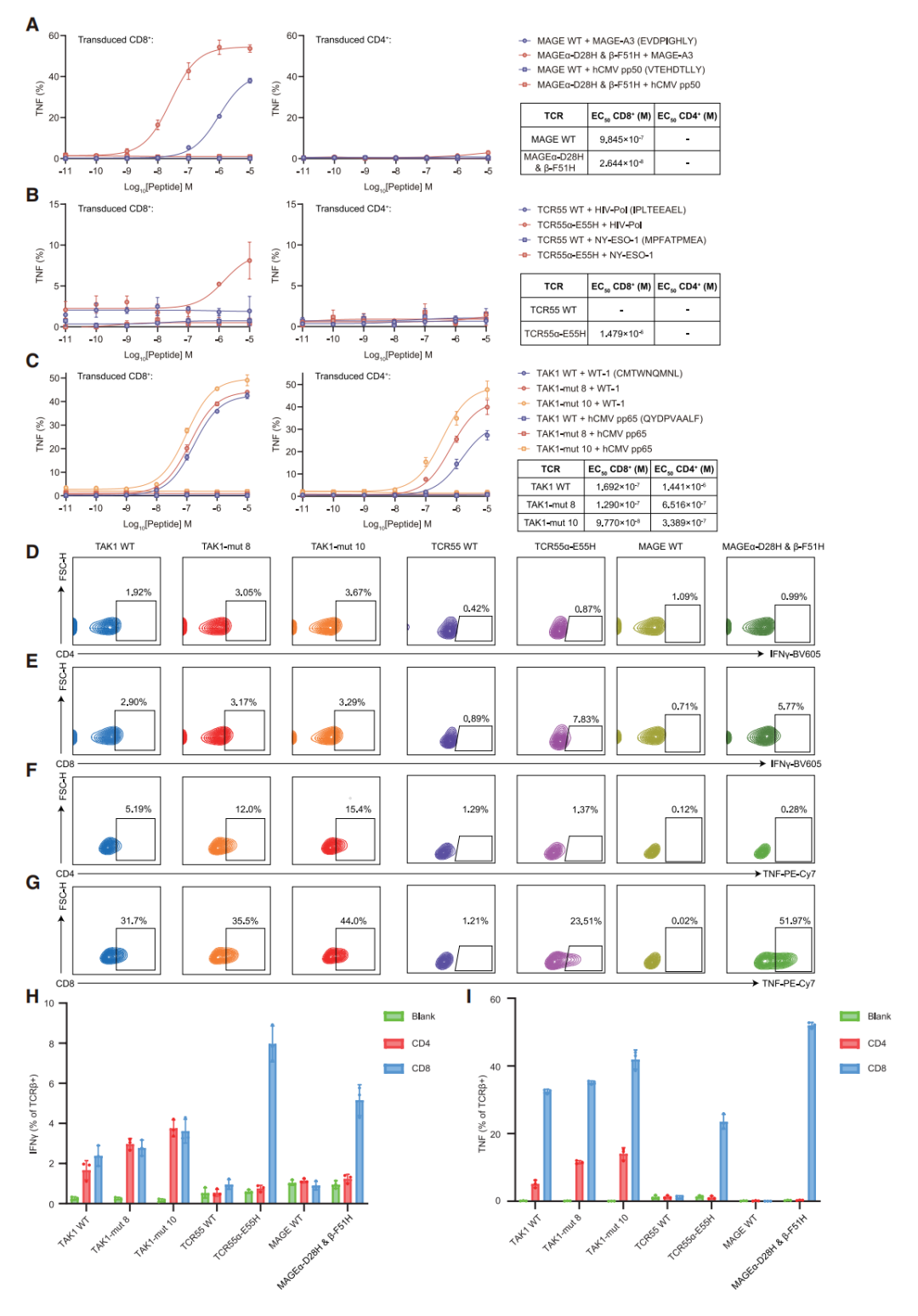
图6 MAGE野生型TCR、TCR55野生型、TAK1野生型TCR及其捕获键工程化变体的共受体依赖性
Result 7 组氨酸广泛调节机械敏感受体的敏感性
作者进一步将组氨酸扫描策略拓展至其他机械敏感受体系统,验证了其通用性。以DLL4-Notch1系统为例,二者已知可通过逆锁键相互作用,作者采用Notch信号报告系统定量评估Notch信号强度(图7A)。通过对DLL4与Notch1相互作用界面的关键残基进行组氨酸扫描,鉴定出多个单点组氨酸突变即可显著增强Notch信号的热点(图7H-7J)。其中,Notch1-Q470H突变体在与DLL4结合时表现出Notch信号的显著提升(图7B),而DLL4-K215H突变体在与Notch1作用时同样诱导Notch信号增强(图7C)。单分子光镊实验进一步证实,这两种突变体均形成比野生型更强的逆锁键(图7D)。
类似地,在Fc-FcγRIA系统中,作者利用Jurkat-NFAT-GFP报告细胞株检测FcR信号强度(图7A)。通过对IgG1-Fc及FcγRIA的相互作用残基进行组氨酸扫描,筛选出多个能显著增强FcR信号的IgG1-Fc及FcγRIA突变体(图7K-7M)。具体而言,FcγRIA-L168H相较于野生型FcγRIA引起更强的下游信号(图7E);IgG1-Fc-L235H也比野生型IgG1-Fc诱导更高的FcγRIA信号活性(图7F)。单分子光镊实验同样显示,这两种突变体与对应配体间的逆锁键强度均高于野生型对照(图7D)。综上,组氨酸扫描方法可成功应用于DLL4-Notch1与Fc-FcγRIA系统,通过增强逆锁键精确调控其信号强度,证明了该策略在蛋白质工程领域的广泛适用潜力。
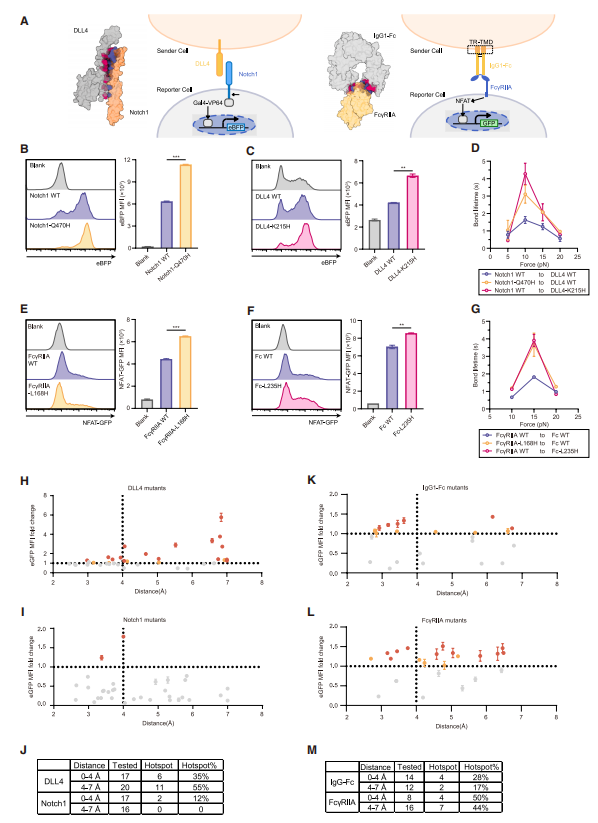
图7 Notch与Fc的组氨酸扫描
研究结论
本研究证明了组氨酸扫描能够识别能够形成额外逆锁键的TCR热点,这些热点可以被随机化以创建用于筛选低亲和力、更高效力变体的TCR文库。从机制上讲,组氨酸促进氢键和盐桥的形成,并加强细胞内信号级联反应。使用这种方法,作者设计了针对不同抗原的多种TCR,没有脱靶毒性或靶上毒性。总的来说,本研究介绍了一种通用的方法来设计低亲和力、高效力的TCR,用于安全的TCR-T细胞疗法,且无需依赖结构来设计TCR文库。此外,该技术还可广泛应用于其他机械感觉配体-受体系统。
参考文献:
Yuanhao Wang et al. , Tuning the sensitivity of mechanosensory receptors through histidine scanning. Cell(2026).https://doi.org/10.1016/j.cell.2025.12.050.






