前言
2026年2月27日,浙江大学医学院第二附属医院肿瘤研究所所长于晓方教授团队,在Science发表了题为STING–NF-κB signaling builds an influenza spillover barrier的文章,该研究系统地揭示了STING–NF-κB信号这条在人体先天免疫系统中起到关键防御作用的这条通路,在限制禽源流感病毒跨物种传播中也发挥了重要作用。这一重要发现不仅深化了对RNA病毒天然免疫识别机制的理解,还推进了病毒跨物种传播方面的研究,对流感疫情预警具有现实意义,更为未来抗流感治疗策略提供了全新靶点和方向。

发表期刊:Science
影响因子:45.8
涉及欧易生物的服务产品:转录组测序
研究背景
禽源甲型流感病毒(Influenza A viruses,IAV)持续对人类公共卫生构成潜在威胁,但由于宿主中存在尚未完全阐明的天然免疫屏障,多数禽源病毒在人类细胞中难以高效复制。既往传统研究主要关注受体结合、病毒聚合酶适配及干扰素(IFN)反应,但这些因素皆无法完全解释跨种传播受限的现象。STING(stimulator of interferon genes)作为DNA感知通路关键接头蛋白,近年来被发现可以在RNA病毒感染中被激活,而其是否参与限制流感病毒跨种传播尚不明确。本研究系统解析了STING介导的抗病毒机制,及其在阻断禽源流感病毒跨物种传播中的作用。
研究内容
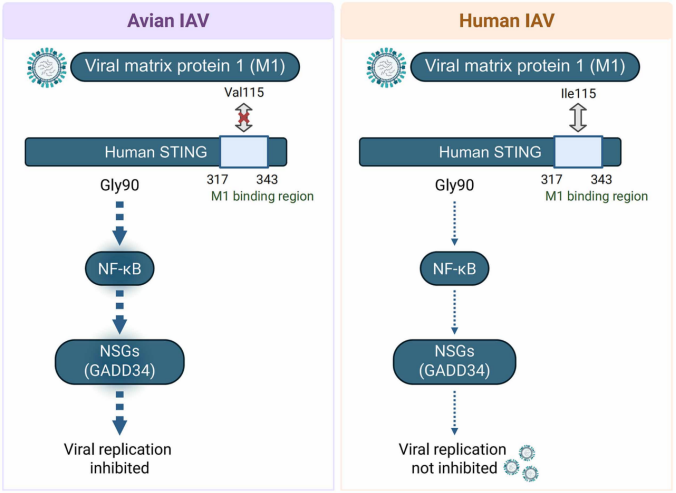
本研究围绕宿主天然免疫是否可以构成流感跨种传播屏障这一核心问题展开,通过构建STING敲除细胞、小鼠模型以及结构功能分离突变体模型,首先发现STING能够显著限制流感病毒复制,且这一作用依赖NF-κB而非经典IRF3–干扰素通路。随后通过系统的STING点突变筛选,鉴定出Gly90为特异性调控NF-κB活化的关键结构位点,并在敲入模型中证实该位点对抗病毒功能至关重要。在机制层面,结合RNA-seq筛选与功能干预实验,研究进一步发现GADD34是STING–NF-κB轴下游的核心抗病毒效应分子,其通过非经典方式直接结合并抑制流感病毒RNA聚合酶活性,从而阻断病毒复制。进一步分析病毒适应机制时发现,人源流感病毒M1蛋白通过第115位氨基酸突变增强对STING信号的拮抗能力,从而突破宿主免疫限制。综合来看,该研究系统揭示了STING–NF-κB–GADD34信号轴构成限制禽源流感向人类传播的分子屏障,并阐明了病毒通过关键结构位点进化实现宿主适应的机制,为流感跨种传播风险评估和干预策略提供了重要理论依据。
技术路线
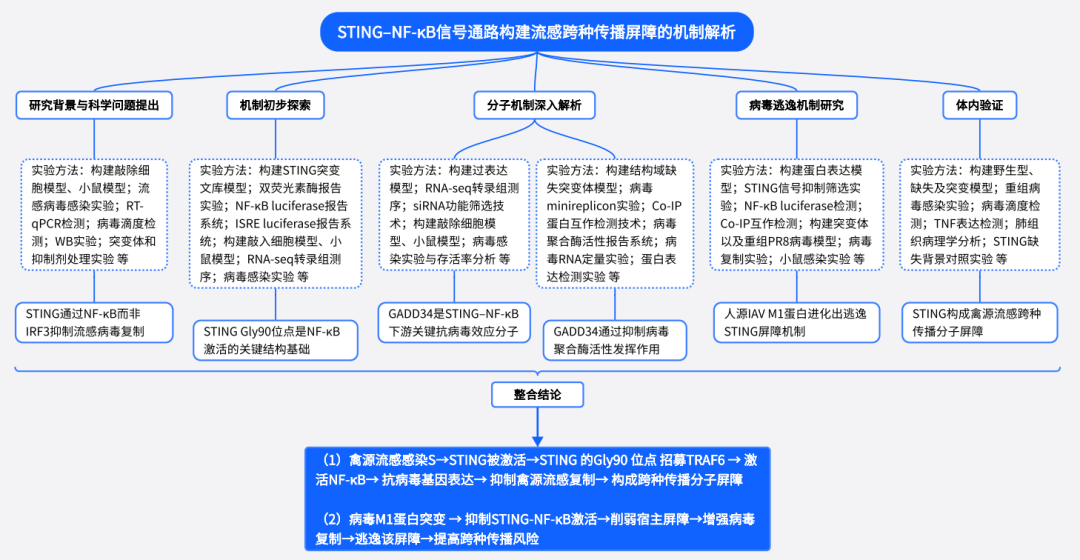
研究结果
Result 1 STING通过NF-κB而非IRF3抑制流感病毒复制
构建STING敲除细胞模型、STING激动剂处理模型以及Sting1−/−小鼠模型,对这些模型分别进行了流感病毒感染实验。利用RT-qPCR检测病毒RNA水平,并通过Plaque assay检测病毒滴度,同时结合WB实验检测信号分子磷酸化水平,发现STING缺失会显著增强病毒复制,而STING激活显著抑制病毒复制。进一步通过IRF3突变体和NF-κB抑制剂ACHP处理实验,证明STING的抗病毒功能依赖NF-κB信号通路而非IRF3-IFN轴。
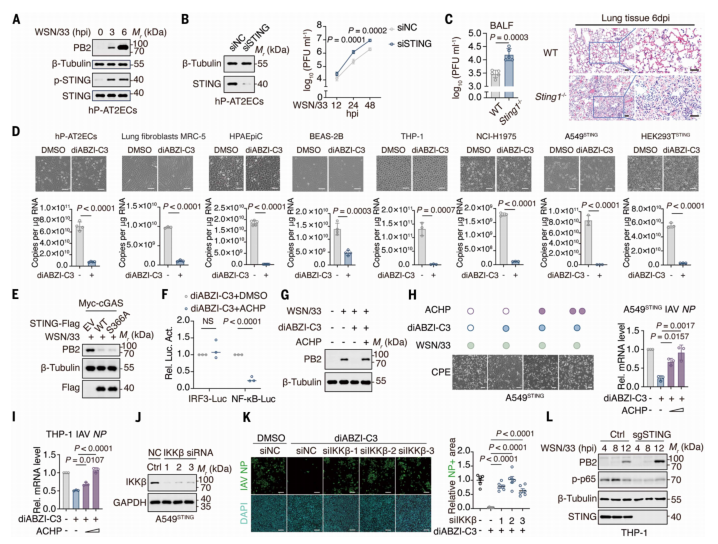
Figure1.STING 介导的对IAV的限制作用需要 NF-κB 信号通路参与
Result 2 STING Gly90位点是NF-κB激活的关键结构基础
通过构建包含90个点突变体的STING突变文库模型,进行了双荧光素酶报告实验。利用NF-κB luciferase报告系统和ISRE luciferase报告系统技术,发现Gly90突变选择性丧失NF-κB激活能力而保留IRF3功能。进一步通过构建G90A敲入细胞和G90A敲入小鼠模型,并进行RNA-seq转录组测序、病毒感染实验与TNF表达检测,证明Gly90是STING介导NF-κB抗病毒功能的核心结构位点。
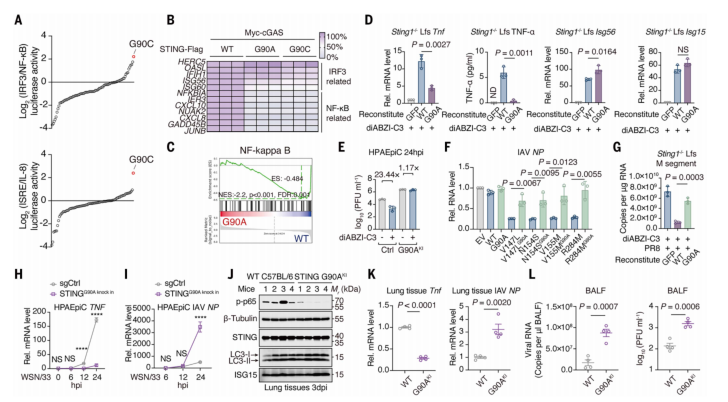
Figure2.STING 蛋白的第 90 位甘氨酸残基对于 NF-κB 的激活以及对IAV的抑制至关重要
Result 3 GADD34是STING–NF-κB下游关键抗病毒效应分子
构建cGAS/STING过表达模型,对该模型进行了RNA-seq转录组测序。通过差异基因表达分析筛选出了一组候选基因,并通过siRNA功能筛选技术,发现GADD34是最关键的下游抗病毒基因。进一步通过构建GADD34敲除细胞模型和Gadd34−/−小鼠模型,进行病毒感染实验与存活率分析,证明GADD34在体内外均发挥重要抗流感病毒作用。
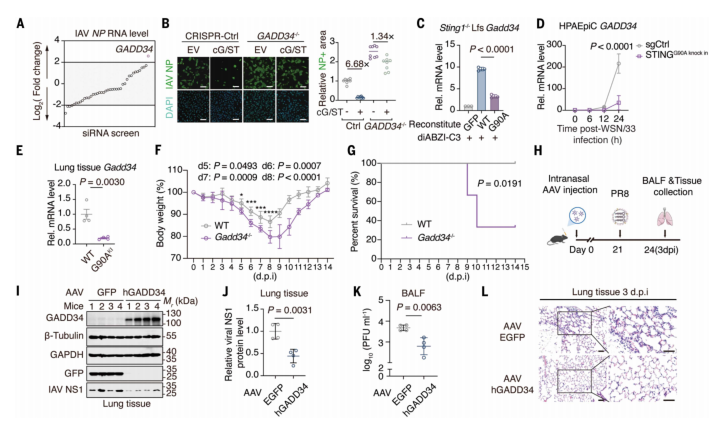
Figure3.GADD34 是一种由 STING-NF-κB 诱导的抗IAV因子
Result 4 GADD34通过抑制病毒聚合酶活性发挥作用
通过构建GADD34结构域缺失突变体模型,进行了病毒minireplicon实验。利用Co-IP蛋白互作检测技术和病毒聚合酶活性报告系统,发现GADD34通过PEST结构域与PB1、PB2、PA结合。进一步通过病毒RNA定量实验和蛋白表达检测实验,证明GADD34直接抑制病毒RNA聚合酶活性,且该作用不依赖其经典磷酸酶功能。
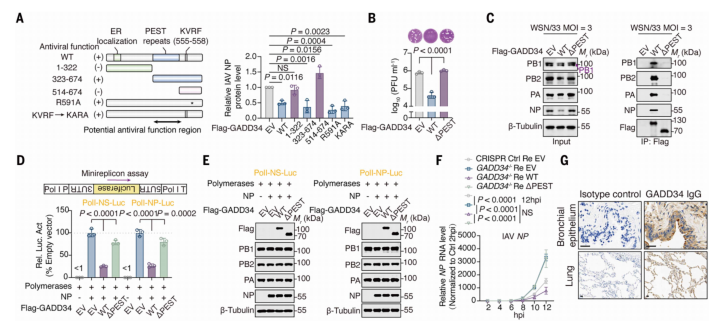
Figure4.GADD34 通过其 PEST 结构域以不依赖磷酸酶的方式抑制IAV
Result 5 人源IAV M1蛋白进化出逃逸STING屏障机制
通过构建了多种IAV来源的M1蛋白表达模型,进行STING信号抑制筛选实验。利用NF-κB luciferase检测技术和Co-IP互作检测技术,发现人源IAV M1可结合STING并抑制NF-κB激活。进一步通过构建M1 I115V和V115I突变体以及重组PR8病毒模型,通过病毒复制实验和小鼠感染实验,证明M1第115位Ile是病毒逃逸人源STING限制的关键适应性突变。
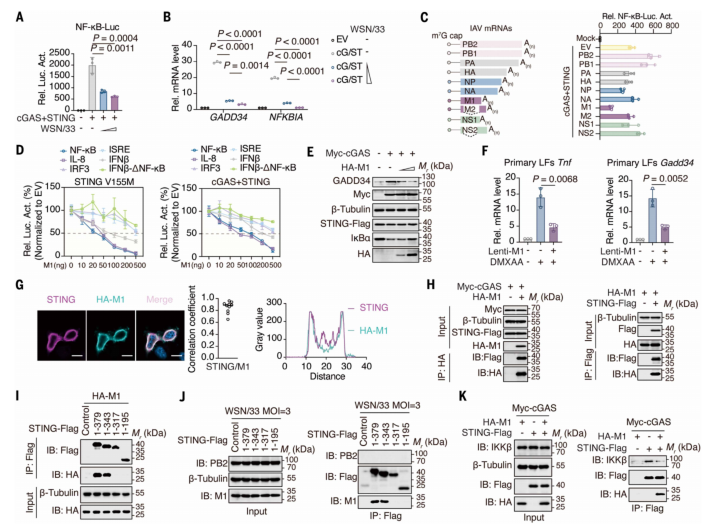
Figure5.IAV M1 蛋白会抑制 STING - NF-κB - GADD34 这一抗病毒通路
Result 6 STING构成禽源流感跨种传播分子屏障
通过构建STING野生型、STING缺失及G90A突变模型,进行了重组病毒感染实验。利用病毒滴度检测、TNF表达检测和肺组织病理学分析技术,发现携带M1 I115V突变的病毒在功能性STING系统中复制受限。进一步通过STING缺失背景对照实验,证明STING–NF-κB–GADD34信号轴构成限制禽源流感适应人类宿主的关键分子屏障。
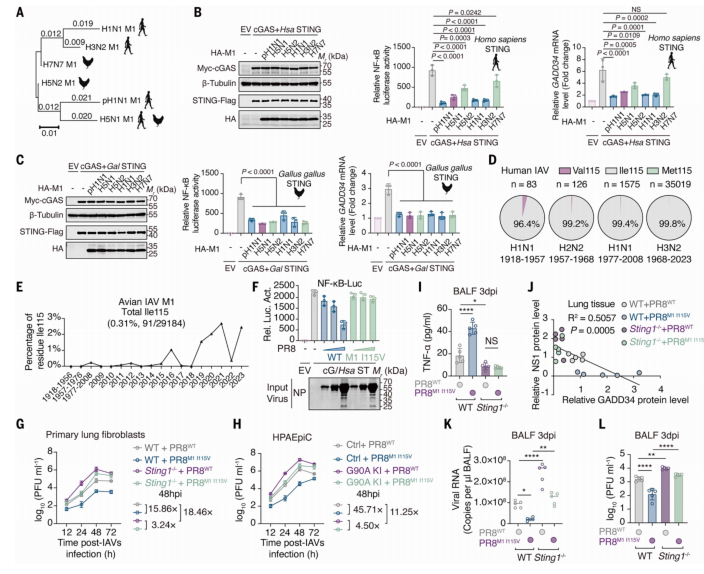
Figure6.STING 有助于限制IAV的跨种传播潜力
研究结论
本研究提出STING‑NF‑κB‑GADD34信号轴作为限制流感病毒跨种传播的重要先天免疫屏障。STING通过NF‑κB而非干扰素通路发挥关键抗病毒作用,而病毒通过M1蛋白Ile115突变实现对该屏障的适应性逃逸。该发现不仅深化了对RNA病毒天然免疫识别机制的理解,还提出M1‑115位点可作为预测流感跨种传播风险的重要分子标志。这一重要发现揭示l 新的跨种传播宿主限制机制,提出NF‑κB依赖型抗病毒新模式 ,在临床上,为流感疫情风险监测提供分子指标,并为靶向STING‑M1互作的抗病毒药物开发提供理论基础。
参考文献:
Ye R, Wang S, Hu Y, Pan Y, Zheng W, Xia F, Wang Y, Guo H, Zheng S, Wei W, Yu XF. STING-NF-κB signaling builds an influenza spillover barrier. Science. 2026 Feb 26;391(6788):eads4405. doi: 10.1126/science.ads4405. Epub 2026 Feb 26. PMID: 41747053.






