非小细胞肺癌(NSCLC)作为肺癌中最常见的类型,占所有肺癌病例的 80% 以上,免疫检查点抑制剂(ICIs)的出现为其治疗带来了革命性突破,成为临床一线治疗方案。但遗憾的是,仅有约 40% 的患者能从免疫治疗中获益,如何精准筛选适用人群,一直是临床亟待解决的难题。
近期,发表在国际知名期刊《Theranostics》2026 年第 16 卷的一项研究,为这一问题提供了全新答案。由武汉大学多家附属医院联合开展的研究团队,通过整合肿瘤微生物组和转录组分析,首次发现癌旁组织中的普雷沃菌(Prevotella)是 NSCLC 患者预后和免疫治疗疗效的关键预测标志物,其联合常规血液指标的诊断模型,预测准确性远超传统的 PD-L1 检测,为肺癌个性化免疫治疗开辟了新路径。

这项研究的核心,在于打破了以往仅关注肿瘤组织本身的研究局限,将目光投向了癌旁组织的微生物群落。研究团队收集了多组 NSCLC 患者的肿瘤组织和癌旁组织配对样本,利用 2bRAD-M 微生物测序和全转录组测序技术(欧易生物提供),构建了全面的微生物组和转录组图谱。通过条件互信息算法等多种生物信息学分析手段,系统解析了肿瘤内微生物与宿主基因的相互作用网络。
研究首先发现了一个有趣的现象:与肿瘤组织相比,癌旁组织的微生物丰富度、α 多样性和 β 多样性均显著更高,且在肺腺癌和肺鳞癌中,这种微生物分布的差异主要体现在肿瘤与癌旁组织之间,而非两种癌种之间。通过差异分析和随机森林筛选,研究团队锁定了慢生根瘤菌(Bradyrhizobium)和普雷沃菌两个关键菌属,它们均在癌旁组织中高度富集,且与 CD8+T 细胞、自然杀伤细胞、活化树突状细胞等抗肿瘤免疫细胞群密切相关。
而进一步的预后分析显示,这两种菌属的临床价值存在显著差异:癌旁普雷沃菌的高丰度与 NSCLC 患者的总生存期、疾病特异性生存期显著延长相关,是独立的预后良好指标;而慢生根瘤菌则与患者预后无明显关联。这一结果在 TCGA 公共数据库和包含 165 例患者的临床组织芯片中均得到验证,充分证实了癌旁普雷沃菌在肺癌预后评估中的重要价值。
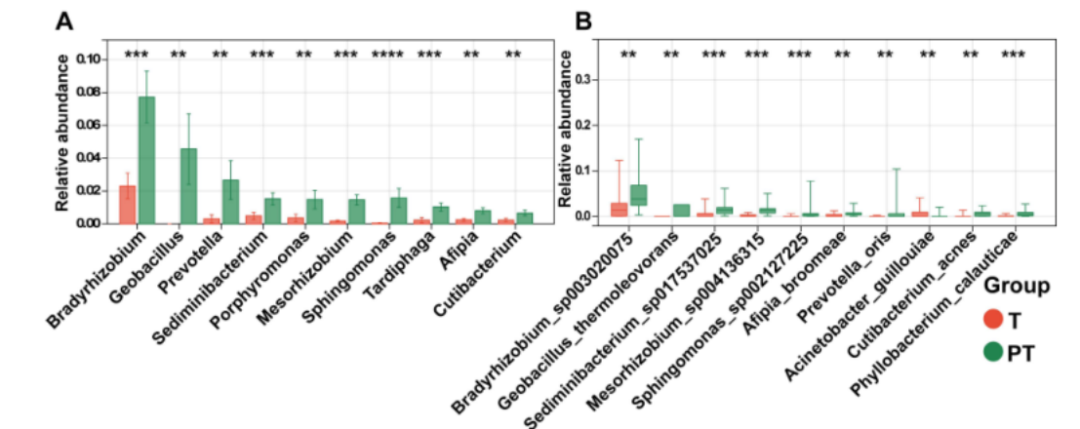
图1、肿瘤组织(T)与癌旁组织(PT)组间细菌类群的差异丰度。(A、B)箱线图显示:通过双侧配对Wilcoxon符号秩检验确定,PT组中前十大菌属(a)和物种(b)的相对丰度显著升高(*P < 0.05为统计学显著)。其中:*P < 0.05, P < 0.01, *P < 0.001, P < 0.0001。
那么,癌旁普雷沃菌究竟是如何影响患者免疫治疗疗效的?研究团队通过功能富集分析发现,普雷沃菌相关的宿主基因主要富集在 AMP 介导的免疫反应、黏膜固有免疫反应等多条免疫相关通路,且其丰度与肿瘤微环境中抗肿瘤免疫细胞的浸润水平呈显著正相关。更重要的是,普雷沃菌的丰度与 PD-L1 表达呈正相关,提示其可能通过调控肿瘤免疫微环境,增强免疫检查点抑制剂的治疗效果。
为了验证普雷沃菌对免疫治疗疗效的预测价值,研究团队纳入了 94 例接受抗 PD-L1 免疫治疗的 NSCLC 患者,结合患者的临床指标构建了预测模型。结果令人振奋:将癌旁普雷沃菌丰度与钙、年龄、血红蛋白等常规血液指标整合的联合诊断模型,预测免疫治疗疗效的 AUC 值达到 0.97,而传统的 PD-L1 检测 AUC 值仅为 0.66,癌旁普雷沃菌单独检测的 AUC 值也达到 0.86。
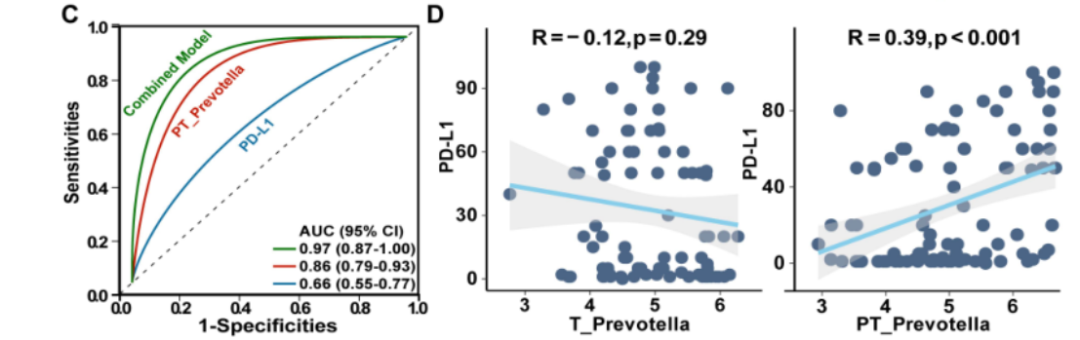
图2、(C) 采用联合诊断模型、癌旁组织来源的普雷沃菌(Prevotella)及PD-L1预测免疫治疗响应的ROC曲线。(D) 肿瘤组织(T)与癌旁组织(PT)来源的普雷沃菌同PD-L1表达的相关性分析(采用双侧Spearman等级相关检验,P < 0.05视为统计学显著)。
同时,研究团队还探索了该标志物对 EGFR 靶向治疗的预测价值,发现癌旁普雷沃菌对靶向治疗疗效的预测能力有限,提示其是免疫治疗特有的预测标志物,这也为临床治疗方案的选择提供了精准依据。
这项研究的意义,不仅在于发现了一个全新的肺癌免疫治疗预测标志物,更在于为肿瘤微生物组的研究提供了新的思路。以往的肿瘤微生物研究多聚焦于肠道微生物或肿瘤组织内微生物,而该研究证实,癌旁组织的微生物群落同样是肿瘤微环境的重要组成部分,其与宿主的相互作用深刻影响着肿瘤的发生发展和治疗反应。
此外,该研究构建的联合诊断模型,仅需检测癌旁普雷沃菌丰度和常规血液指标,检测方法简便、成本低廉,易于在临床推广应用,为实现 NSCLC 患者的个性化免疫治疗提供了可行的工具。相较于传统的 PD-L1 检测,该模型的高预测准确性,能更大程度地筛选出免疫治疗获益人群,减少无效治疗,降低患者的治疗成本和不良反应。
当然,研究也存在一定的局限性,比如普雷沃菌的体外培养尚未成功,其调控肿瘤免疫微环境的具体分子机制仍需进一步探索,且预测模型仍需更大样本量的多中心临床研究验证。但不可否认的是,这项研究为肺癌的精准治疗打开了新的窗口,也让肿瘤微生物组成为肿瘤免疫治疗领域的重要研究方向。
随着对肿瘤微生物与宿主相互作用机制的深入解析,未来有望通过调控微生物群落(如益生菌补充、菌群移植等)来重塑肿瘤免疫微环境,增强免疫治疗疗效,为肺癌患者带来更多的治疗选择。而癌旁普雷沃菌这一标志物的发现,也为后续临床研究和转化应用奠定了坚实基础,相信在不久的将来,肿瘤微生物组将成为肿瘤精准治疗的重要靶点,为更多癌症患者带来希望。
参考文献:
Wang N, Ma L, Huang Y, et al. Tumor microbiome-transcriptome crosstalk identifies Prevotella as an immunotherapy predictive predictor in NSCLC. Theranostics 2026; 16(7):3426-3446.






