一项最新研究揭示,肠道中的大肠杆菌竟会“策反”免疫细胞,成为癌症转移的帮凶。
你是否知道,我们肠道内数以万亿计的细菌,一直在与我们的身体进行着复杂的“对话”?当结直肠癌发生时,这场对话的走向可能决定着患者的命运。
近日,一项发表在《自然-通讯》上的研究为我们揭开了一个令人惊讶的真相:来自中国福建医科大学的研究团队发现,原本普普通通的大肠杆菌,竟然会通过一系列精密的分子操作,帮助结直肠癌细胞向肝脏转移。

一个危险的“三人组”
研究团队首先发现了一个关键线索:在有肝转移的结直肠癌患者组织中,大肠杆菌的数量明显高于没有转移的患者。(应用了欧易生物2bRAD-M®微生物检测技术)
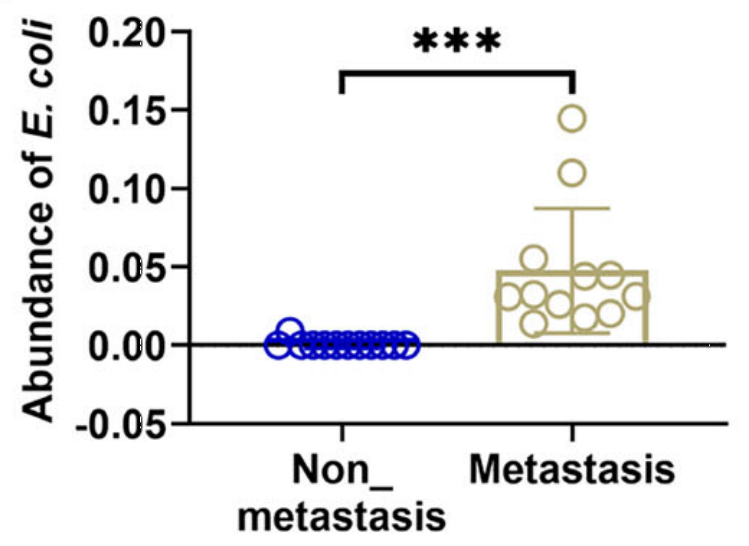
图1、有肝转移的患者组织中大肠杆菌的数量明显高于没有转移的
这是巧合吗?研究人员的进一步实验给出了否定答案。
当将大肠杆菌与结直肠癌细胞一起注入小鼠体内时,肿瘤的生长速度加快,肝转移增多,而且癌细胞的“侵略性”明显增强——它们变得更擅长离开原发部位,向远处扩散。
那么,大肠杆菌是如何做到这一点的呢?
被“策反”的免疫细胞
正常情况下,中性粒细胞是我们身体对抗细菌感染的第一道防线。当大肠杆菌入侵时,中性粒细胞应该挺身而出,消灭这些细菌。
但在这项研究中,科学家们发现了令人震惊的逆转:大肠杆菌竟然“策反”了中性粒细胞。
具体来说,大肠杆菌通过激活中性粒细胞中的RIPK2蛋白,启动了一系列连锁反应。这个RIPK2就像是细胞内一个被打开的“开关”,它招募了另一个叫做HNRNPK的蛋白,后者进一步激活了两个关键转录因子:ATF3和RelB。
这两个转录因子联手,启动了一个叫做Ncf4的基因表达。NCF4蛋白是NADPH氧化酶复合物的一部分,它的活跃导致中性粒细胞释放出一种叫做“中性粒细胞胞外陷阱”(NETs)的结构。
这些NETs原本是为了捕捉和杀死细菌而设计的“渔网”,但在这里,它们却变成了帮助癌细胞转移的工具。
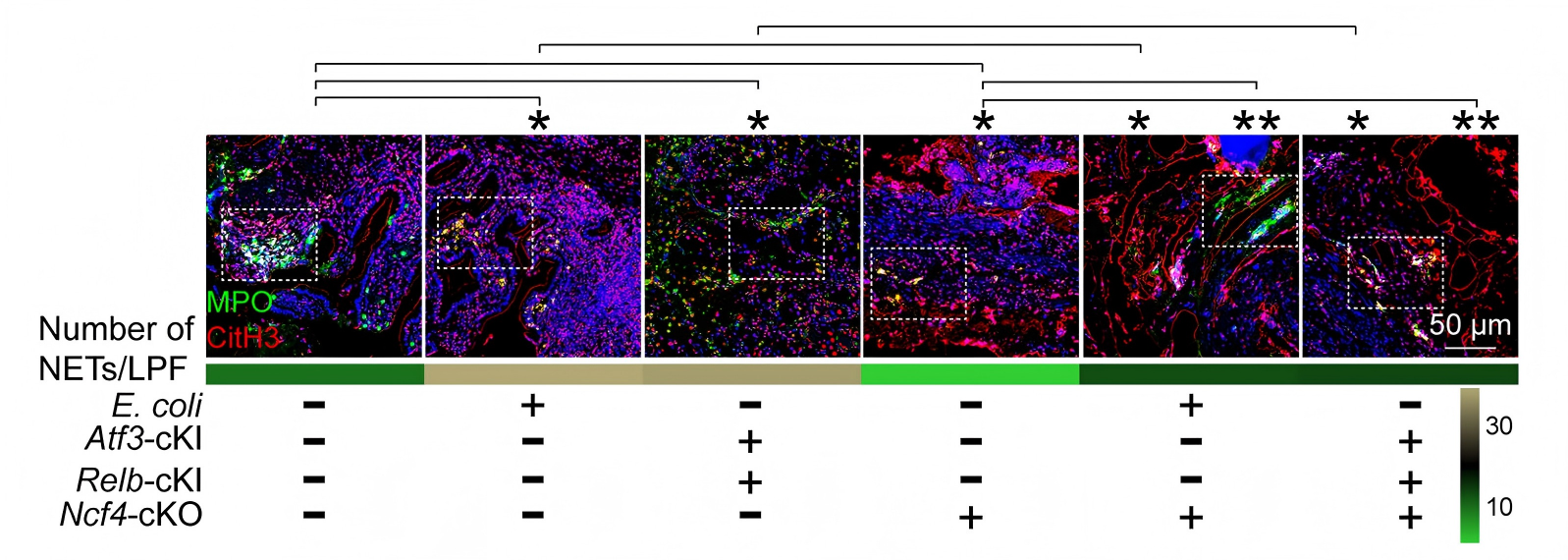
图2、小鼠结直肠癌组织中中性粒细胞胞外陷阱的免疫荧光
癌细胞的“钙离子盛宴”
当中性粒细胞释放的NETs包围癌细胞时,它们引发了癌细胞内部的剧烈变化。
研究发现,NETs会刺激结直肠癌细胞表面的一个钙通道蛋白——TRPC1大量表达。这就像是给癌细胞打开了一扇钙离子涌入的大门。
细胞内钙离子浓度的升高,激活了另一个蛋白NFATC3,而NFATC3反过来又促进了TRPC1的表达。这就形成了一个自我强化的正反馈循环:更多的TRPC1意味着更多的钙离子内流,而更多的钙离子内流又进一步促进TRPC1的表达。
这场“钙离子盛宴”的直接后果是激活了两个关键蛋白:S100A8和S100A9。这两个蛋白在钙离子的帮助下形成了紧密的二聚体。
致命的“三人行”
S100A8/9二聚体随后与STAT3蛋白结合,形成了一个异源三聚体。这个三聚体进入细胞核后,发挥了一个特殊的“建筑师”功能。
我们的DNA在细胞核内并不是随机散落的,而是经过精密折叠和组织的。基因的激活需要远处的“增强子”和基因本身的“启动子”在空间上靠近,形成一个叫做“增强子-启动子环”(EPLs)的结构。
STAT3/S100A8/9三聚体恰恰起到了稳定这种环状结构的作用。研究发现,这个三聚体特别稳定了一个叫做Tns1的基因的增强子-启动子环。
TNS1蛋白是一种促进细胞运动和侵袭的因子。当它的表达上调时,结直肠癌细胞的转移能力大大增强。
治疗新希望
这项研究的发现不仅揭示了结直肠癌肝转移的新机制,更重要的是提供了多个潜在的治疗靶点。
研究团队测试了几种药物组合,发现同时靶向RIPK2(用GSK583)、STAT3(用Stattic)和S100A8/9(用Paquinimod)能够最有效地抑制大肠杆菌诱导的肿瘤转移。
相比直接使用抗生素清除大肠杆菌,这种靶向治疗策略可能更为可靠。因为广谱抗生素会破坏肠道菌群的整体平衡,反而可能带来不可预测的后果。
启示与展望
这项研究为我们理解肠道菌群与肿瘤免疫的相互作用提供了全新的视角。它揭示了一个复杂的多步骤过程:从肠道细菌开始,到“策反”中性粒细胞,再到NETs释放,最后激活癌细胞内部的钙信号和基因调控网络,最终促进转移。
这就像是一部精心编排的“背叛”剧本,而大肠杆菌则是一位高明的“导演”。
未来的研究还需要进一步探索:如何在不破坏整体免疫功能的前提下,阻断这一过程?能否通过调节肠道菌群来降低结直肠癌患者的转移风险?
对于患者而言,这项研究也提示:维持肠道菌群健康,避免有害细菌过度生长,可能是预防肿瘤转移的重要一环。当然,具体如何操作还需要更多临床研究的指导。
无论如何,这项研究让我们离解开癌症转移之谜又近了一步。在对抗癌症的道路上,每一个新机制的揭示,都是我们迈向胜利的一小步。
参考文献:Pan B, Yao Y, Zhang Z, et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nature Communications. 2026. DOI: 10.1038/s41467-026-69005-y






