
前言

2026年3月18日,成都医学院陈虎、李逢添团队联合西南医科大学、中山大学等单位在Nature Communications在线发表了题为 “Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression” 的论文。本研究利用单细胞转录组和空间转录组技术,解析了口腔鳞状细胞癌(OSCC)肿瘤微环境的细胞组成与空间分布特征,发现髓源性抑制细胞(MDSCs)的空间分布随OSCC进展发生动态重塑,ANXA1-FPR2信号轴是介导MDSCs募集和免疫抑制的核心通路;阻断该信号轴可显著提升免疫检查点抑制剂对OSCC的治疗效果,为改善OSCC免疫治疗疗效提供了全新的靶向策略。欧易生物提供了单细胞转录组、空间转录组的测序工作。
发表期刊
Nature Communications
影响因子
15.7
涉及的欧易生物服务产品
单细胞转录组测序、空间转录组测序

研究背景

口腔鳞状细胞癌(OSCC)是高发头颈部恶性肿瘤,近60%患者确诊时为晚期,传统疗法疗效有限,免疫检查点阻断(ICB)治疗虽带来希望,但肿瘤微环境(TME)的免疫抑制异质性导致患者响应率差异显著。髓源性抑制细胞(MDSCs)是OSCC免疫抑制核心,可抑制CD8+ T细胞功能、放大肿瘤免疫逃逸,但其在OSCC进展中与其他细胞的时空互作及空间分布调控通路尚不明确。ANXA1-FPRs信号调控免疫细胞募集极化,FPR2被证实与T细胞耗竭相关,探究该信号对MDSCs空间异质性的调控,有望为破解OSCC免疫治疗耐药提供新靶点。

研究内容

本研究通过单细胞转录组测序揭示OSCC肿瘤微环境的细胞组成及功能变化,空间转录组技术明确了MDSCs在OSCC进展中的空间分布特征;通过细胞间通讯分析、多重免疫荧光验证,揭示了ANXA1-FPR2信号轴介导MDSCs从肿瘤核心向边缘迁移、并与CD8+ T细胞共定位进而增强免疫抑制的分子机制;最后在OSCC小鼠模型中证实,FPR2拮抗剂与抗PD-1抗体的联合治疗可显著清除MDSCs、恢复CD8+ T细胞功能,大幅提升免疫治疗效果。该研究首次阐明了OSCC中MDSCs空间异质性的调控机制,为OSCC的免疫联合治疗提供了新的潜在靶点。

技术路线

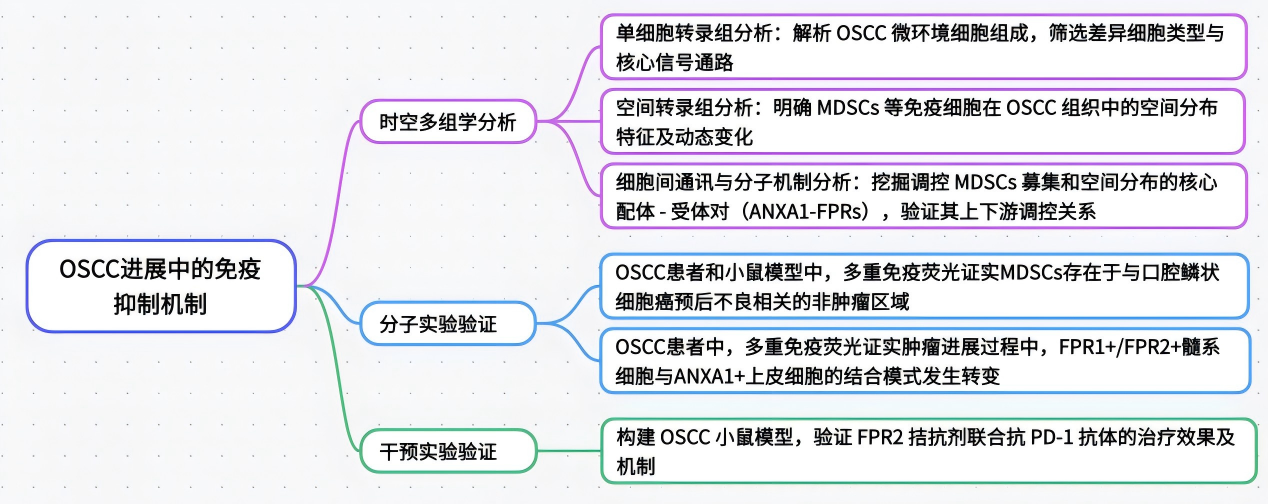

研究结果

1.单细胞转录组揭示晚期OSCC存在典型的免疫抑制性肿瘤微环境
对早期(N=7)和晚期(N=9)OSCC样本进行单细胞RNA测序,鉴定出10种细胞类型,包括鳞状上皮细胞、CD8⁺T细胞、髓系细胞、成纤维细胞等(图1a~d)。结果显示,晚期OSCC中CD8+ T细胞数量显著减少,且其T细胞受体(TCR)信号通路富集程度显著降低,功能受损;而髓系细胞的免疫抑制信号通路显著激活,抗原提呈功能受损(图1e~i)。同时,晚期OSCC上皮细胞的染色体异常更显著,恶性程度更高,提示晚期OSCC肿瘤微环境呈现出CD8+ T细胞功能耗竭、髓系细胞介导免疫抑制的典型特征。
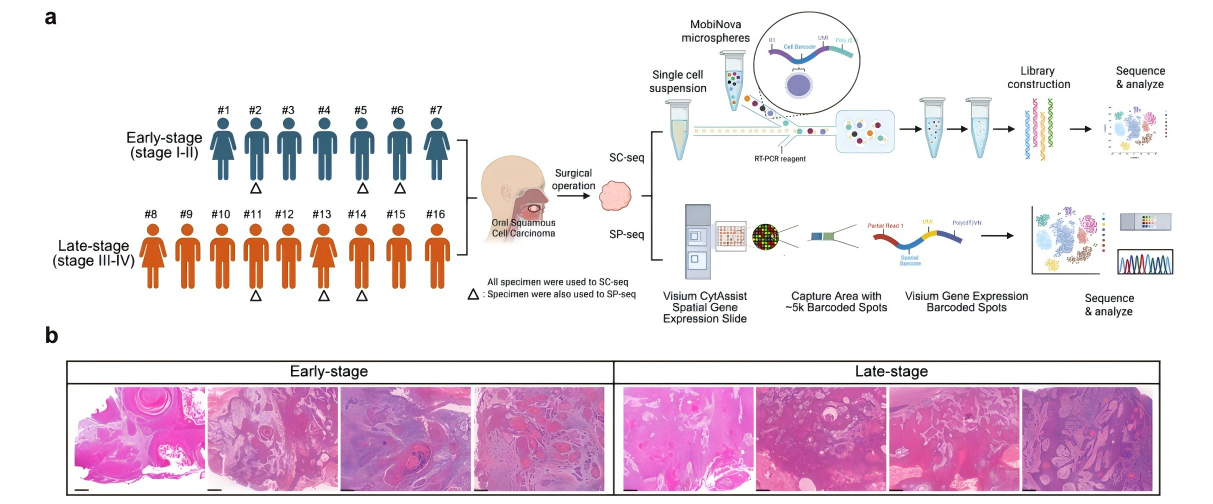
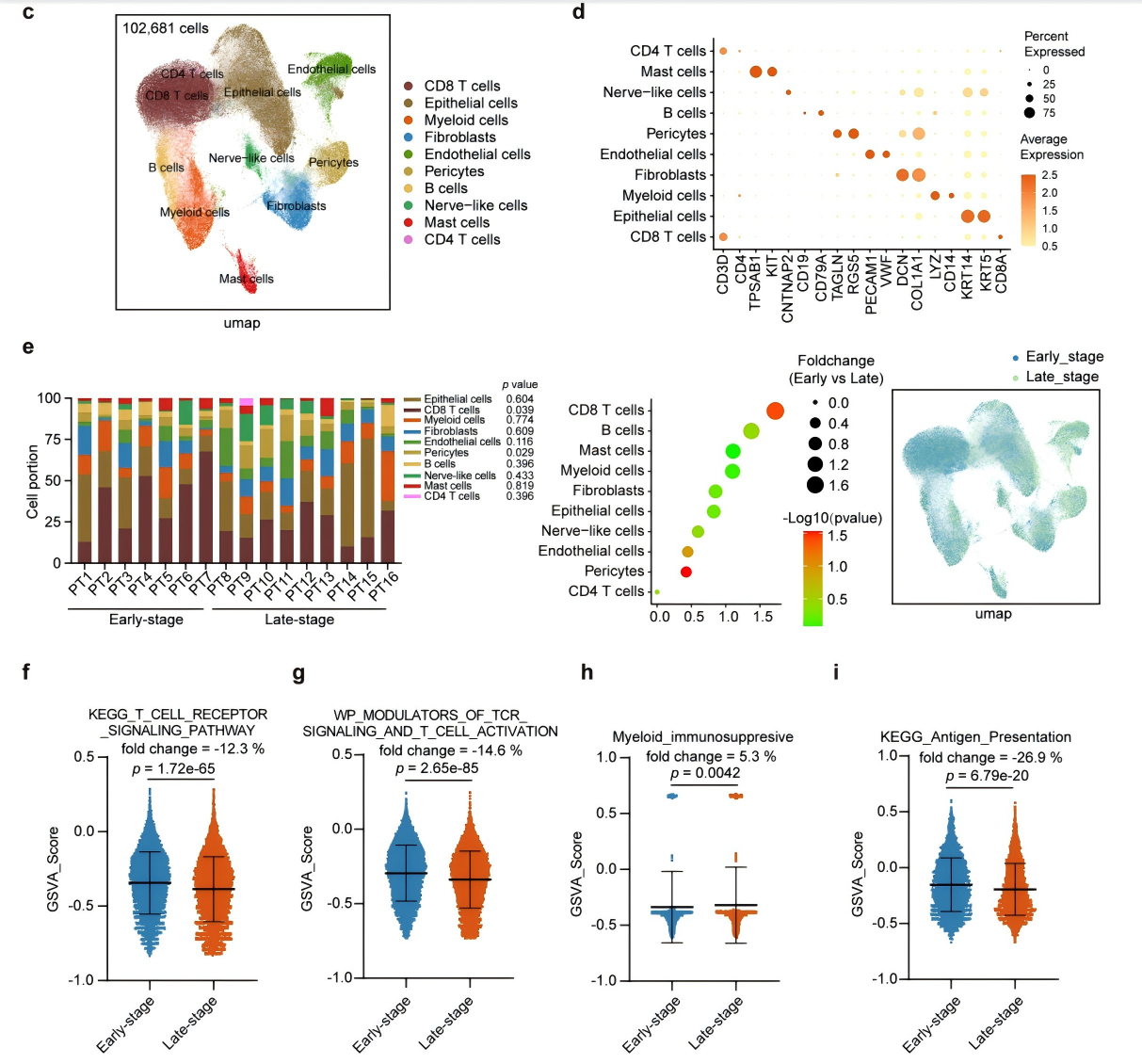
图1 单细胞RNA测序揭示了早期和晚期口腔鳞状细胞癌的肿瘤微环境
2.晚期口腔鳞状细胞癌中上皮肿瘤细胞与髓源性抑制细胞的通讯减弱
细胞间通讯分析发现,早期OSCC中上皮肿瘤细胞与髓系细胞的相互作用显著增强,且主要由ANXA1-FPR1、ANXA1-FPR3配体-受体对介导;而晚期OSCC中这两种相互作用显著减弱,ANXA1-FPR2成为代偿性的核心通讯对(图2a~d)。进一步分析发现,FPR1/2主要在MDSCs中表达,FPR3主要在肿瘤相关巨噬细胞(TAM)中表达,且晚期OSCC中FPR2高表达的MDSCs占比显著增加(图2g~o),提示MDSCs是ANXA1-FPRs信号介导肿瘤-免疫细胞通讯的核心细胞,且ANXA1-FPR2是晚期OSCC的代偿性调控通路。
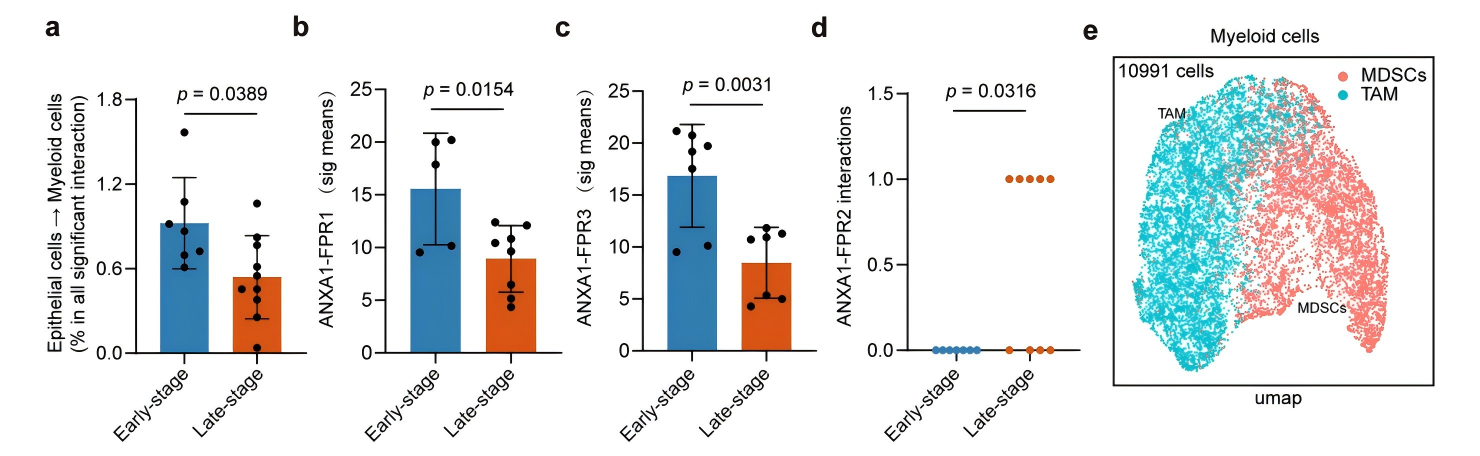
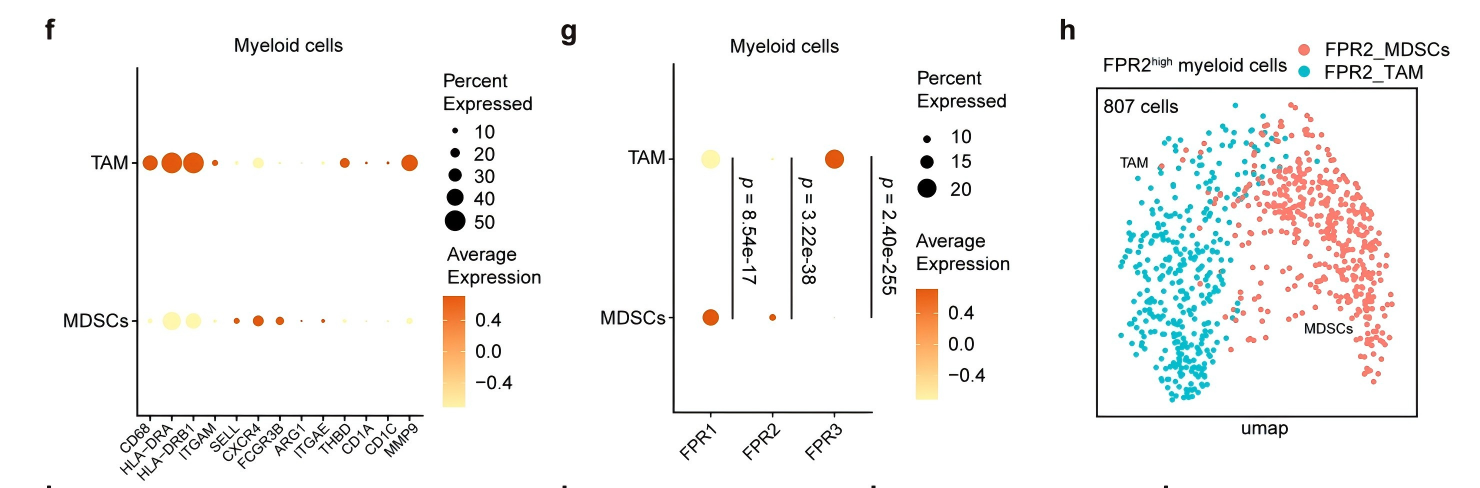
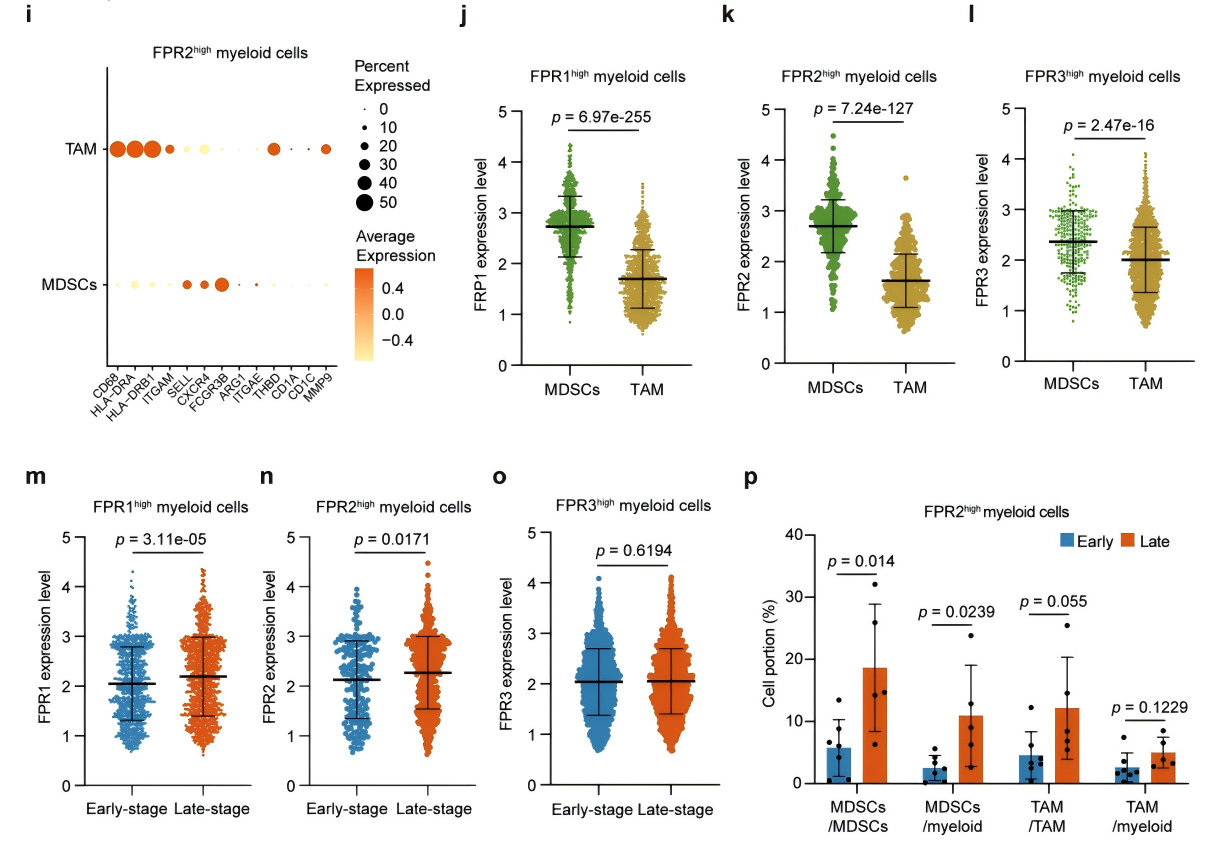
图2 上皮肿瘤细胞与MDSCs之间的相互作用在晚期OSCC中减少
3.晚期OSCC中MDSCs向肿瘤边缘重分布,与CD8+ T细胞共定位并关联不良预后
结合空间转录组技术与RCTD细胞类型反卷积分析,将OSCC组织分为肿瘤细胞贫乏区(R1区)和富集区(R2区),发现早期OSCC中MDSCs主要富集于R2区,而晚期MDSCs则显著向肿瘤边缘迁移,该空间重分布为MDSCs特有(图3a,b)。邻域分析发现,早期OSCC的髓系细胞主要富集于上皮细胞的同一位点,而晚期髓系细胞则主要分布于相邻位点和远端位点(图4a、b),同时在晚期OSCC中CD8+ T细胞也主要定位于肿瘤细胞贫乏区,与MDSCs形成共定位(图4c);早期髓系细胞在同一位点的占比最高,在相邻和远端位点中占比降低(图4d~f);晚期成纤维细胞在同一位点占比最高,髓系细胞在相邻和远端位点占比增加(图4g~i)。单细胞转录组显示ANXA1在多数细胞类型中均有表达,而空间转录组则发现其在上皮肿瘤细胞富集区表达上调(图4j)。进一步分析显示,早期MDSCs倾向于定位于肿瘤细胞富集区,而晚期MDSCs和早晚期TAM均主要分布于肿瘤细胞贫乏区(图4k)。多重免疫荧光实验验证了这一空间特征(图5),且MDSCs与肿瘤细胞区域的重叠程度越低,OSCC患者总生存期越差,提示MDSCs的空间重分布是OSCC免疫抑制和不良预后的重要标志。
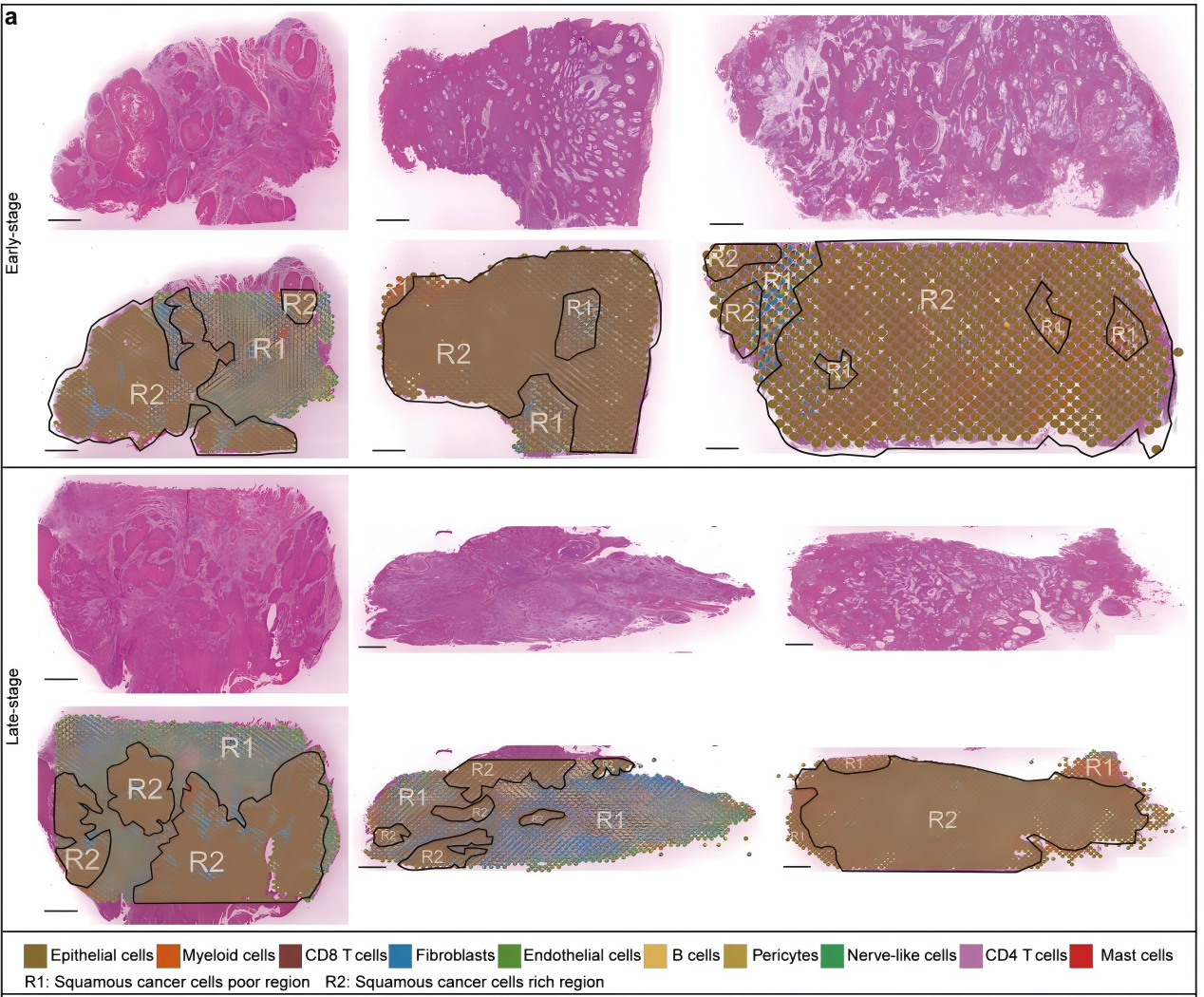
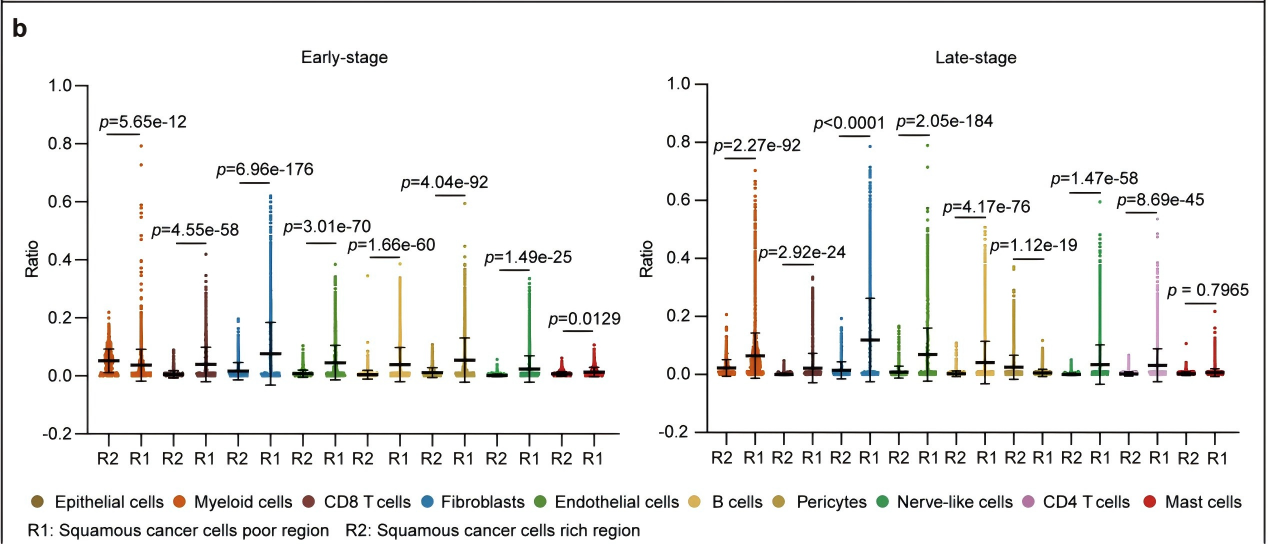
图3 空间转录组分析揭示了早期和晚期口腔鳞状细胞癌中髓样细胞的不同分布模式
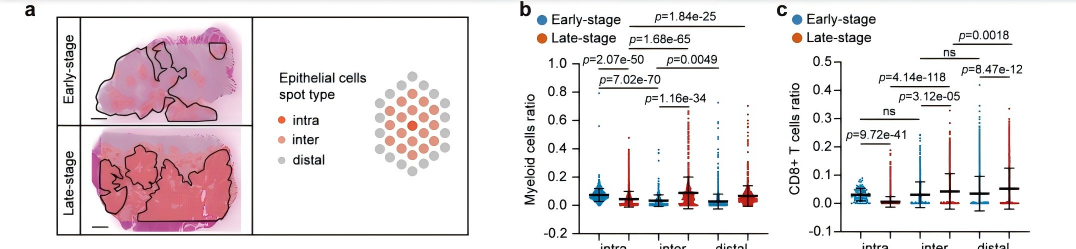
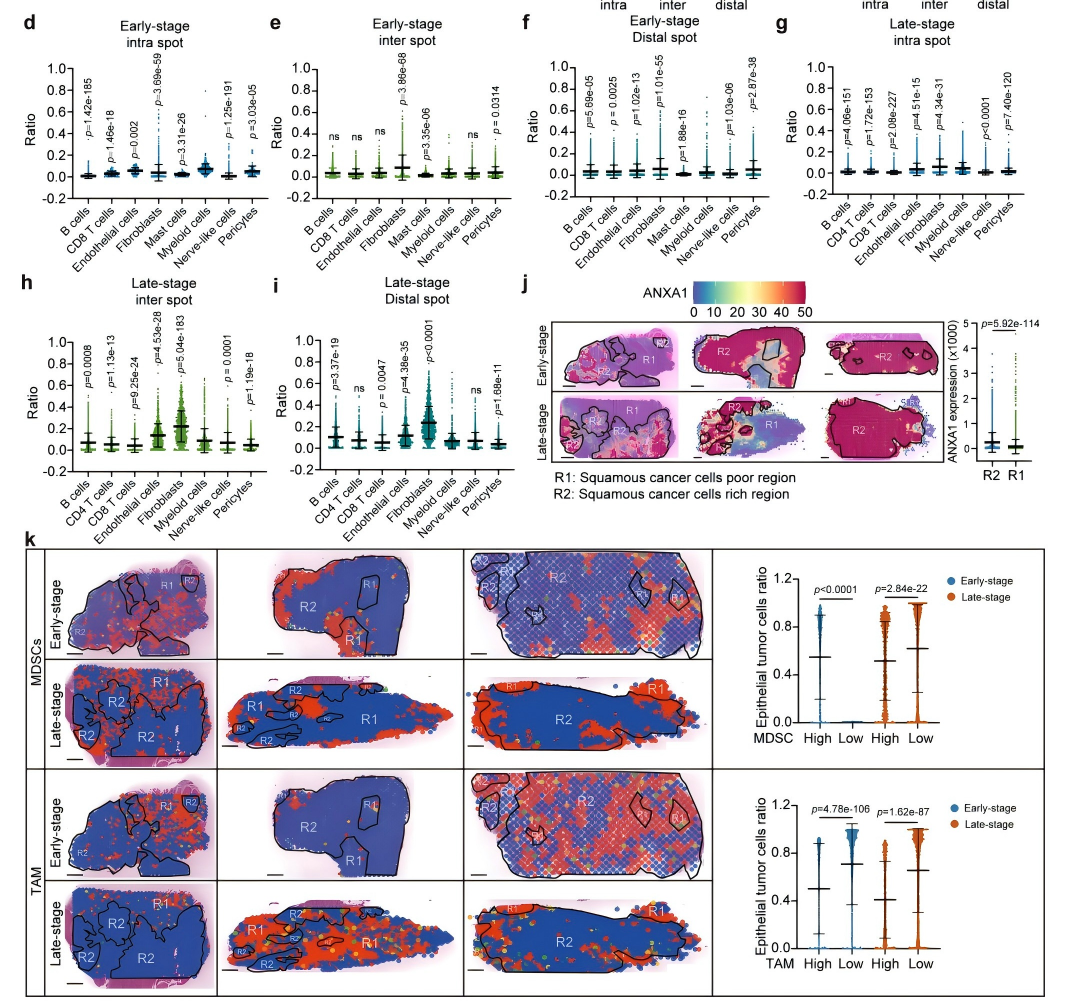
图4 早期OSCC中,R2区域聚集的髓样细胞是MDSCs,而非TAM。
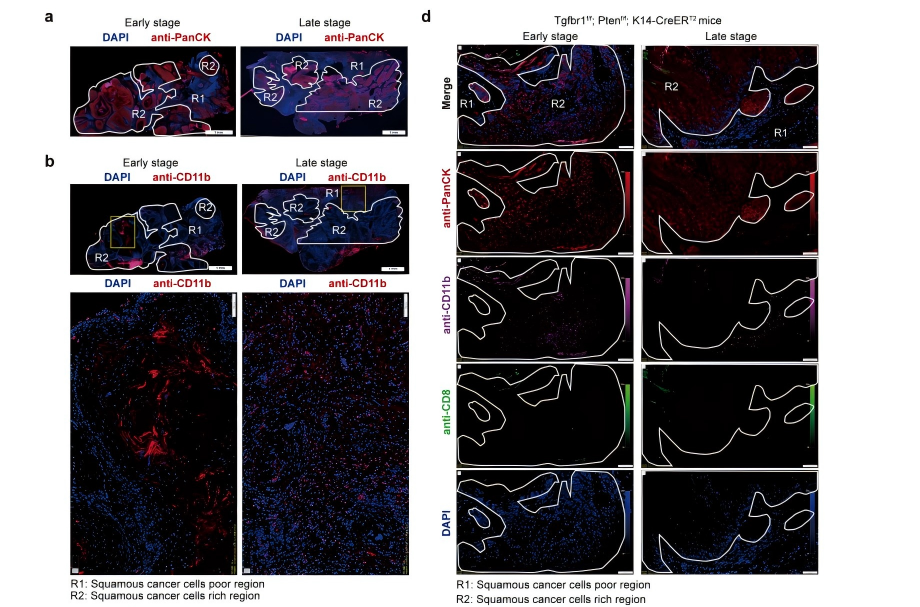
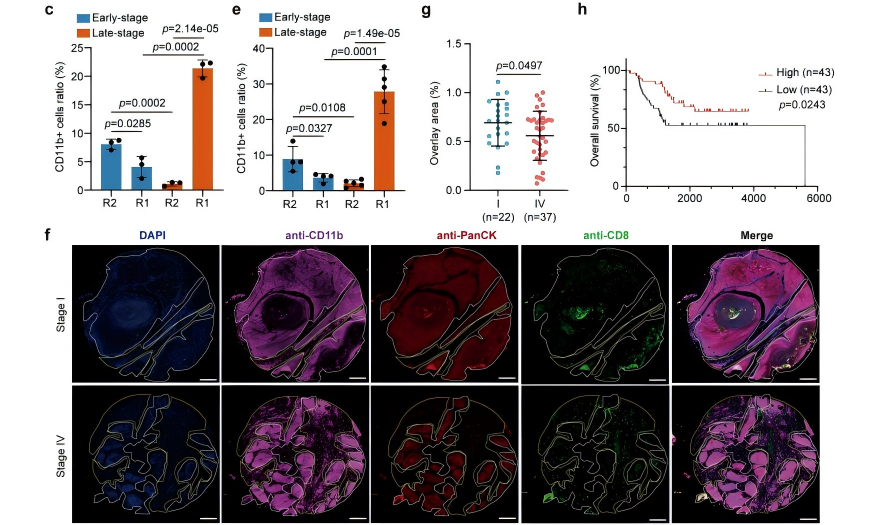
图5 MDSCs存在于与口腔鳞状细胞癌预后不良相关的非肿瘤区域
4.肿瘤进展过程中,FPR1⁺或FPR2⁺髓系细胞与ANXA1⁺上皮细胞的结合模式发生转变
单细胞转录组结果显示,早期口腔鳞状细胞癌中上皮肿瘤细胞与髓系细胞间的ANXA1-FPR1通讯作用增强,而晚期ANXA1-FPR2通讯作用增强。为进一步验证该结果,研究利用多重免疫组化检测了对应标本中这三种蛋白的表达。结果显示,与ANXA1阳性上皮肿瘤细胞相邻的FPR1阳性髓系细胞在晚期显著减少,而FPR2阳性髓系细胞则显著增加(图6a、b);且晚期ANXA1的蛋白水平下调,FPR2蛋白水平上调,FPR1蛋白水平则无显著变化(图6c、d),与单细胞转录组结果一致。以上结果表明,ANXA1表达下调可能导致上皮肿瘤细胞与髓系细胞间的FPR1相互作用减弱,而FPR2表达上调则试图代偿这种细胞间通讯。
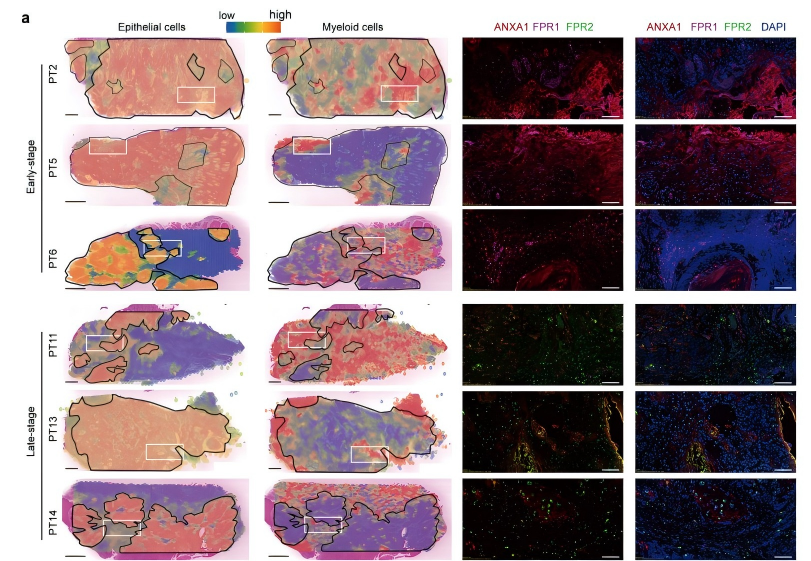
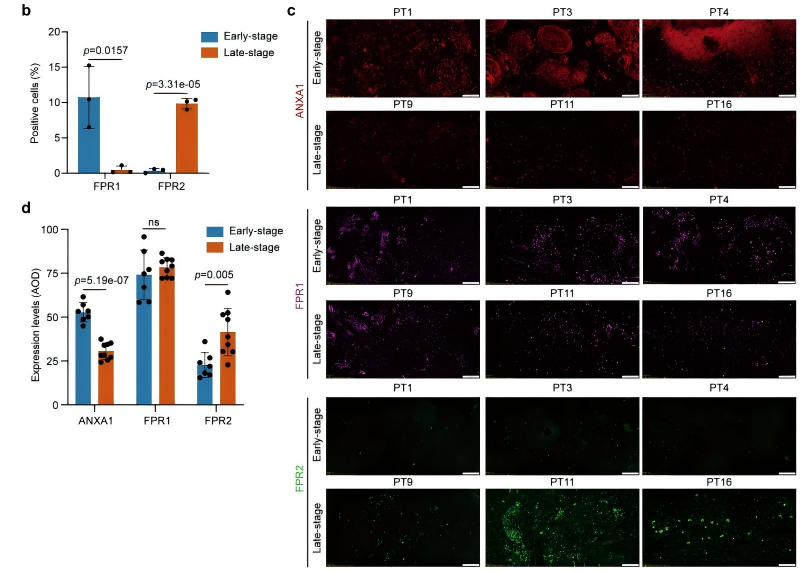
图6 FPR1/2阳性的髓系细胞与ANXA1阳性的上皮肿瘤细胞之间存在相互关联
5.ANXA1高表达上皮肿瘤细胞是调控MDSCs的核心亚群
对OSCC上皮肿瘤细胞进行亚群分析,鉴定出ANXA1高表达(ANXA1high_Epi)和低表达(ANXA1low_Epi)两个亚群,其中ANXA1high_Epi是与MDSCs发生通讯的核心亚群,且其干细胞特性显著更高,提示该亚群在肿瘤发生早期即参与MDSCs募集(图7a~f)。随着OSCC进展,两个亚群的ANXA1表达均显著下调,导致肿瘤细胞与MDSCs间的ANXA1-FPRs通讯减弱,这是MDSCs发生空间重分布的重要分子基础(图7c);同时,晚期ANXA1high_Epi的干扰素应答信号和抗原提呈通路显著下调,进一步加剧了肿瘤免疫逃逸(图7h)。
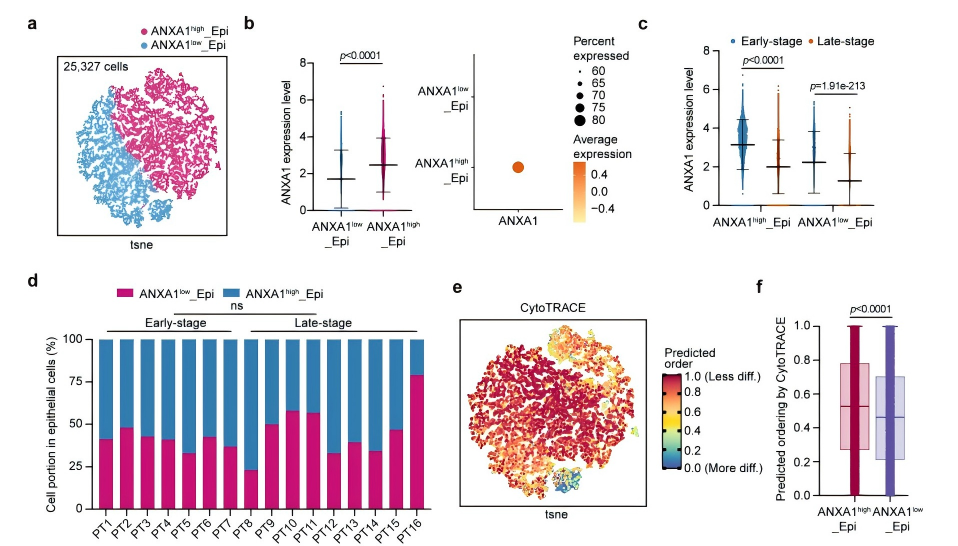
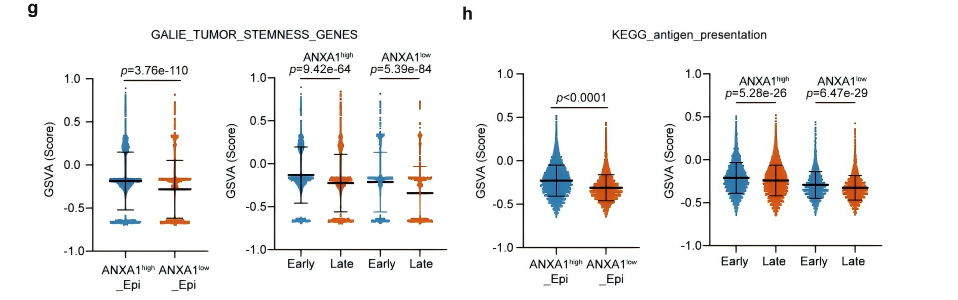
图7 ANXA1high的上皮肿瘤细胞能够促进与髓系细胞的相互作用
6.FPR2拮抗剂联合抗PD-1抗体可增强口腔鳞状细胞癌小鼠模型的治疗应答
构建SCC7细胞皮下接种的OSCC小鼠模型,将小鼠分为IgG对照、WRW4单药、抗PD-1单药、WRW4+抗PD-1联合治疗四组(图8a)。结果显示,单药治疗对肿瘤生长的抑制作用极弱,且几乎不延长小鼠生存期;而联合治疗可显著抑制肿瘤生长,大幅延长小鼠生存时间(图8b~d)。进一步的病理检测发现,联合治疗组肿瘤组织中MDSCs浸润显著减少,CD8⁺T细胞浸润显著增加,且CD8⁺T细胞的细胞毒性功能显著恢复(图8e~g),证实ANXA1-FPR2阻断可有效逆转OSCC免疫抑制微环境,增强免疫检查点抑制剂的治疗效果。
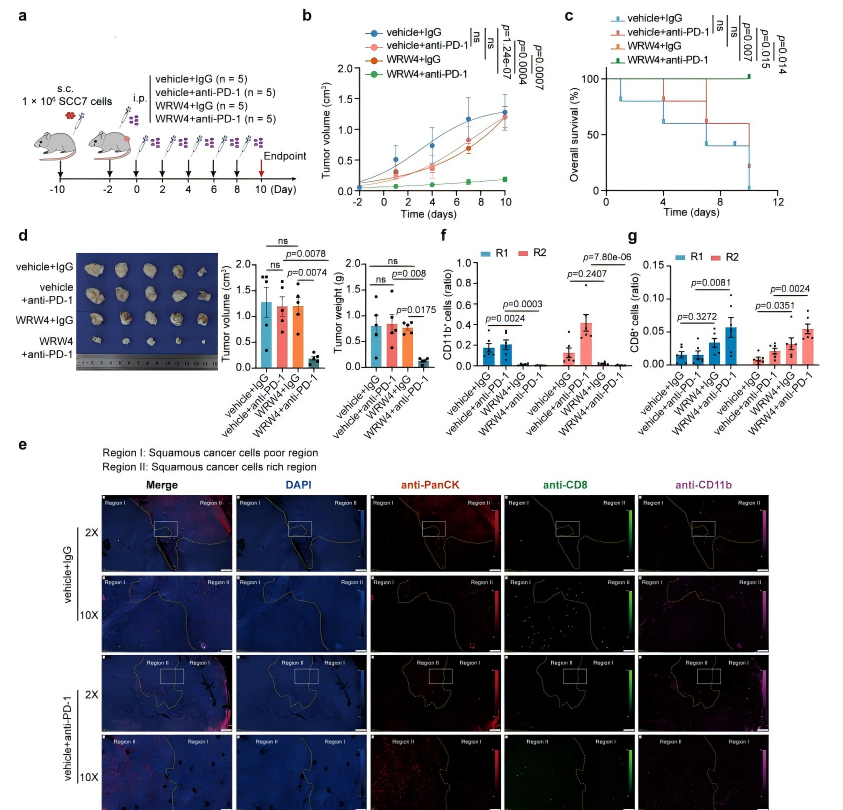

图8 抑制FPR2可增强免疫检查点阻断疗法的抗肿瘤效果

研究结论

本研究从多层面解析ANXA1-FPRs信号对OSCC的调控机制:机制上,OSCC进展中MDSCs从肿瘤核心迁至边缘并与CD8⁺T细胞共定位,是OSCC免疫治疗耐药的关键原因,ANXA1-FPR2是调控其募集、分布的核心通路,晚期通过代偿维持抑制效应;分子上,ANXA1high_Epi表达下调使ANXA1-FPR1/3通讯减弱,ANXA1-FPR2代偿驱动MDSCs迁移并抑制CD8⁺T细胞;治疗上,FPR2拮抗剂可阻断该信号,与抗PD-1抗体联用显著提升晚期OSCC免疫治疗效果。研究首次揭示MDSCs空间异质性调控机制,提出新型治疗策略,为OSCC及其他实体瘤研究提供新靶点与参考。

欧易点评

本文借助单细胞转录组联合空间转录组技术,结合细胞间通讯分析、动物模型验证等多手段,系统揭示ANXA1-FPRs信号调控MDSCs空间异质性在口腔鳞状细胞癌(OSCC)免疫抑制中的核心作用。研究创新性阐明:OSCC进展中MDSCs从肿瘤核心向边缘重分布并与CD8⁺ T细胞共定位是免疫治疗耐药的关键,ANXA1ʰⁱᵍʰ_Epi亚群表达下调引发ANXA1-FPR1/3通讯减弱,ANXA1-FPR2轴代偿性激活介导MDSCs募集、分布及免疫抑制。并通过OSCC小鼠模型验证FPR2拮抗剂联合抗PD-1抗体的协同治疗作用,显著逆转免疫抑制微环境。文章整合空间分布、分子机制到治疗验证数据,完整勾勒OSCC免疫抑制调控网络,为“靶向MDSCs空间调控+免疫检查点阻断”治疗策略提供理论与实验依据,临床转化价值与研究参考价值兼具。

参考文献

Li F, Han Y, Ou F, Deng L, Li H, Yu X, Yi Y, Ma R, Wu Z, You Z, Chen H. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun. 2026 Mar 18;17(1):2535. doi: 10.1038/s41467-026-70861-x. PMID: 41851114; PMCID: PMC13000289.






