前言
你是否曾经历经期剧痛、经量过多、甚至因此影响生育?你可能听说过子宫腺肌症。这种被称为“不死的癌症”的妇科顽疾,影响着全球高达20%-30%的育龄女性,但其病因一直是个谜。医生们长久以来都认为这与激素、炎症或遗传因素有关。但一项发表于国际顶级期刊《Advanced Science》(IF14.1)上的突破性研究,为我们揭开了背后一个惊人的秘密:子宫腺肌症的发生,可能源于一种特定细菌的感染,它通过驱动一种前所未见的细胞“身份转换”,导致了疾病的形成。
这不仅仅是发现了新的致病菌,更是打开了一扇全新的诊疗大门。今天,就让我们一起走进这项来自中国科研团队的原创性发现。

新机制:上皮细胞“变身”为内皮细胞
要理解这个新发现,首先得了解腺肌症的核心病变:原本应该老实待在子宫腔内的子宫内膜腺体和间质,“跑”到了子宫的肌肉层(肌层)里生长,引发了疼痛、出血和不孕。
传统理论认为,这种“入侵”是通过一个叫做上皮-间质转化(EMT)的过程实现的,即上皮细胞失去原有的特性,变得像间质细胞一样具有游走和侵袭能力。
然而,中山大学附属第六医院生殖医学中心陈培根、刘贵华、杨星团队,通过对患者病灶组织进行单细胞RNA测序,发现了完全不同的场景。他们首次在腺肌症病灶中明确鉴定出了一种全新的细胞转化过程——上皮-内皮细胞转化(EET)。
这意味着,这些“出逃”的子宫内膜上皮细胞,并没有变成间质细胞,而是直接朝着血管内皮细胞的方向“叛变”了。这些细胞同时表达上皮细胞标志物(如EPCAM)和内皮细胞标志物(如PECAM1/CD31),变成了兼具两者特性的“混合体”。轨迹分析显示,这些处于“中间态”的细胞高度表达MMP2和VEGFA,这意味着它们不仅能降解细胞外基质(为“入侵”开路),还能促进血管新生(为“定居”提供营养),简直是如虎添翼。
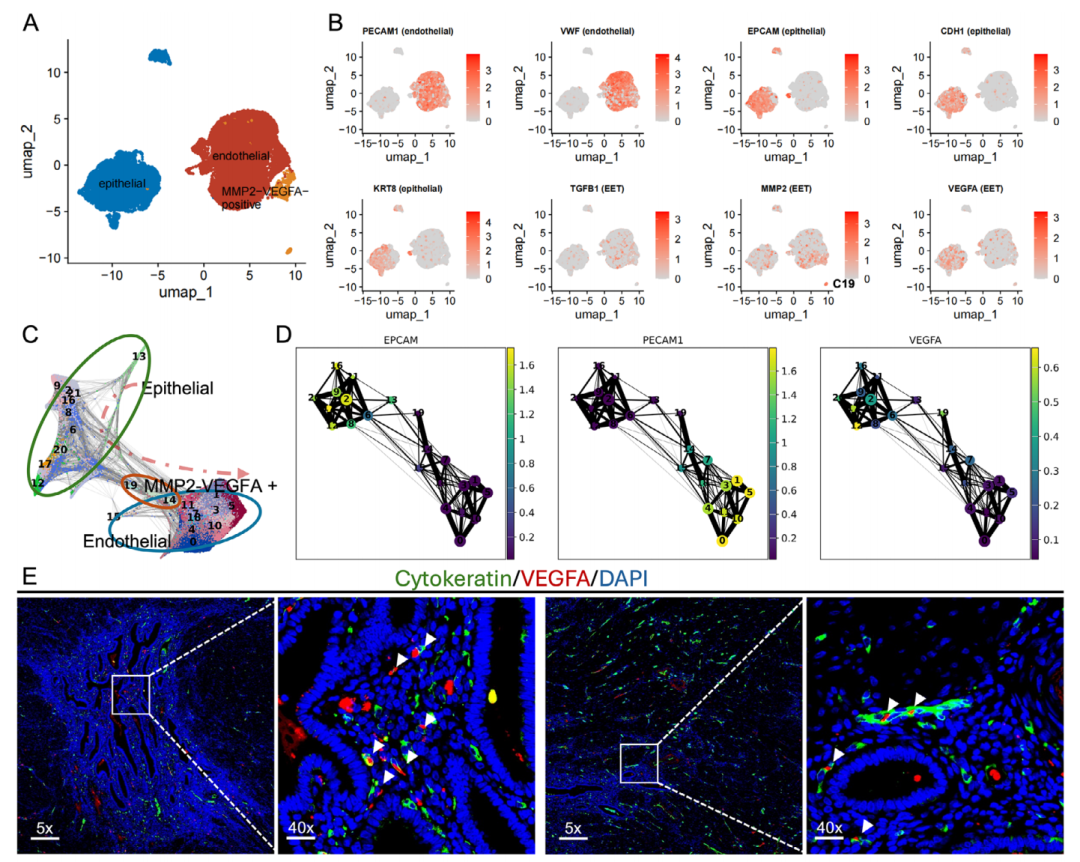
图1. 上皮-内皮细胞转化过程的轨迹分析与分子特征。
1.联合重聚类分析(图A):对上皮与内皮细胞进行UMAP可视化,揭示了二者之间存在过渡性细胞群体。
2.关键基因表达特征(图B):热图显示,MMP2在C19簇中高表达,而其他上皮(EPCAM、CDH1、KRT8)和内皮(PECAM1、VWF)标志物也在特定簇中呈现共表达模式,提示“杂交”表型的存在。
3.轨迹推断分析(图C):PAGA算法识别出位于上皮与内皮细胞状态之间的中间态细胞群体(C19和C14),表明EET是一个可追踪的连续过程。
4.基因动态表达(图D):沿轨迹分析发现,MMP2和VEGFA在中间态细胞中表达显著升高,赋予细胞基质重塑与促血管生成能力。
5.空间验证(图E):在子宫腺肌症患者全层子宫壁切片中,多重免疫荧光染色直接观测到共表达上皮与内皮标志物的细胞,确证了计算分析结果的真实性。
真凶浮现:一个名叫“少动鞘氨醇单胞菌”的“卧底”
那么,是什么驱动了这种奇特的EET呢?研究团队的目光投向了近年来的研究热点——微生物组。越来越多的证据表明,生殖道菌群失调与多种妇科疾病相关,腺肌症患者的宫颈和阴道菌群也确实存在异常。
研究人员利用先进的CSI-Microbes技术和FFEP样品的2bRAD-M®验证(欧易生物提供),在腺肌症病灶中进行了大规模的“微生物侦探”工作。结果令人震惊:他们发现了一种名为 “少动鞘氨醇单胞菌”的细菌在病灶中显著富集。更关键的是,通过荧光原位杂交技术,他们看到这些细菌在空间上直接与那些正在发生EET的“混合细胞”共定位——细菌就驻扎在病变的最前沿。
这一点,在健康对照组的子宫组织中并未发现。这强烈暗示,S. paucimobilis并非“路过”的游客,而是与病灶形成密切相关的“肇事者”。
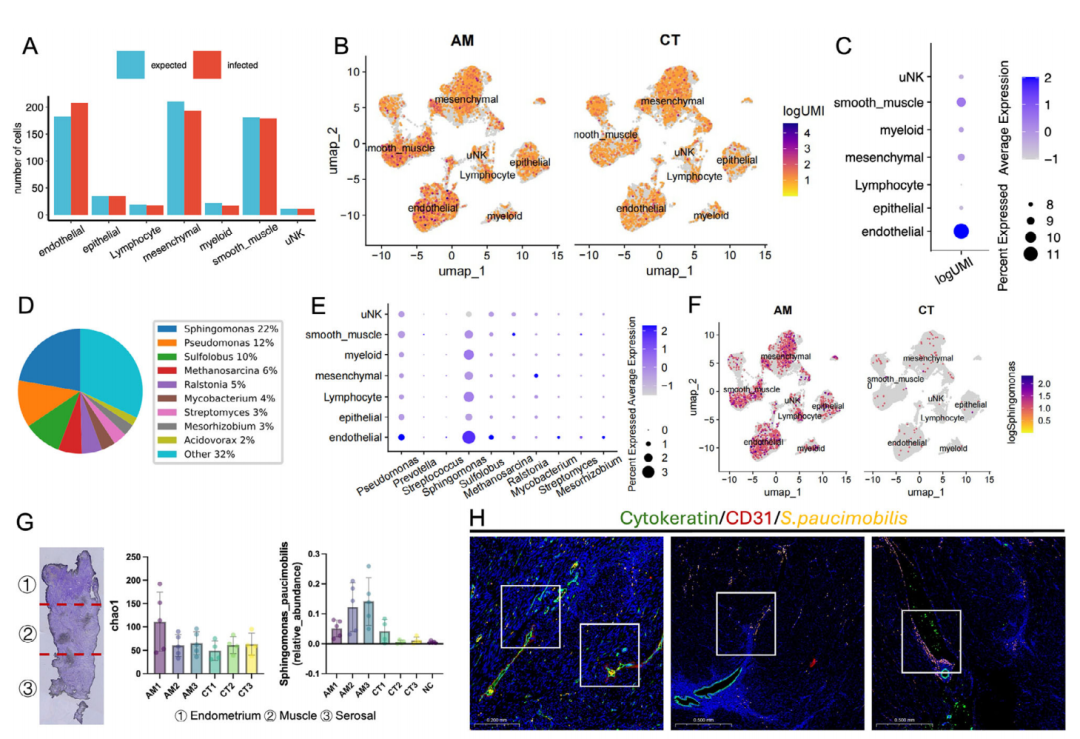
图2. 子宫腺肌症病灶中寡营养型少动鞘氨醇单胞菌的鉴定与定位。
1.微生物信号显著高于污染基线(图A–C):采用CSI-Microbes方法分析发现,在腺肌症组织的内皮细胞中检测到的细菌序列数量显著超过预期污染水平的基线,提示存在真实的微生物信号;同时在上皮细胞中也检测到一定量的细菌序列。
2.优势菌群鉴定与细胞定位(图D–E):细菌分类注释结果显示,鞘氨醇单胞菌属(Sphingomonas spp.)是主要的优势菌群,且主要集中定位于内皮细胞。
3.单细胞水平的菌群分布可视化(图F):UMAP分析显示,鞘氨醇单胞菌属的信号在AM组的所有细胞类型中广泛分布,而在对照组(CT)中几乎检测不到。
4.微生物多样性与特异性富集验证(图G):基于2bRAD-M®探针的检测表明,AM组患者的子宫内膜和浅肌层微生物Chao1多样性指数显著高于对照组,而浆膜层无显著差异;S. paucimobilis的信号在腺肌症子宫组织中明显富集,进一步证实其与病灶的密切关联。
5.细菌聚集于病灶前沿并与EET细胞共定位(图H):多重免疫荧光联合S. paucimobilis特异性FISH探针显示,细菌在腺肌症病灶的前沿区域聚集,其迁移轨迹与正在发生上皮-内皮转化(EET)的细胞直接共定位,提示其在驱动病理转化中的关键作用。
实锤证据:细菌直接导致小鼠患上腺肌症
关联不等于因果。为了证实是这种细菌“导致”了疾病,而非疾病“吸引”了细菌,研究团队进行了严谨的动物实验。
他们构建了小鼠模型,向小鼠阴道内接种活的少动鞘氨醇单胞菌。四周后,令人信服的结果出现了:这些小鼠的子宫内,真的形成了与人类腺肌症高度相似的病变,子宫内膜组织异常地侵入到了子宫肌层。
而作为对照,如果仅给小鼠接种经过滤除菌的细菌培养上清液(含有细菌分泌物但无活菌),则完全无法诱导出疾病。这雄辩地证明,活的细菌、其与宿主细胞的直接接触或定植,是致病的关键,单纯的细菌代谢产物并不足以引发这一过程。
在体外实验中,将这种活菌与人类子宫内膜上皮细胞共培养,研究人员直接观察到了EET的实时上演:上皮标志物减少,内皮标志物增多,细胞的迁移和侵袭能力显著增强。
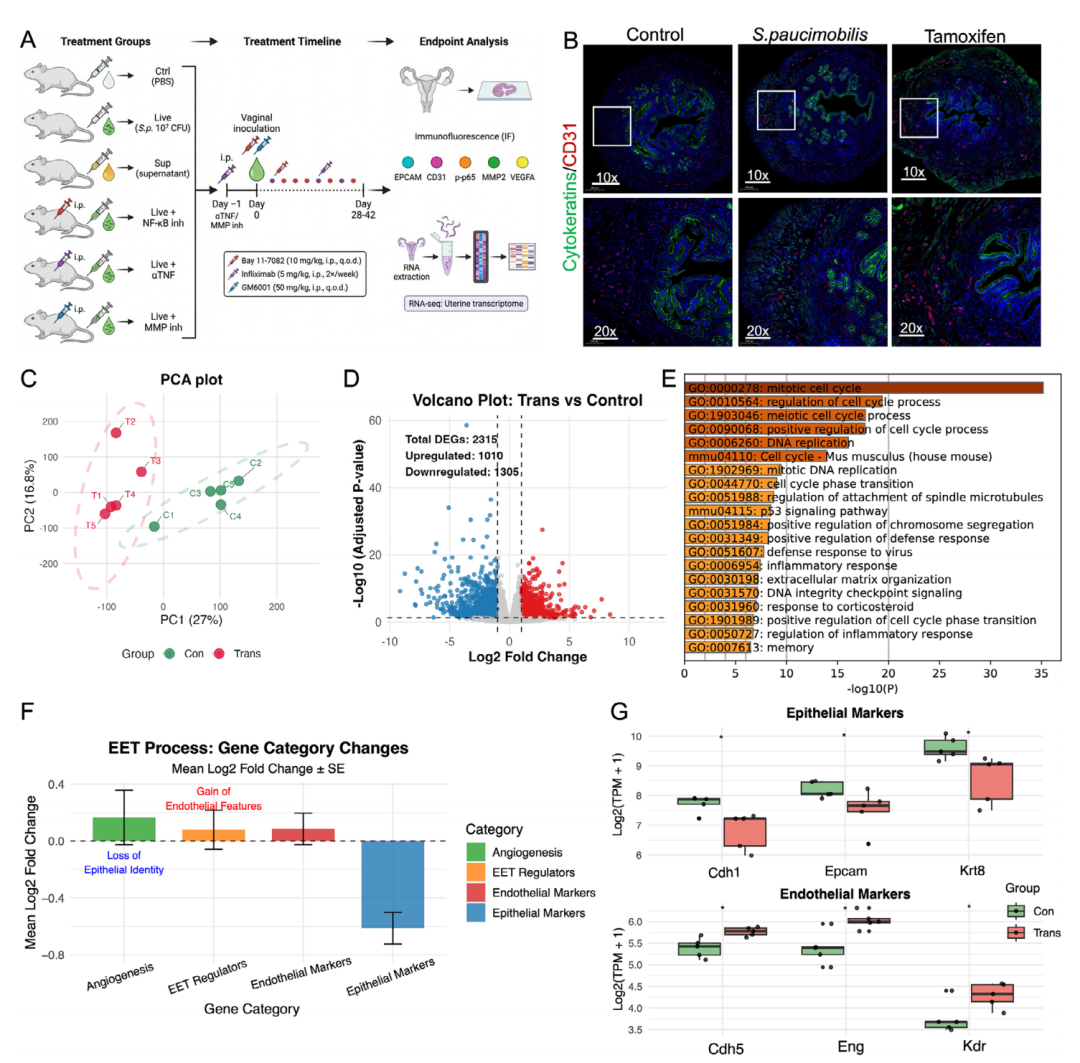
图3. 少动鞘氨醇单胞菌感染诱导的子宫腺肌症小鼠模型。
1.成功建立动物模型(图A–B):通过阴道接种活的S. paucimobilis,在成年CD1小鼠中成功诱导出子宫腺肌症。免疫荧光分析显示,模型小鼠出现子宫内膜腺体和间质向子宫肌层的深层浸润,其组织病理学特征与经典模型(如他莫西芬诱导)高度相似,验证了该菌的致病能力。
2.全基因组表达发生显著改变(图C–D):对感染后子宫组织进行转录组测序,主成分分析(PCA)显示基因表达谱发生显著分离;火山图鉴定出2315个差异表达基因(|log2FC|≥1,调整p<0.05),表明细菌感染引发了广泛的宿主反应。
3.细胞增殖活性增强(图E):功能富集分析显示,差异基因显著富集于细胞有丝分裂、DNA复制和细胞周期调控等通路,提示感染后子宫组织细胞增殖能力增强,为病灶扩张提供了基础。
4.EET及血管生成相关基因上调(图F):上皮-内皮转化(EET)调控、内皮细胞身份维持和血管生成相关基因表达显著上调,与人类病灶中发现的EET机制相呼应,表明该过程在动物模型中被成功复现。
5.上皮标志物表达下调(图G):关键上皮细胞标记基因(Epcam、Krt8、Krt9、Cdh1、Ocln)在S. paucimobilis组中显著下调(p<0.05,p<0.01,p<0.001 vs. 对照组**),进一步支持上皮细胞发生了去分化或表型转换。
锁定路径:一条清晰的致病“信号通路”
细菌是如何指挥细胞“叛变”的呢?研究团队像排查电路一样,系统性地解析了背后的分子机制。他们通过体内外一系列抑制剂实验,最终验证了一条清晰的信号通路:
少动鞘氨醇单胞菌 → 激活TNFα(肿瘤坏死因子α) → 激活NF-κB(一个核心的炎症转录因子) → 上调MMP(基质金属蛋白酶,尤其是MMP2)等效应分子
这条通路的每一个环节都被精准“敲除”验证:
阻断TNFα(使用英夫利西单抗)或抑制NF-κB,可以完全阻断整个通路的激活,防止EET发生。
而抑制MMP,则不影响上游NF-κB的激活,但能有效阻断下游的细胞迁移、侵袭等表型变化。
这条“TNFα–NF-κB–MMP”信号轴,正是连接细菌感染与细胞恶性转化的核心桥梁。它最终驱动了MMP2和VEGFA的表达,重塑了细胞外环境,赋予了细胞侵袭和血管生成能力,从而完成了腺肌症病灶的形成与扩张。
颠覆与希望:从“抗炎”到“抗菌”的治疗新思路
这项研究的意义重大,它为我们理解和管理子宫腺肌症带来了革命性的视角:
病因学突破:首次将一种特定的细菌感染与腺肌症的发病机制直接、因果地联系起来,提出了 “微生物驱动细胞转化” 的全新发病范式。
诊断新靶点:未来,我们或许可以通过检测子宫内膜或阴道分泌物中是否存在少动鞘氨醇单胞菌,或者检测EET相关的分子标志物(如共表达EPCAM/CD31的细胞),来更早、更精准地诊断甚至预测腺肌症风险。
治疗新策略:
抗菌疗法:既然细菌是“始作俑者”,那么针对性地使用抗生素消除这种细菌,是否可以从源头阻止或治疗疾病?这为开发新的抗菌治疗方案提供了理论基础。
抗炎/通路阻断:研究验证的通路中的关键节点,如TNFα(已有临床药物如英夫利西单抗)和NF-κB,都可能成为新的药物靶点,为那些对传统激素疗法不敏感或副反应大的患者提供了替代选择。
结语
这项来自中国团队的研究,像一道强光,照亮了子宫腺肌症病因中一个长期被忽视的角落。它不仅揭示了少动鞘氨醇单胞菌通过驱动上皮-内皮细胞转化(EET)致病的新机制,更为无数受此困扰的女性带来了新的希望——未来的治疗,可能不仅是“控制症状”,而是“祛除病因”。
从抗炎到抗菌,从缓解疼痛到逆转病理,我们对子宫腺肌症的认知和治疗,正在翻开全新的一页。科学探索的每一步,都向着最终战胜疾病的目标更近一步。
参考文献:Chen, P., Liu, G., Shi, H., He, J., Liu, Z., Zhu, Y., Liang, X., & Yang, X. (2026). Sphingomonas paucimobilis-Driven Epithelial–Endothelial Transition in Adenomyosis Pathogenesis. Advanced Science, 0:e16652. https://doi.org/10.1002/advs.202516652






