前 言
2026年1月17日,东南大学柴人杰教授团队联合多家研究单位在国际知名期刊Nature Communications上在线发表了题为“Molecular heterogeneity of the non-human primate cochlea”的研究论文。研究团队采用高分辨率单细胞测序技术,系统解析了非人灵长类(食蟹猴)耳蜗的细胞图谱,全面揭示了耳蜗内各类细胞的分子异质性特征,明确了不同细胞类群的特异性分子标记、功能通路与细胞间通讯网络。研究进一步阐明了耳蜗关键细胞类群(如毛细胞、支持细胞、免疫细胞等)的分子特征与功能分工,为理解灵长类听觉系统的结构与功能、构建更贴近人类的听觉研究模型提供了核心数据支撑。

发表期刊:Nature Communications
影响因子:15.7
涉及的欧易生物服务产品:单细胞核转录组测序
研究背景
听觉是生物体感知外界环境、进行交流的核心感官之一,而耳蜗作为听觉系统的核心外周器官,其复杂的细胞组成与精细的分子调控,是实现声音感知、信号转导的结构基础。解析耳蜗的细胞构成与分子特征,对于阐明听觉感知的生理机制、揭示听觉障碍疾病的发病机理、开发听力损伤的干预策略,都具有至关重要的科学意义与临床价值。
哺乳动物耳蜗呈现出高度有序的特化结构,包含毛细胞、支持细胞、螺旋神经节神经元、血管纹细胞等多种功能迥异的细胞类群,不同细胞类群的分子特征与功能分工,共同支撑了听觉处理的多样性与复杂性。非人灵长类在进化上与人类亲缘关系密切,其耳蜗的解剖结构、细胞组成与分子特征,相较于啮齿类等模式动物,更能模拟人类听觉系统的生理与病理状态,是研究人类听觉机制、开展听觉疾病转化研究的理想模型。
但截至目前,非人灵长类耳蜗的细胞异质性、分子图谱、细胞间互作机制仍未被充分探索,领域内缺乏系统、高分辨率的灵长类耳蜗单细胞分子图谱,这一空白极大限制了对灵长类听觉系统演化、人类听觉生理与疾病机制的精准理解,也阻碍了听觉障碍治疗策略的转化应用。
技术路线
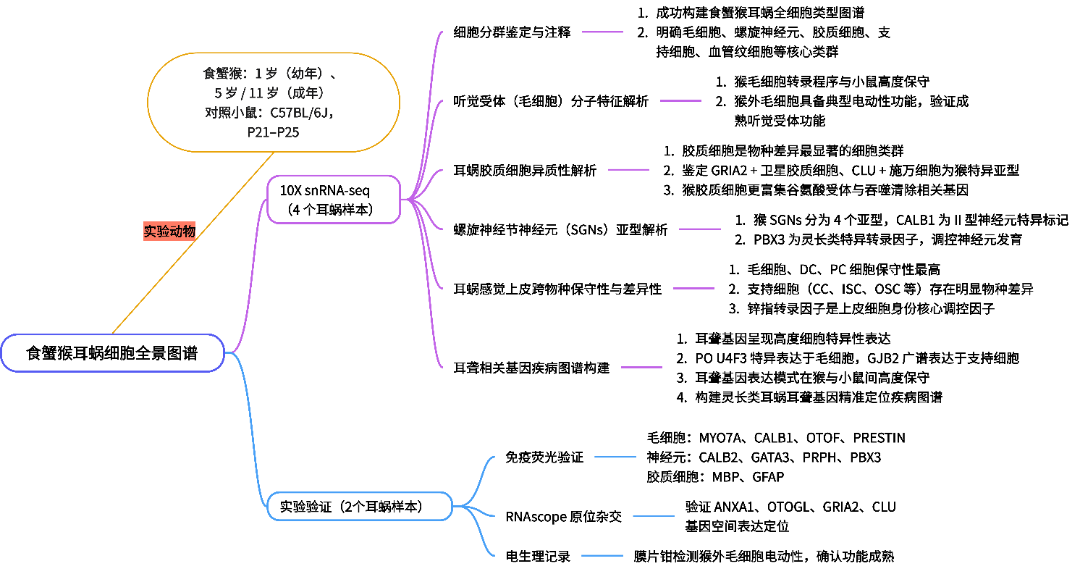
研究内容
本研究以1岁(幼年)、5岁及11岁(成年)食蟹猴为研究对象,采用10X Genomics单细胞核转录组测序技术开展分析,经质控后共获得36701个耳蜗细胞核数据,同时获取小鼠 P21-25耳蜗转录组数据作为跨物种对照;基于小鼠耳蜗已知标记基因完成食蟹猴耳蜗细胞的分群与注释,明确耳蜗主要细胞类群,并系统对比食蟹猴与小鼠耳蜗在毛细胞、胶质细胞、螺旋神经节神经元、耳蜗上皮等关键细胞类群的分子特征差异;进一步通过免疫荧光、RNAscope、膜片钳电生理实验,对关键基因的表达模式与细胞功能进行验证,最终将遗传性耳聋基因映射至食蟹猴耳蜗细胞图谱,明确其细胞特异性表达模式,全面解析非人灵长类耳蜗的分子异质性特征。
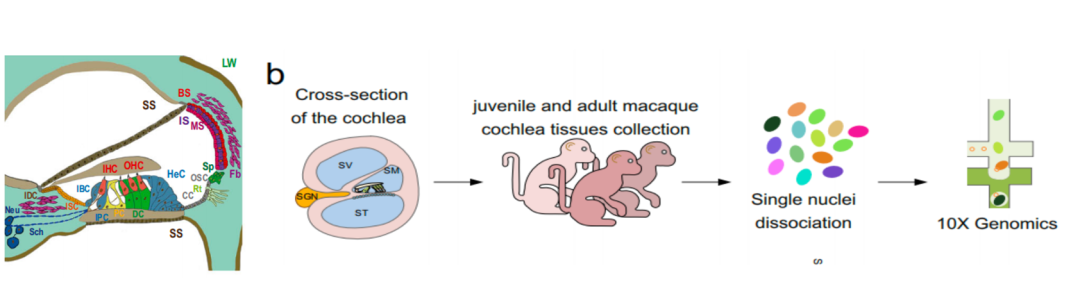
10x snRNA-seq 技术在食蟹猴中的实验操作流程
研究结果
一、 食蟹猴耳蜗细胞类型图谱构建
本研究通过对1岁、5岁及11岁食蟹猴耳蜗开展10x Genomics 单细胞核转录组测序,经严格质控后共获得36701个高质量细胞核数据,全面覆盖感觉上皮、螺旋神经节、血管纹、螺旋韧带等主要结构,并以小鼠耳蜗转录组为参照完成精准细胞注释,成功鉴定出20余种耳蜗细胞类型,归为五大核心细胞类群;利用支持向量机分类验证显示,食蟹猴与小鼠感觉器官细胞的转录谱特征高度对应,细胞分型结果可靠,同时通过免疫荧光与RNAscope实验证实CALB1、OTOF、CALB2、ANXA1、OTOGL等关键基因的细胞定位与测序结果高度一致,且GO功能富集分析表明各细胞类型的生物学功能在物种间高度保守,毛细胞、支持细胞、螺旋神经节神经元、施万细胞及边缘纹细胞分别行使声音感知、肌动蛋白调控、突触传递调节、髓鞘形成与细胞连接组装等核心功能,最终构建了覆盖幼年至成年阶段的食蟹猴耳蜗完整细胞分类图谱。
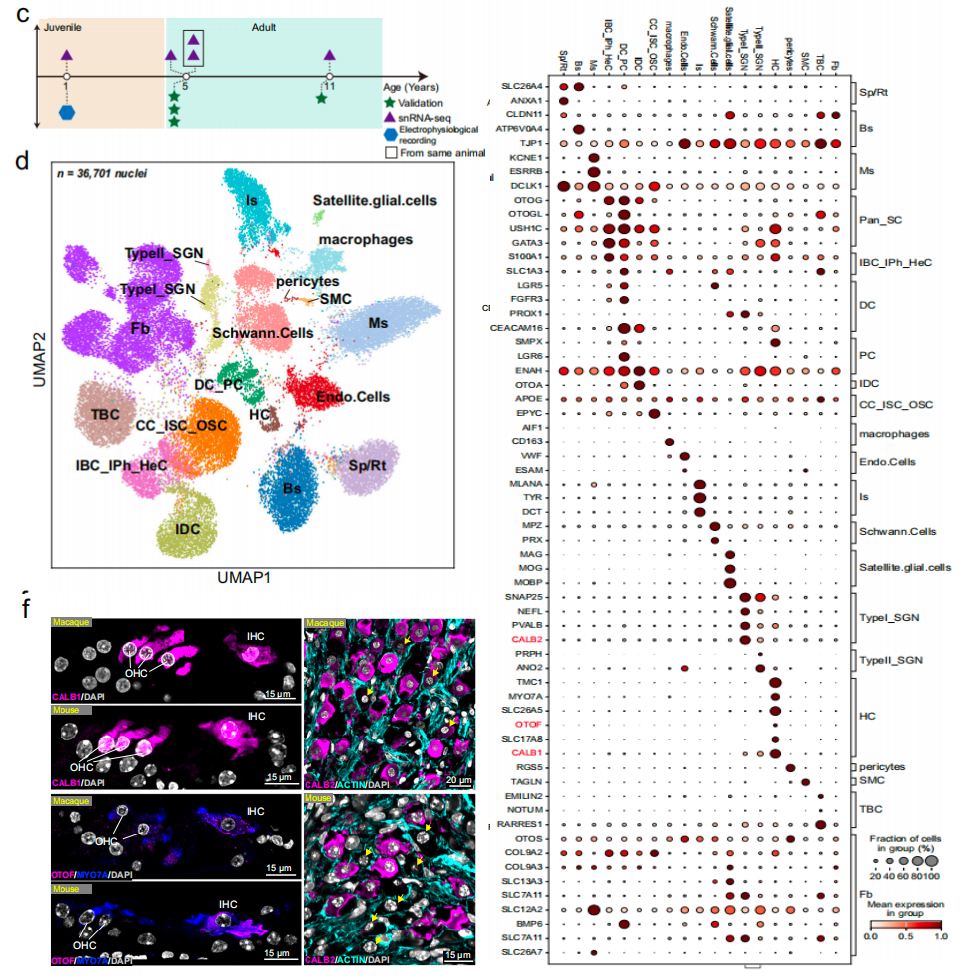
图1 食蟹猴耳蜗的单细胞转录组图谱
二、 食蟹猴耳蜗听觉受体(毛细胞)特征解析
研究从总细胞群中筛选出259个毛细胞并明确划分为内毛细胞与外毛细胞两大亚型,以MYO7A作为特异性标记基因,进一步对比分析发现,食蟹猴与小鼠毛细胞的转录特征高度保守,外毛细胞特异性表达 SLC26A5、KCNQ4、PCP4,内毛细胞特异性表达SLC17A8、CALB2、ATP2A3,调控内外毛细胞命运决定的核心转录因子IKZF2与TBX2在两个物种中均稳定高表达;免疫荧光结果显示运动蛋白PRESTIN 精准定位于外毛细胞基底外侧膜,膜片钳电生理记录进一步证实食蟹猴外毛细胞具备电刺激诱发的细胞运动功能,与小鼠完全一致,充分说明灵长类与啮齿类耳蜗毛细胞的分子调控机制与生理功能具有高度进化保守性。
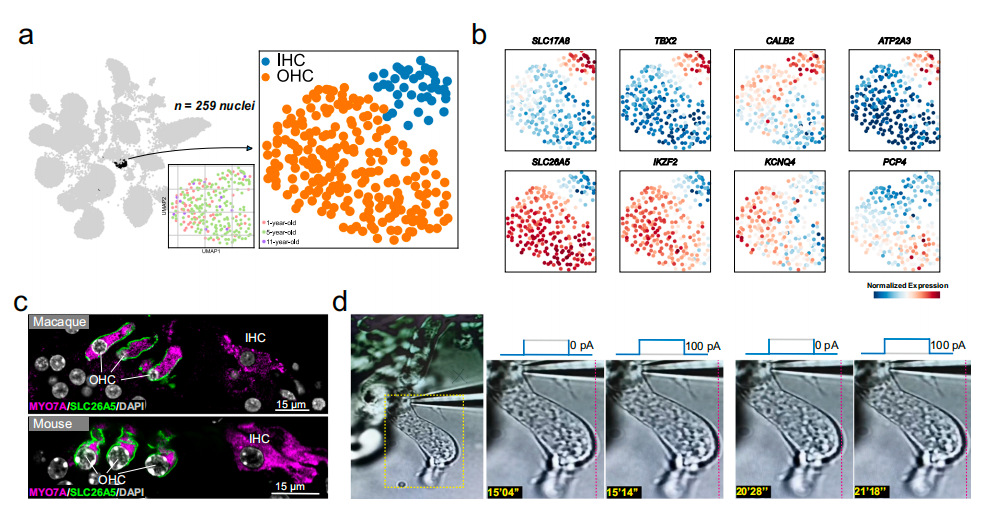
图2 食蟹猴耳蜗中听觉受体的特征
三、 食蟹猴耳蜗胶质细胞的多样性与物种特异性
研究对2800个胶质细胞进行重新聚类分析,将其划分为卫星胶质细胞、有髓施万细胞、无髓施万细胞三个亚型,形态学观察显示这些胶质细胞分别呈现包裹神经元胞体、包裹轴突形成髓鞘、构成雷马克束等典型特征,与小鼠胶质细胞结构相似;但关键差异在于小鼠胶质亚型经典标记基因SCN7A、NCAMP、IGFBP6 无法准确匹配食蟹猴胶质亚型,跨物种分类准确率低且细胞群存在明显交叉,提示二者胶质细胞在转录组水平存在显著趋异;进一步基因表达分析显示,小鼠胶质细胞高表达Na⁺-K⁺-ATPase通道相关基因,食蟹猴胶质细胞则高表达谷氨酸受体GRIA2、GRIK2,碎片清除相关基因CLU、LRP1在食蟹猴胶质中富集,而MEGF10、MERTK在小鼠胶质中高表达,最终依据GRIA2与CLU的表达将食蟹猴胶质细胞分为蜗轴区GRIA2阳性卫星胶质细胞,以及蜗轴外侧区CLU/GRIA2双阳性或CLU阳性施万细胞两类,空间分布与测序结果完全吻合。
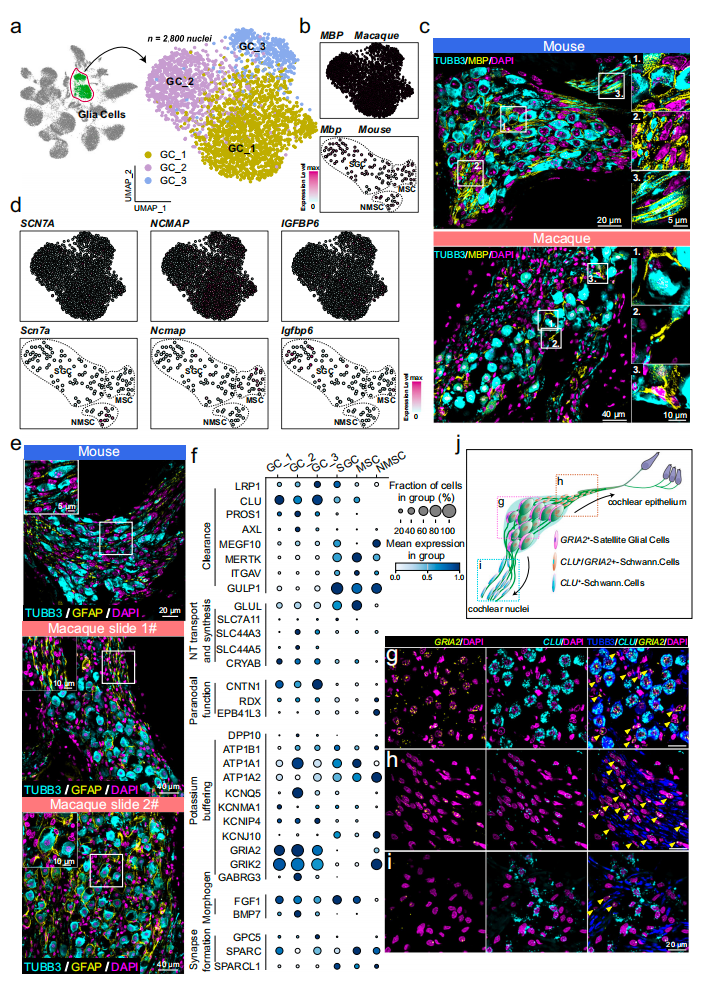
图3 灵长类听觉外周系统中神经胶质细胞的多样性
四、 食蟹猴螺旋神经节神经元的异质性
研究对955个螺旋神经节神经元进行分型分析,将其划分为I型与II型,并进一步细分为IA、IB、IC、II四个亚型,整体分型框架与小鼠保持一致,但存在明显物种特异性标记特征:小鼠II型神经元高表达TH,IC型神经元特异性表达POU4F1、LYPD1,而食蟹猴II型神经元特异性富集CALB1,并与GATA3、PRPH 共定位,成为灵长类II型螺旋神经节神经元的独有标记;差异表达基因分析鉴定出PROX1、RUNX1、SMAD1等在两个物种I型或II型神经元中均保守表达的转录因子,其中RUNX1对IC型神经元特化具有关键作用,同时发现PBX3为食蟹猴II型神经元特异性高表达的灵长类独有转录因子,GO分析显示其主要参与神经系统发育、神经元发生等生物学过程,免疫荧光实验进一步证实PBX3仅定位于食蟹猴螺旋神经节神经元细胞核,在小鼠中不表达,提示该因子可能介导灵长类听觉神经元的特异调控功能。
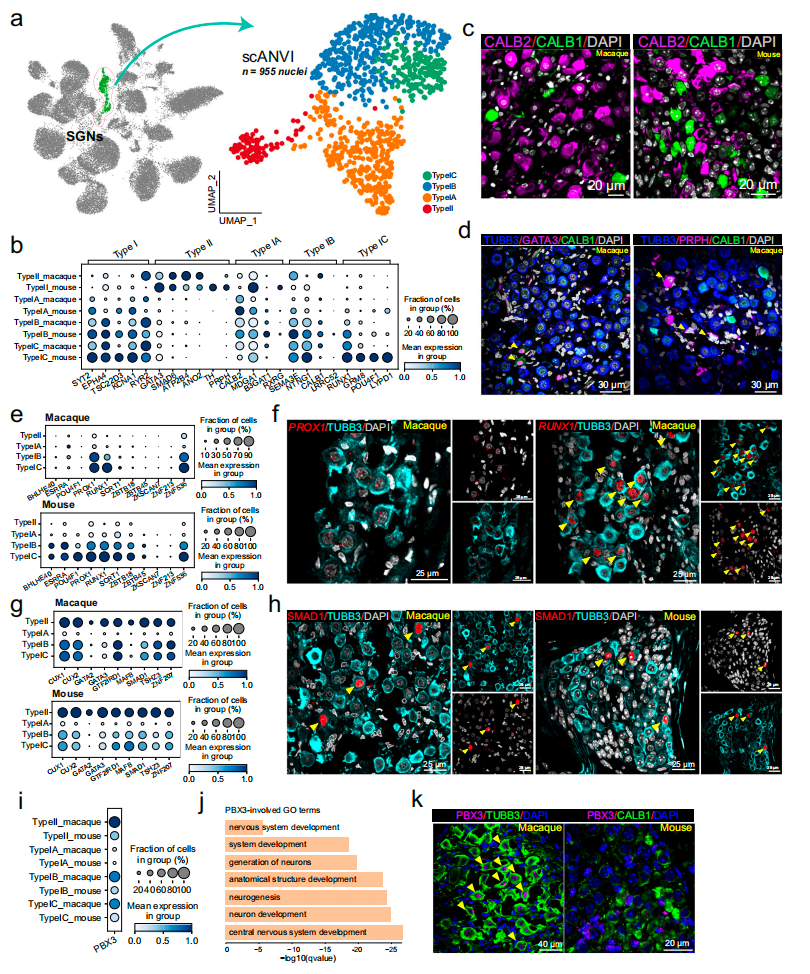
图4 食蟹猴神经节神经元的详细特征
五、 食蟹猴耳蜗上皮的保守性与差异性
研究采用scVI、CCA、Symphony多种标签转移算法,将食蟹猴10870个耳蜗上皮细胞映射至小鼠参考数据集,结果显示细胞类型锚定重叠度高,毛细胞、代特斯细胞、柱细胞、鼓膜边缘细胞的转录组相似度最高,表明耳蜗上皮整体具有高度进化保守性;但克劳迪乌斯细胞/内沟细胞/外沟细胞、内边界细胞/内指细胞/亨森细胞存在明显物种差异,这一差异可能与物种听觉频率适应相关,小鼠具备超声听觉能力,而食蟹猴听力范围更接近人类;基因家族分析显示,G蛋白偶联受体与锌指家族转录因子在耳蜗上皮中呈现严格的细胞类型特异性表达,锌指转录因子可作为两个物种耳蜗上皮细胞的身份标记,而跨物种分类测试表明,信号通路、离子通道、细胞黏附相关基因集在物种内分类效果优异,跨物种区分能力显著下降,说明进化保守性由核心转录因子组合维持,而物种特异性适应则由物种富集基因驱动。
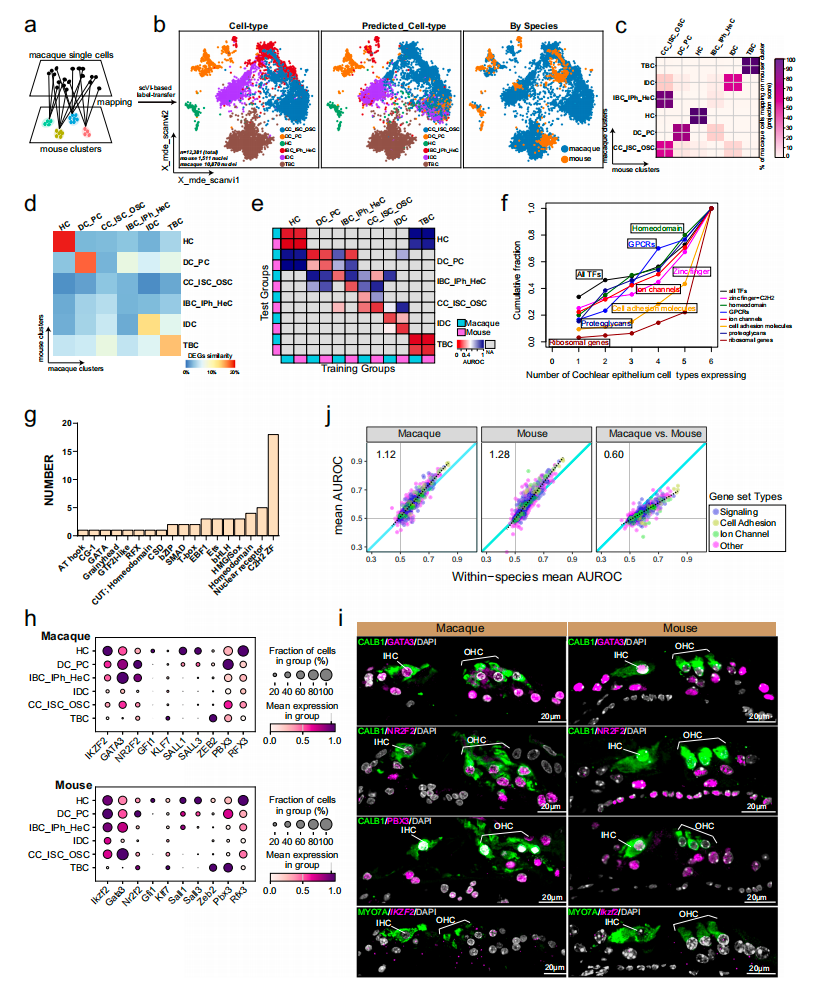
图5 对比分析揭示了食蟹猴和小鼠耳蜗上皮的保守特征和差异特征
六、 耳聋相关基因在食蟹猴耳蜗的定位图谱
研究系统整合常显非综合征型、常隐非综合征型、综合征型及X连锁非综合征型/年龄/噪声/顺铂相关四大类共209个遗传性耳聋基因,将其精准映射至食蟹猴耳蜗细胞图谱,结果显示绝大多数耳聋基因呈现严格的细胞类型特异性表达模式,其中POU4F3、MYO7A、USH1C等基因特异性富集于毛细胞,GJB2基因广泛表达于支持细胞与侧壁细胞,各类综合征型耳聋相关基因也均表现出特定细胞类型表达特征;更重要的是,这些耳聋基因的表达模式在1岁、5岁、11岁食蟹猴个体间高度稳定,且与小鼠表达谱高度保守,充分证明该图谱可作为人类耳聋致病机制解析、基因治疗靶点筛选及临床前疗效验证的核心参考资源。

图6 绘制食蟹猴耳蜗中与耳聋相关的基因图谱
研究结论
这项研究首次完整绘制了非人灵长类耳蜗的单细胞分子图谱,系统解析了食蟹猴耳蜗的分子异质性,不仅填补了灵长类耳蜗分子特征研究的空白,为理解听觉系统的进化与生理机制提供了核心数据支撑,更突破了啮齿类动物模型的局限性,搭建起连接基础研究与临床转化的关键桥梁。
未来,基于这一图谱,研究人员可进一步挖掘听觉感知、损伤修复的关键分子机制,筛选更精准的耳聋治疗靶点,推动遗传性耳聋、感音神经性耳聋等疾病的治疗研究,为改善人类听力健康、攻克听觉障碍难题提供重要助力。
参考文献
Chen X, Che Y, Qi J, Cen M, Gao S, Zhu B, Ao Y, Ma X, Cheng C, Guo R, Wang X, Shen T, Wu J, Kong F, Si W, Chen Y, Tan T, Lu L, Chai R. Molecular heterogeneity of the non-human primate cochlea. Nat Commun. 2026 Jan 17;17(1):1633. doi: 10.1038/s41467-026-68350-2. PMID: 41547823; PMCID: PMC12905143.






