前言
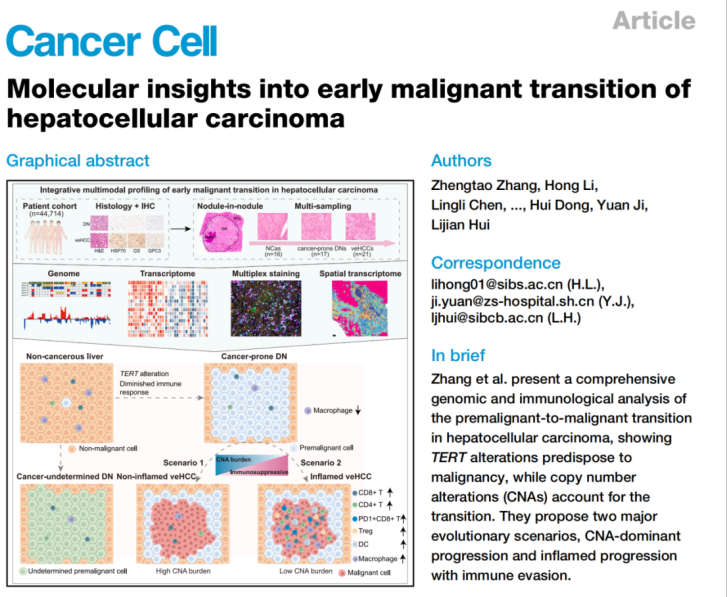
2026年3月26日,中国科学院分子细胞科学卓越创新中心(生物化学与细胞生物学研究所)惠利健团队联手中国科学院营养与健康研究所李虹团队、中山医院病理科纪元团队在Cancer Cell在线发表了题为“Molecular insights into early malignant transition of hepatocellular carcinoma”的研究论文。该研究利用空间转录组技术、全外显子测序(WES)、转录组测序、全基因组测序(WGS),首次系统解析了肝癌极早期恶性转变的分子驱动机制与免疫微环境演化规律。研究不仅明确了CNA累积而非SNV是驱动肝癌早期恶变的核心事件,鉴定出TERT异常为关键前置风险因素,更挑战了肝癌起源于炎症活跃微环境的传统认知,揭示了免疫静默-免疫逃逸的动态表型转换,并提出肝癌早期恶变的双演化路径,为肝癌的早期预警及早期免疫干预策略开发提供了全新的理论依据。欧易生物提供了空间转录组的测序服务。
发表期刊:Cancer Cell
影响因子:47.2
涉及的欧易生物服务产品:空间转录组测序
研究背景
癌前病变向早期癌症的转变是整个癌变进程里最关键的核心环节。既往研究多基于缺乏演化关联的癌前病变与肿瘤样本,通过统计推断分析恶性转变相关的遗传及微环境变化,然而,多数纳入的癌前病变缺乏实际癌变潜力,参考价值有限;此外,由于肿瘤微环境动态变化,对无关样本进行分析无法准确锁定恶性转化过程中微环境的真实变化规律。因此,采用具有明确演化关联的配对癌前与肿瘤样本,才能为解析恶性转变的机制提供确定性证据。其中,伴早期癌的“结节内结节”型不典型增生结节(Dysplastic nodule, DN)是理想的研究对象。这类病变能够精准定格恶性转变的关键节点,同时捕捉癌前与早期癌恶性特征,是界定驱动恶性转变的关键遗传变异及微环境改变的理想载体。然而,此类病变在临床样本中极为罕见,因为由于恶性细胞的高增殖率,DN和癌症共存的时间很短。为攻克人肝细胞癌(HCC)早期恶性转变的分子机制这一科研难题,本研究中,利用“结节内结节”病变这一独特视角来研究DN内极早期HCC(veHCC)的发展,开展了系统性的基因组与免疫图谱全景分析。
研究内容
本研究通过全外显子测序(WES)、转录组测序、全基因组测序(WGS)在CNA和SNV水平上的肝癌恶变的驱动因素,鉴定出TERT异常为关键前置风险因素。结合样本表达谱、空间转录组与原位多色染色分析,进一步揭示了肝癌早期恶性转变区域的免疫静默表型特征。发生恶性转变后,43%的veHCC形成“炎症型伴免疫逃逸”表型,免疫与基质细胞浸润显著增多,同时启动多重免疫抑制程序;而剩余veHCC则维持免疫静默的非炎症表型,且这类非炎症型veHCC的CNA负荷显著高于炎症型veHCC。基于上述基因组与免疫图谱数据,研究团队提出肝癌早期恶性转变的“双演化路径”:一是CNA主导型进展(高CNA负荷、低免疫浸润),二是伴早期免疫逃逸的炎症型进展(低CNA负荷、高免疫浸润伴免疫抑制),为肝癌的早期预警及早期免疫干预策略开发提供了全新的理论依据。
技术路线
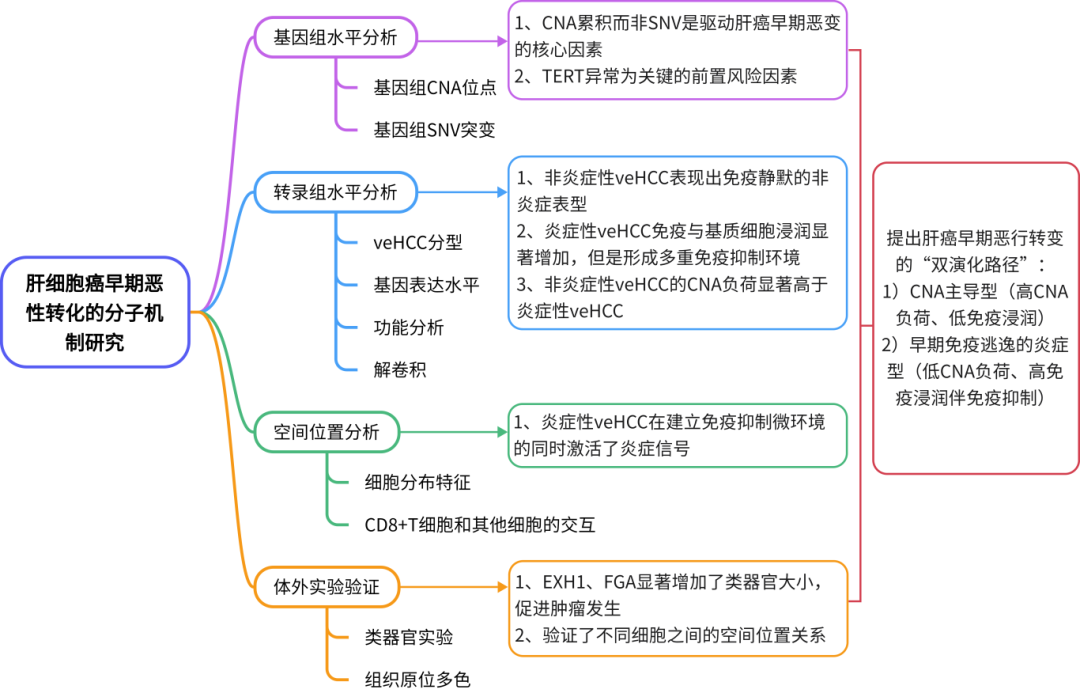
研究结果
一、 HBV感染患者Cancer-prone DN区域的基因突变特征
在44,714份人肝脏FFPE标本中,找到了16名HBV感染患者的标本符合同时包含高级别DN和veHCC的需求,包含17个“结界内结界”区域、21个veHCC区域(图1A)。全基因组测序测序结果显示,17个DN(Cancer-prone DN)与配对的veHCC共享7-85%的单核苷酸变异(SNV)(图1C)。结果显示,配对的DN和veHCC表现出相似的突变特征模式。
取另外19名HBV感染患者无癌病变的DN(Cancer-undetermined DN)及其配对的非癌组织(NCA)作为对照,结合8个已发表HCC队列公布的37个肝癌功能基因(CFG)列表,分析Cancer-prone DN中的关键突变。在82%的Cancer-prone DN中检测到TERT变异(图1D),突变频率显著高于Cancer-undetermined DN组别的 32%(p = 0.003),说明TERT突变在Cancer-prone DN中富集,进一步分析发现,TERT突变上调了Cancer-prone DN及其配对veHCC中TERT 的表达水平(图1E);在携带TERT突变的Cancer-prone DN中,79%的样本观察到端粒显著缩短,在65%的veHCC中,端粒长度得以维持甚至缩短(图1F)。这些数据表明,即使在存在TERT突变的情况下,端粒磨损在恶性转化过程中持续存在。同时,发现Cancer-prone DN中的CNA显著增加(图1G,p = 0.002)。
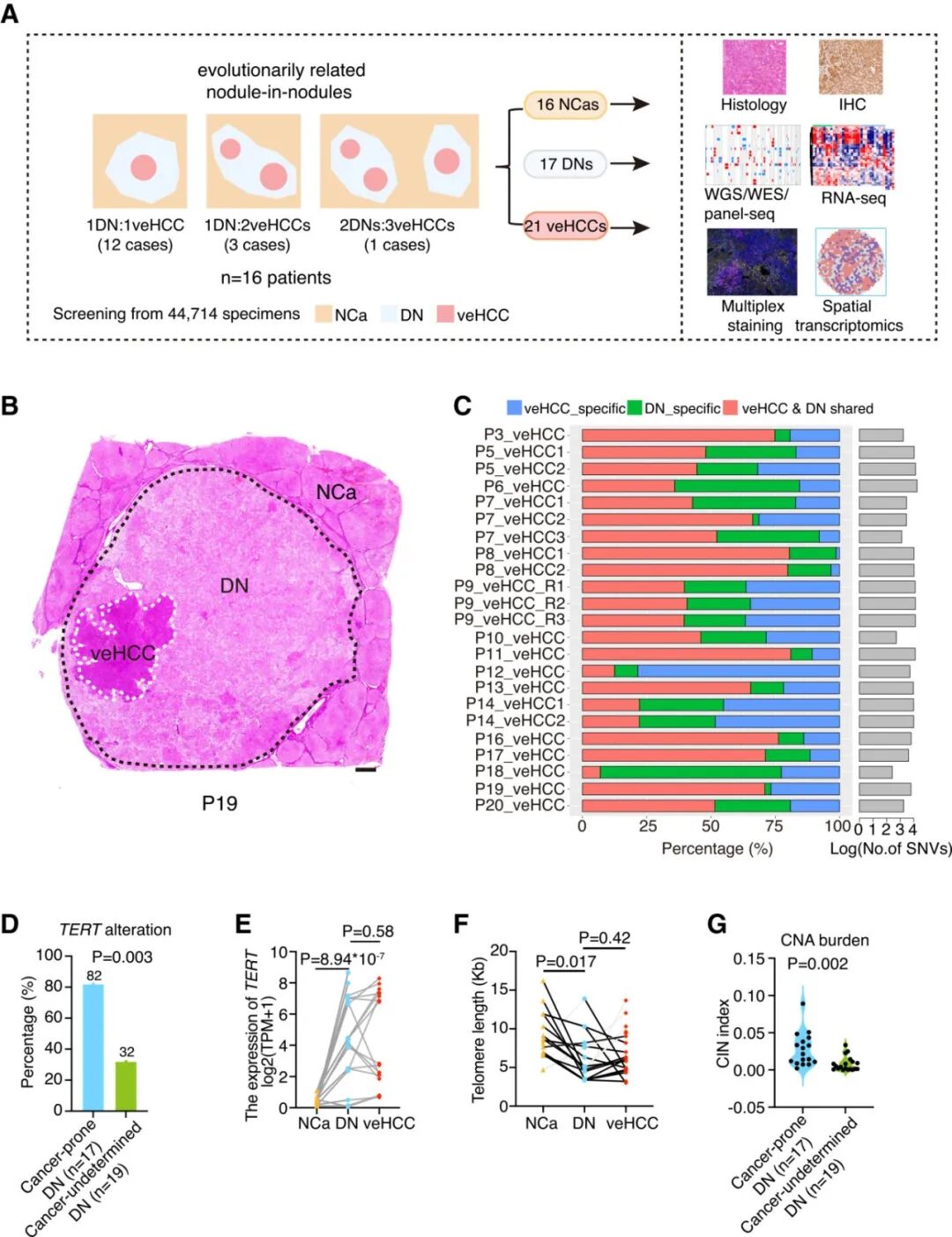
图一DN和veHCC的基因组特征
二、veHCC恶性转化的驱动因素
通过比较Cancer-porne DN区域和配对veHCC之间总SNV数量、CFG突变数量以及导致蛋白质改变性SNV数量差异,没有发现显著差异(图3A,2C-D),表明从DN到veHCC的转变与SNV负担无关。与SNV相反,veHCC与配对DN相比表现出显著更高的CNA水平(图3B),89%的arm-level CNA在veHCC中频率增加,例如ECHS1和TP53的局部缺失以及ARID1A
和MYC的扩增(图3C)。veHCC中存在10个独特性的CFG,包括TSC1、RB1缺失和KRAS扩增(图3D)。与中国肝癌图谱(CLCA)和癌症基因组图谱数据集(TCGA)中的晚期HCC进行比较,veHCC中富集的arm-level CNA在晚期HCC中也很常见。
比较veHCC独特性的CFG,发现,Chr1p(15-28 Mb)缺失在19%的veHCC中检测到,而在DN中不存在(图3D),表明在恶性转化过程中Chr1p局部缺失,缺失区域包含两个肿瘤抑制基因(TSG),ARID1A和NR0B2,两者在veHCC中的表达均降低(图2J)。将分析扩展到803个泛癌癌基因和1,218个泛癌TSG。与配对DN相比,veHCC区域拥有更多的致癌基因插入以及TSG缺失 (图2K)。基因富集分析显示veHCC表现出染色体不稳定性相关基因的富集表达(图2L)以及升高的DNA修复和染色体断裂特征(图2M-2P)。TP53 变异在具有高染色体不稳定性(CIN)的veHCC中显著富集,而在低CIN的veHCC中则不显著(图2Q)。这些发现进一步强调了CNA在恶性转化过程中的重要性。
通过对恶性转化过程中37个CFG与SNV、CNA和HBV插入的整合分析。结果显示,在cancer-prone DN和匹配的veHCC中,总共有33个CFG发生突变(图3E),其中,22个在DN和veHCC中均发生突变,有 11 个 CFG 的改变仅在 veHCC 中检测到(图3F)。在 veHCC 中,由 CNA 导致的 CFG 改变数量显著高于由 SNV 导致的 CFG 改变数量(见图 2R)。这些发现进一步表明,虽然 CFG 突变对恶性转化有促进作用,但 CNAs导致的CFG突变是恶性转化过程中的一个主要事件。(图 3F)。
为了评估候选基因在早期肝脏肿瘤发生中的功能作用,利用了基于人诱导肝细胞(hiHep)的类器官培养系统对候选的潜在驱动基因进行筛选。结果显示,ECHS1以及FGA基因敲除,显著增加了类器官的大小(图3I-3K)和EdU阳性细胞的百分比。总之,这些结果为ECHS1和FGA变异与肝脏肿瘤发生早期恶性转化的联系提供了实验证据。
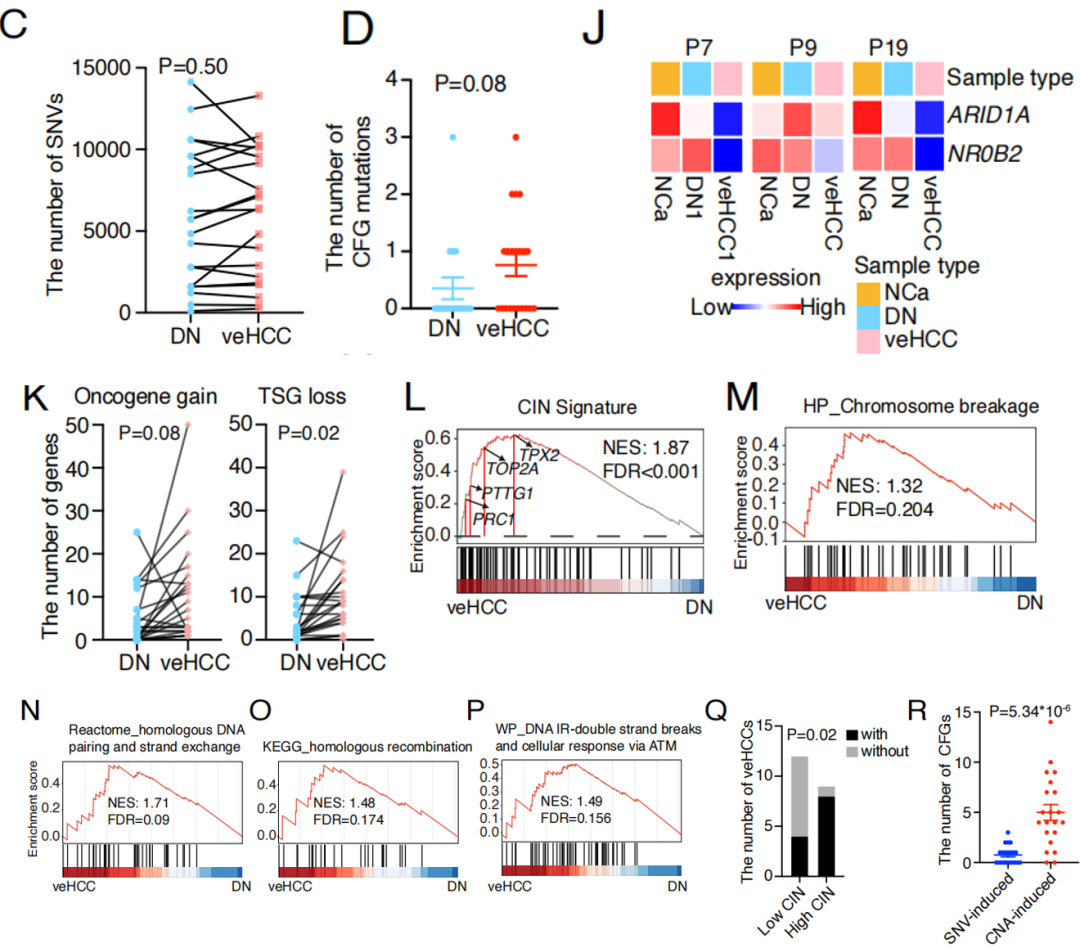
图2 veHCC恶性转化的驱动因素
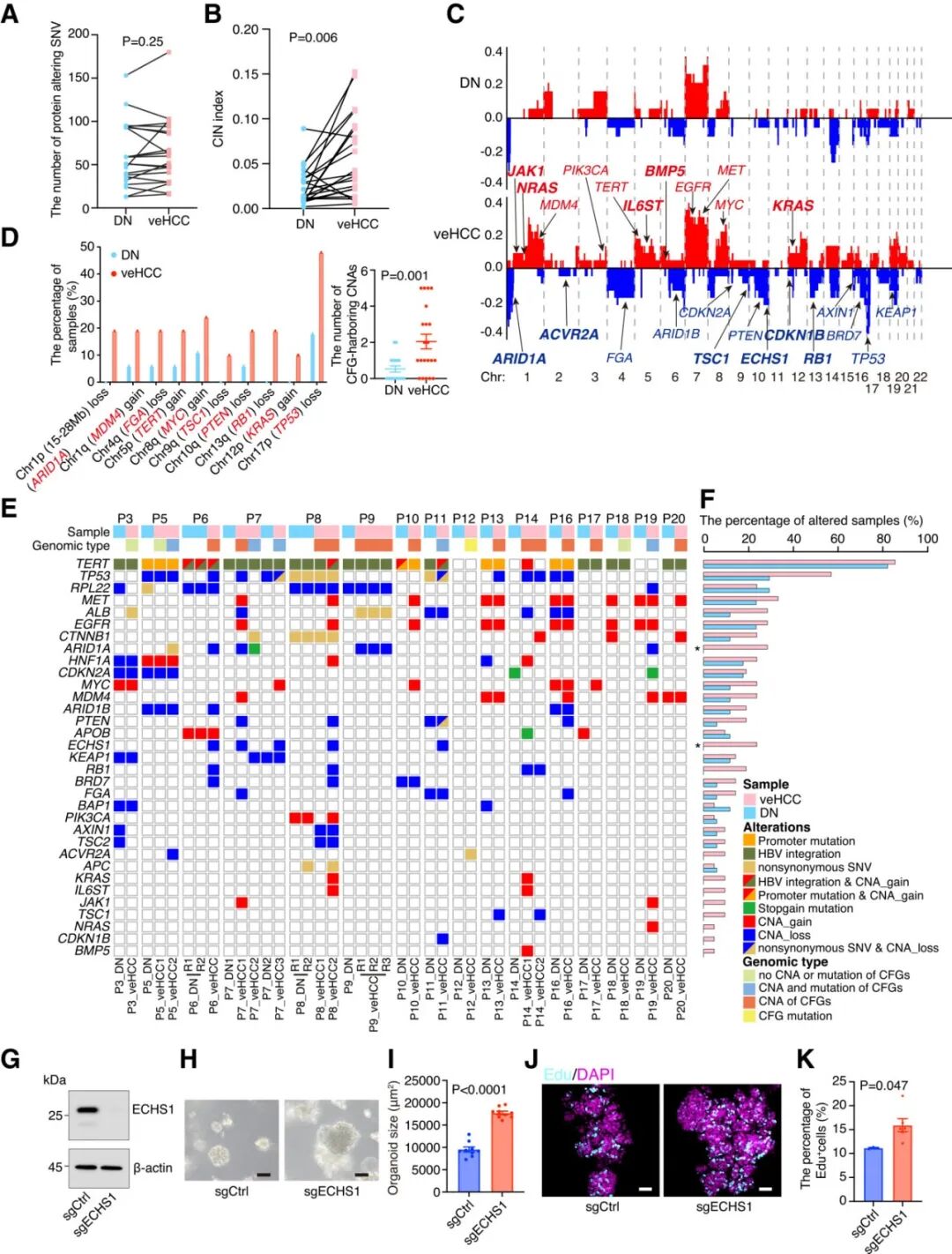
图3 veHCC恶性转化核心基因组学特征
三、 癌前DN的免疫沙漠表型
对转录组进行分析,PCA结果显示,尽管Cancer-prone DN在基因组变异上表现出显著的个体特异性,但这些DN的表达谱彼此紧密聚集在一起,Cancer-prone DN管积累了遗传变异,尚未发展出癌性表型,veHCC的表达谱彼此分散,并表现出增加的表达异质性(图4A)。
对NCA、Cancer-prone DN和veHCC的差异基因(DEG)分析,揭示了veHCC发展中的三个主要模块。第一个模块与增殖相关通路相关,在肿瘤发生过程中表达增加(图5D);第二个模块在肿瘤发生过程中表达逐渐下降,并富集于肝脏代谢通路,包括天冬氨酸、天冬酰胺代谢、括脂肪酸、肝脏维生素等代谢通路,表明在恶性转化过程中发生了部分去分化和重编程(图5G-5H);第三个模块呈现出先下调后上调的表达模式,并富集于与上皮-间充质转化(EMT)、血管生成和免疫相关通路相关的通路(图5D),表明恶性转化过程中微环境的动态变化。
研究表明,肝癌经常在炎症微环境中发展。然而,炎症相关基因的表达表明,促肿瘤的炎症信号在Cancer-prone DN中减少,包括TNFα/NF-κB、IL6/JAK/STAT3和NLRP3炎症小体信号通路(图4B)。具体来说,与NCA相比,Cancer-prone DN中与小鼠HCC发展相关的炎症因子基因表达水平降低,这些基因编码促炎性I型干扰素、细胞因子和Toll样受体(图4C)。此外,Cancer-prone DN显示与炎症相关纤维化和血管生成相关的基因下调(图4C)。
通过使用MCP-counter对表达数据进行解卷积,估计了不同微环境细胞类型的丰度。NCA表现出成纤维细胞、内皮细胞和单核细胞系的高丰度评分,与这些样本的肝硬化和慢性炎症状态一致。然而,在Cancer-prone DN中,所有这些细胞类型的丰度评分均显著降低(图4D)。对巨噬细胞标志物CD163的多重染色进一步证实了Cancer-proneDN中巨噬细胞的显著减少(图4E和4F)。此外,通过CD4和CD8免疫染色确定,Cancer-prone DN中的T细胞浸润也较低(图4G和4H)。对从NCA到晚期HCC微环境细胞丰度动态变化的分析显示,与其他组相比,Cancer-prone DN的成纤维细胞、内皮细胞、单核细胞系和T细胞的丰度评分显著降低(图5J)。这些数据表明Cancer-prone DN 表现出免疫沙漠表型,提示HCC起源于免疫非活动性而非免疫活动性的微环境。
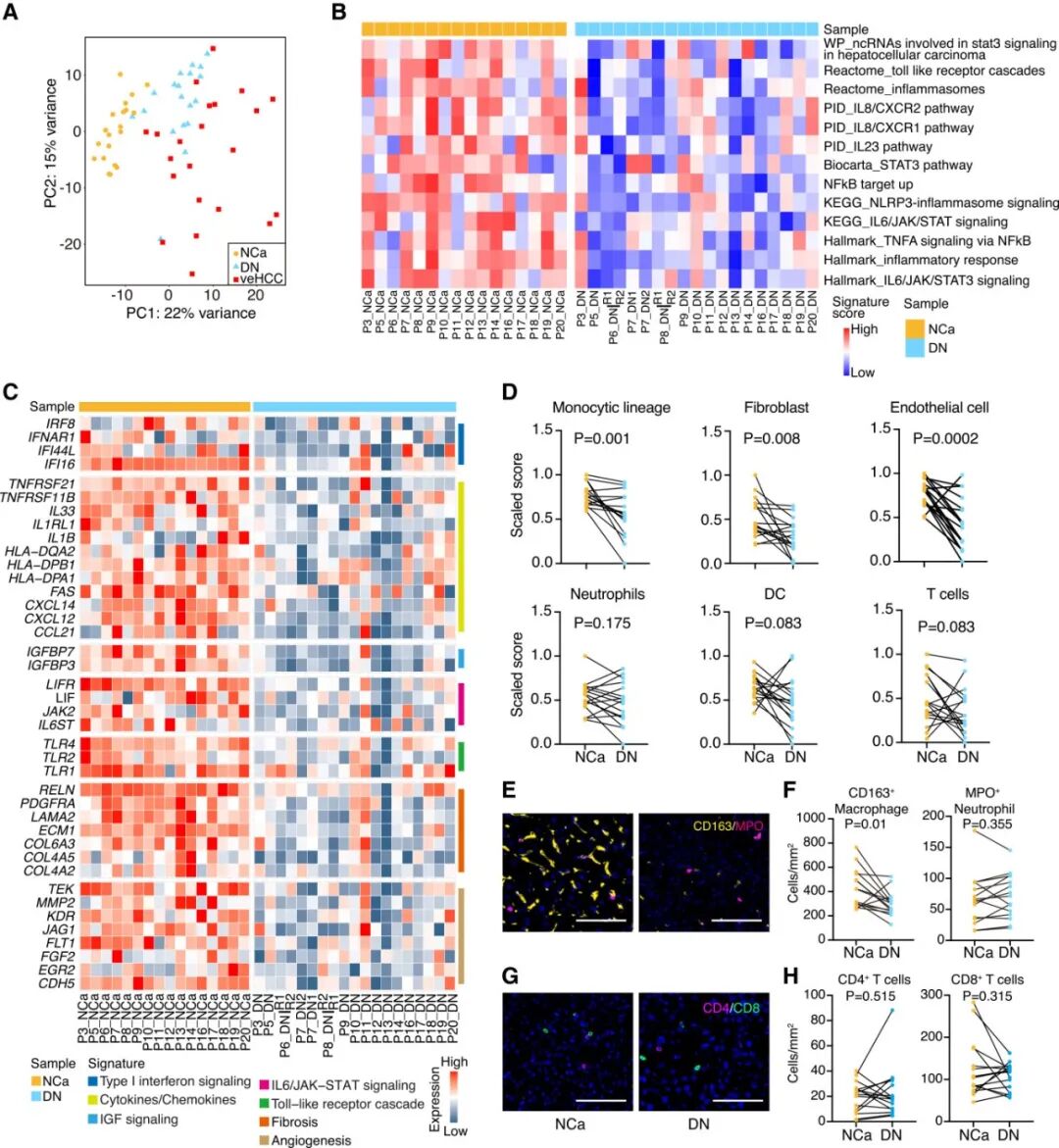
图4 癌前DN的免疫沙漠表型
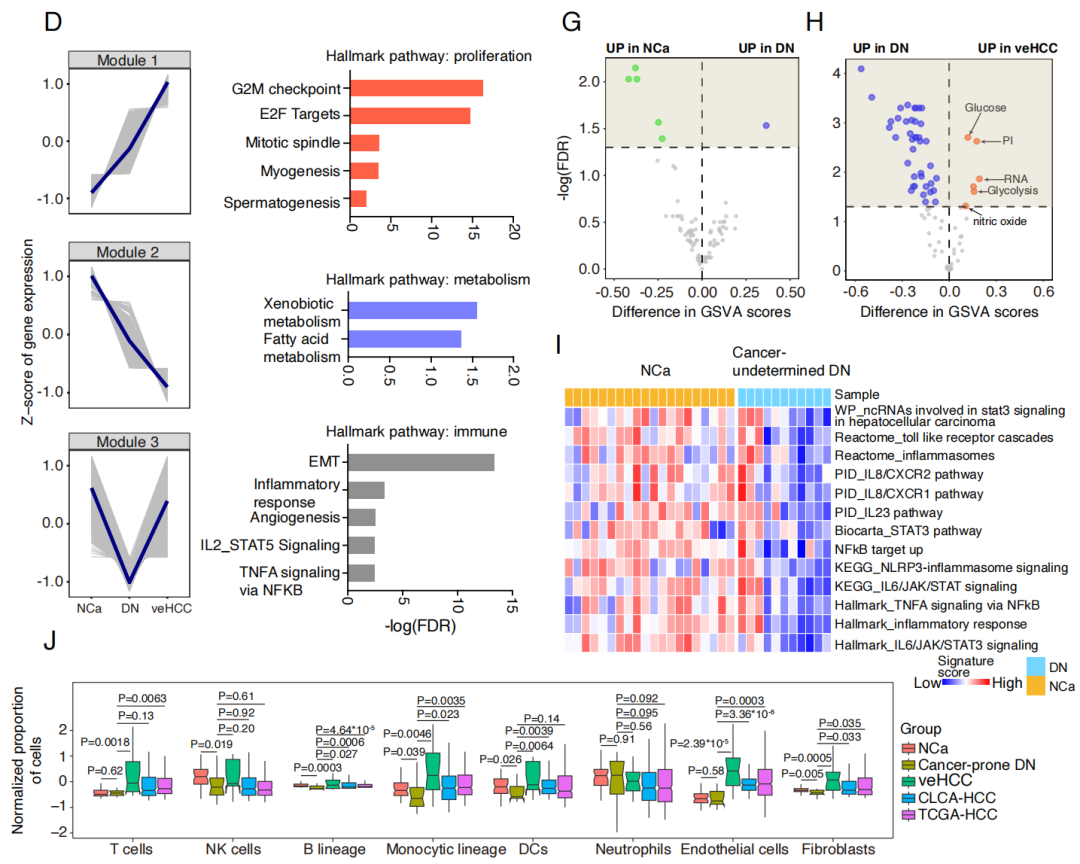
图5 veHCC早期恶变信号特征
四、 炎症性veHCC的免疫逃逸表型
通过免疫细胞丰度以及炎症特征激活评分,veHCC被分为了炎症性和非炎症性。炎症性veHCC表现出高丰度的T细胞和DC细胞以及高炎症特征(图6A-B),与非炎症性相比,炎症性表现出更低的CNA负担(图6C)。与非炎症性veHCC相比,炎症性veHCC展现出CD4和CD8 T细胞浸润水平提高(图6D-F)。以及与其配对DN相比,对CD4、CD8和CD11c的多重染色证实了CD4+ T细胞、CD8+ T细胞和DC向炎症性veHCC的浸润增加(图6G-6J)。有趣的是,参与胆汁酸途径的基因在炎症性veHCC中下调(图7I)。胆汁酸已被证明在小鼠肝癌模型中阻碍T细胞反应,进一步研究该途径的下调是否有助于炎症性免疫表型的发展将是有价值的。
与配对的DN相比,炎症性veHCC与T细胞反应负调控以及抗原加工和呈递相关的通路已经上调(图6K),显示出显著更高的免疫抑制相关特征评分,包括包括耗竭T细胞特征、免疫检查点特征和调节性T细胞(Treg)特征(图6 L-N)。免疫共抑制分子(如CTLA4、PDL1 和PD1)、共刺激分子(如CD80、CD86和ICOS)和抑制性细胞因子(如IL10和TGFB1)在这些炎症性veHCC中上调。免疫染色显示,PD1+CD8+ T细胞、PDL1+细胞、FOXP3+CD4+ T细胞和CD163+巨噬细胞的浸润在炎症性veHCC中增加(图6P-6S)。这些发现表明,炎症性veHCC在早期恶性转化过程中获得了免疫逃逸特征,其特征是强烈的适应性免疫激活与免疫抑制程序的早期建立相结合。
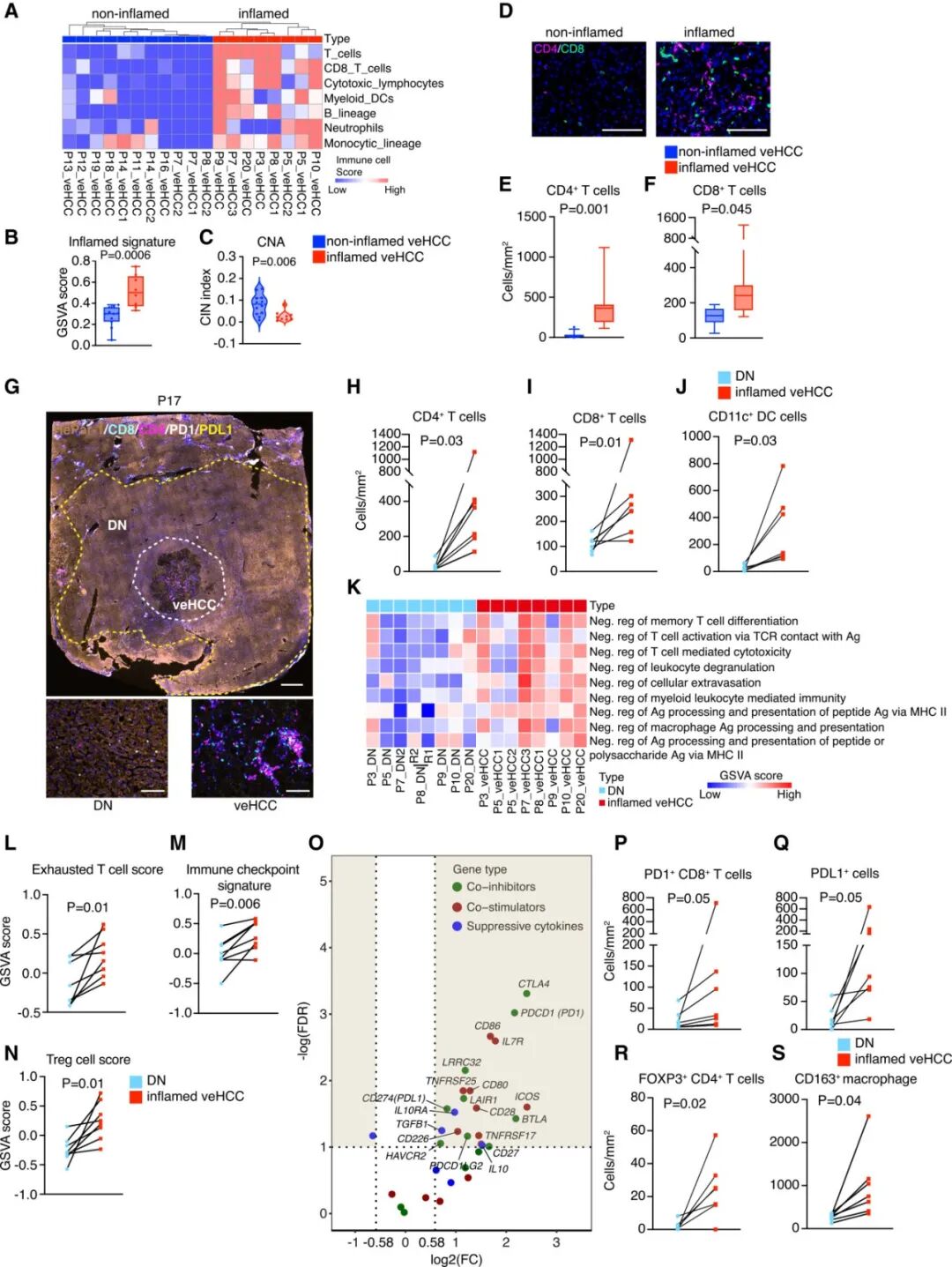
图6 veHCC分型以及炎症性veHCC免疫逃逸表型
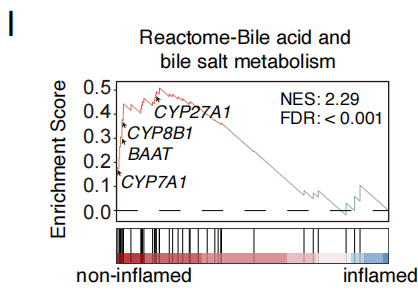
图7 炎症性veHCC的免疫逃逸表型
五、 炎症性veHCC中免疫表型的空间定位
使用Visium HD空间转录组测序方法,对3个炎症性veHCC和1个非炎症性veHCC及其配对的DN进行了分析(图8A)。通过单细胞数据对空转数据进行解卷积,鉴定出9种主要细胞类型(图8B),并通过典型标志物表达进行了验证。与配对的DN相比,炎症性veHCC显示出CD4+和CD8+ T细胞、巨噬细胞和B细胞的丰度增加(图8C)。CAF在2个炎症性veHCC(P7_veHCC3和P20_veHCC)中显著增加(图8C)。相比之下,非炎症性veHCC及其配对的DN表现出持续的低免疫和基质细胞浸润(图8C)。
空间通讯分析结果显示,CD8+ T细胞与多种细胞类型(包括CD4+ T细胞、CAF和巨噬细胞)发生广泛相互作用(图8D-8F)。在3个炎症性veHCC中,CD4+ T细胞与CD8+ T细胞表现出最多的配体-受体相互作用(图8D-8F)。在空间上,CD4+和CD8+ T细胞紧密相邻并形成不同的细胞簇(图8G、8H)。对Treg细胞和耗竭T细胞特征评分的分析表明,这些细胞在CD4+和CD8+ T细胞聚集的区域显著激活(图8I-8L)。
在2个具有高CAF丰度的炎症性veHCC中,CAF在与CD8+ T细胞相互作用的细胞类型中排名靠前(图8D-8F)。一致地,CD8+ T细胞在空间上靠近CAF(图8M和8N)。富含CAF和CD8+ T细胞的区域显示出肌成纤维细胞CAF(myoCAF)和TGF-β特征的强烈激活(图8O-8R)。这些发现与RNA-seq结果一致,并支持TGF-β介导的免疫抑制的作用。鉴于先前有证据表明TAM参与T细胞抑制,我们特别表征了炎症性veHCC中的TAM。在CD8+ T细胞和巨噬细胞之间检测到相互作用(图8D-8F),与多重染色数据一致,该数据显示炎症性veHCC中浸润的TAM显著增加。这些数据表明,炎症性veHCC在建立免疫抑制微环境的同时激活了炎症信号。
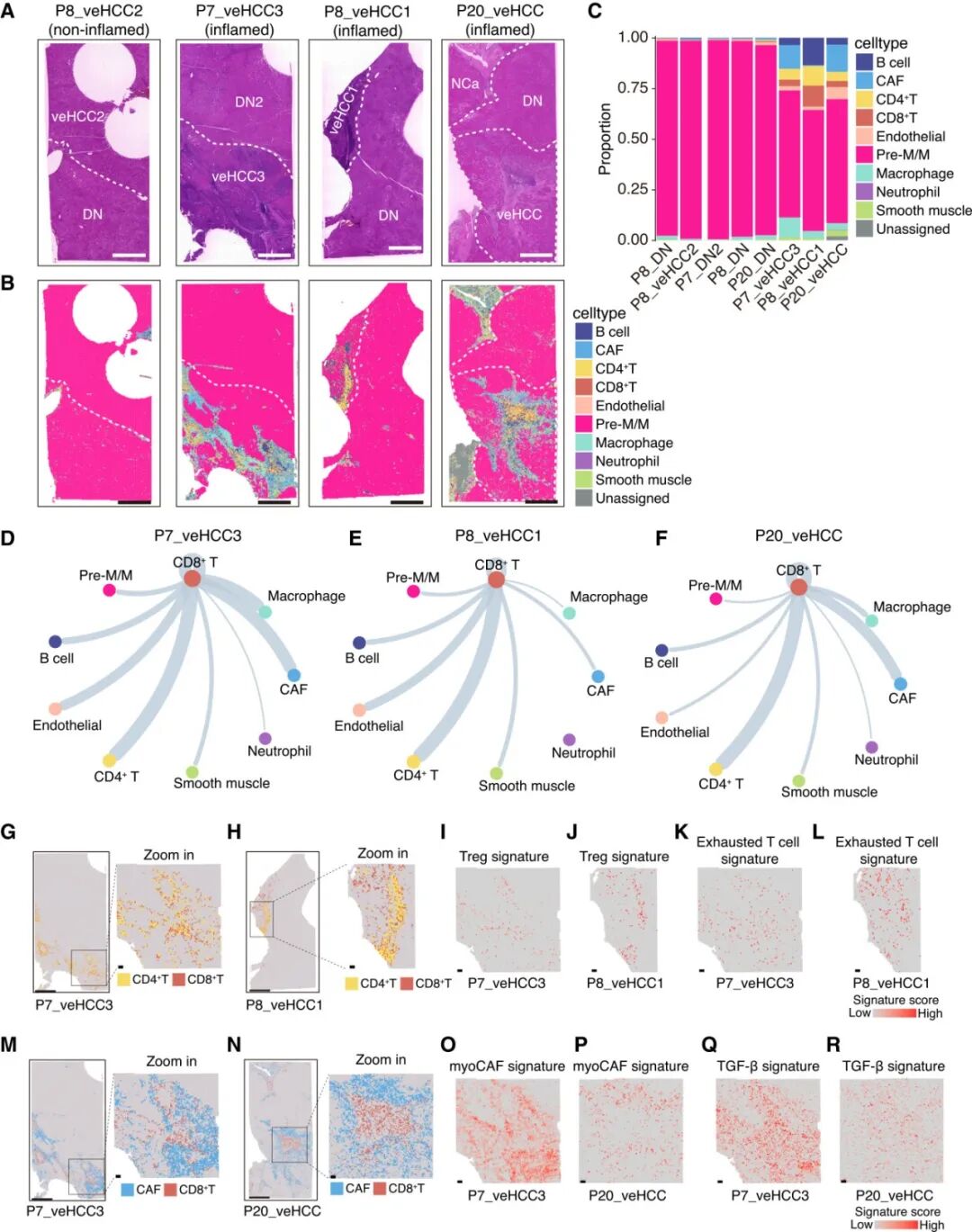
图8 炎症性veHCC中免疫表型的空间定位
六、 恶性转化模式的整合性提出
汇总上述分析结果,TERT变异和免疫反应降低是Cancer-prone DN发展的关键事件(图9A)。基于数据集中的基因组和免疫学特征,作者提出了DN向veHCC恶性转化的两种潜在进化模式:(1)CNA主导的进展(模式1)和(2)伴有免疫逃逸的炎症性进展(模式2)(图9A)。
为了进一步描绘配对DN和veHCC的进化关系,构建了包含影响CFG的SNV和CNA的系统发育树,从而能够注释主干和分支事件。在模式1的所有6个非炎症性veHCC的分支中均检测到CNA诱导的CFG变异(图9B)。在模式2中,炎症性veHCC表现出与其配对DN几乎相同的CNA谱(图9C),这些veHCC中缺乏主要的癌症基因,提示免疫逃逸在这veHCC的恶性转化过程中发挥了潜在作用。
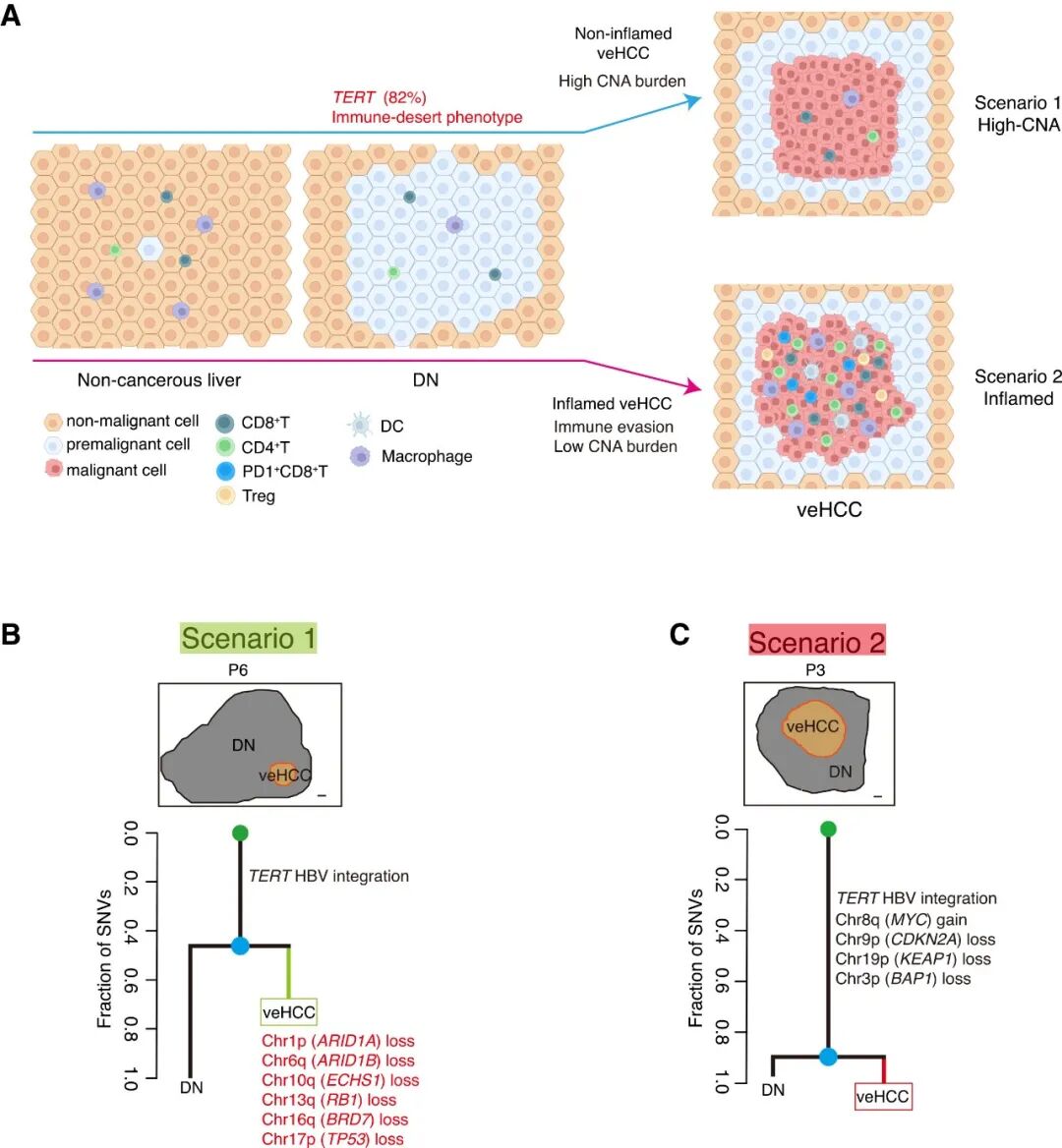
图9 早期HCC恶性转化模式
研究结论
本研究全面解析了极早期肝细胞癌(veHCC)的基因组和免疫学特征:基因组水平上, TERT 突变在恶性转化中可能起易感而非直接驱动作用;拷贝数变异(CNA)的积累,而非单核苷酸变异,与恶性转化密切相关;免疫学特征上,与肝细胞癌发生于慢性炎症环境的传统观点不同,cancer-prone DN表现出免疫非活动性,43%的veHCC表现出炎症性但具免疫逃逸的表型。这些发现提出了早期肝癌发生的两种进化模式:CNA主导的进展和伴有早期免疫逃逸的炎症性进展,强调了免疫疗法在早期干预中的潜力。
参考文献
Zhang Z, Li H, Chen L, Lu T, Shentu X, Liu Y, Tang Z, Ji S, Qiu Z, Zou Y, Wen H, Han J, Jiang Z, Fan J, Gao X, Li D, Mesropian A, Pinyol R, Llovet JM, Dong H, Ji Y, Hui L. Molecular insights into early malignant transition of hepatocellular carcinoma. Cancer Cell. 2026 Mar 26:S1535-6108(26)00157-1. doi: 10.1016/j.ccell.2026.03.005 . Epub ahead of print. PMID: 41895279.






