前言
2026年4月7日,清华大学董家鸿等团队合作在Signal Transduction and Targeted Therapy 在线发表题为“Prostaglandin E2-driven dedifferentiation of Schwann cells leads to perineural invasion in pancreatic ductal adenocarcinoma”的研究论文,该研究通过整转录组测序、空间转录组学以及临床样本的单细胞转录组分析,发现PNI区域中去分化的施旺细胞(Schwann cells,SCs)有显著富集,并且关键标志物(p75NTR、SOX2 和 c-Jun)的表达上调。欧易生物为本研究提供了单细胞时空组学测序及分析服务。

发表期刊:Signal Transduction and Targeted Therapy
影响因子:52.7
涉及的欧易生物服务产品:空间转录组测序;单细胞转录组测序(数据分析)
研究背景
胰腺导管腺癌(PDAC)以神经周围浸润(PNI)为特征病理现象,常伴随疼痛与不良预后。施旺细胞(Schwann cells)作为周围神经的主要胶质细胞,在神经损伤修复中可发生去分化(即从成熟的髓鞘维持状态逆转为不成熟的修复状态)。本研究探讨了前列腺素E2(PGE2)在PDAC中诱导施旺细胞去分化,从而促进PNI的机制。
研究内容
本研究采用多种方法,包括空间转录组与单细胞转录组定位神经侵袭前沿COX-2+施旺细胞,双光子成像验证激活态施旺细胞主动引导癌细胞侵袭;提出"神经-肿瘤共生微环境"概念(Neural-Tumor Symbiosis),首次揭示施旺细胞在PDAC中的"双重角色"——从神经保护者转变为肿瘤侵袭的主动参与者,更新了对PNI机制的理解,同时提出PTGES抑制剂对于PDAC I期临床试验的影响,为后续临床应用提供了治疗靶点;
技术路线
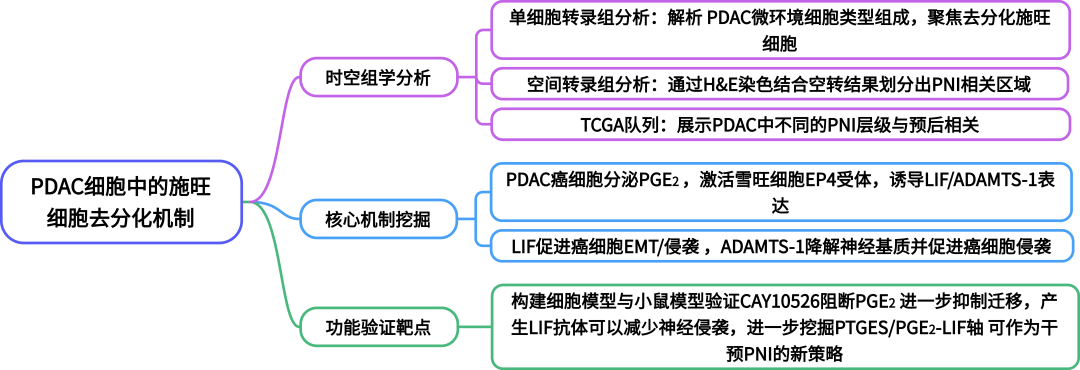
研究结果
Result 1 PDAC中神经周围浸润(PNI)与施旺细胞(SCs)的表型改变相关
作者分析了TCGA-PAAD队列中149例PDAC患者的样本。神经周围浸润(PNI)存在(PNI+)或不存在(PNI-)的分类基于TCGA中可用的手术病理报告和H&E染色图像。PNI−和PNI+病例的Kaplan-Meier(KM)分析显示,PNI状态与总生存期(OS)之间无显著关联(p = 0.56)随后基于H&E染色图像,遵循PNI评分系统对PNI进行定量评分,并相应地将样本分为两个亚组:高PNI组(PNI评分 ≥ 6,n = 48)和低PNI加PNI-组(PNI评分 < 6且无PNI,n = 101)基线特征分析显示,两组间在性别、年龄、病理T/N分期或治疗方式的分布上无统计学显著差异(p > 0.05)。然而,PNI亚分组与转移状态和分子亚型显著相关。具体而言,低PNI加PNI-组主要由经典型PDAC亚型组成,而高PNI组中QM-PDAC亚型的比例更高。KM分析显示,高PNI与较短的总生存期相关。在经典型PDAC亚组中,高PNI亚组的总生存期显著短于低PNI加PNI−组,而在QM-PDAC亚组中未观察到此类差异。按治疗方式分层分析显示:在'无治疗'组中,高PNI组与低PNI加PNI−组之间的生存期无显著差异;在'双重治疗'组(接受放疗和化疗)中亦无显著差异。相比之下,高PNI组中的'单一治疗'组(接受单一放疗或化疗)总生存期显著缩短。基于空间转录组的H&E染色,作者划分了以下区域:PNI区域、PNI邻近区域(PNI-near)、PNI中间区域(PNI-mid)、PNI远区域(PNI-away)、NPNI区域(NPNI)、NPNI邻近区域(NPNI-near)、NPNI中间区域(PNI-mid)(100个点位)以及NPNI远区域(NPNI-away)(图1b)。这些区域的GSVA分析揭示了生物学功能富集的梯度变化。值得注意的是,施旺细胞相关通路(如'轴突导向')从PNI远区域向PNI区域逐渐增强了富集,表明肿瘤微环境中SC的动态改变对PNI至关重要。对7例PDAC患者的14,723个细胞进行单细胞分析,鉴定出11个主要细胞群:成纤维细胞(n = 5359,标记基因:COL1A1, COL1A2, COL3A1)、上皮细胞(n = 5349,EPCAM, KRT18, KRT19)、内皮细胞(n = 1196,CDH5, PECAM1, VWF)、髓系细胞(n = 1089,CD14, CD68, AIF1)、平滑肌细胞(n = 487,ACTA2, TAGLN, SNCG)、浆细胞(n = 461,CD38, XBP1, JCHAIN)、内分泌细胞(n = 245,INS, GCG,SST)、T细胞(n = 325,CD3E, CD3D, CD3G)、腺泡细胞(n = 223,CPA1, SPINK1, PRSS1)、肥大细胞(n = 142,TPSB2, SNCB1, CPA3)和施旺细胞(n = 92,CRYAB, CDH19, SOX10)(图1d,e)。UMAP显示了两个不同的SC亚群。亚群1特异表达无髓鞘施旺细胞marker基因,被定义为:无髓鞘施旺细胞Nomyelinating_SC,同理另一亚群定义为有髓鞘施旺细胞(Myelinating_SC)(图1f,g)。无髓鞘施旺细胞高表达:NGFRAP1、JUND、L1CAM;有髓鞘施旺细胞高表达:ERBB3、PLP1、PMP22。随后通过RCTD反卷积对这些亚群进行空间定位(图1h)。结果显示有髓鞘施旺细胞分布于PNI和NPNI区域,而无髓鞘施旺细胞仅局限于PNI区域(图1i)。作者使用胰腺癌标记物MUC1、神经元标记物PGP9.5以及去分化施旺细胞的高表达marker:p75NTR、SOX2和c-Jun进行了多重免疫组化。结果显示在正常胰腺组织和PNI组织中,SOX2和c-Jun的表达水平较低。相比之下在PNI+组织内,肿瘤包绕的神经纤维呈现SOX2和c-Jun的高表达(图1j,k)。PNI+组织中p75 NTR阳性细胞的比例显著高于PNI-组织,以上结果进一步说明胰腺中施旺细胞的密度可能与PNI的发生相关,去分化施旺细胞与PNI+PDAC的病理状态相关。
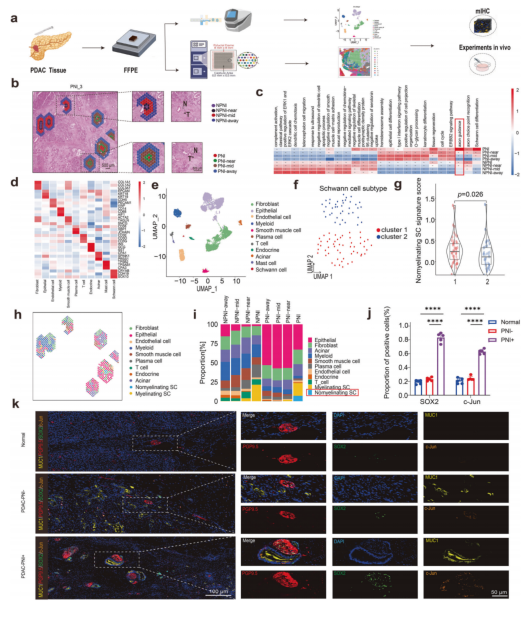
图1.SC在PNI阳性区域富集
Result 2 PNI微环境中的胰腺癌-SC串扰
如前所述,施旺细胞去分化与PNI密切相关。为深入阐明施旺细胞与胰腺癌细胞之间的分子互作机制,作者对与胰腺癌细胞体外共培养后的施旺细胞进行了RNA测序。Venn分析显示,施旺细胞中的差异表达基因显著富集于与'运动蛋白'、'轴突再生'和'细胞周期'等相关的通路中(图2a,b)。这些发现证明,施旺细胞在与胰腺癌细胞共培养后转变为活化、增殖的表型。为验证这一假设,作者使用胰腺癌细胞系(PANC-1和BxPC-3细胞)和施旺细胞系(RSC96和sNF96.2细胞)进行了非接触共培养实验。结果显示,与胰腺癌细胞共培养显著提高了RSC96和sNF96.2细胞的迁移能力(图2c,e,k,m)。在胰腺癌细胞刺激下,RSC96和sNF96.2细胞表现出形态学变化:细胞从具有短而稀疏突起的形态转变为以细长突起为特征的形态,伴随突起数量增加、分枝模式更复杂,甚至通过突起缠结形成网状或束状结构(图2d,l)与这些变化一致的是迁移相关marker:N-钙黏蛋白在RSC96和sNF96.2细胞中显著上调。同时,多种去分化marker(包括p75NTR、c-Jun、SOX2和GDNF)的表达水平也显著升高(图2f-j,n-r)。
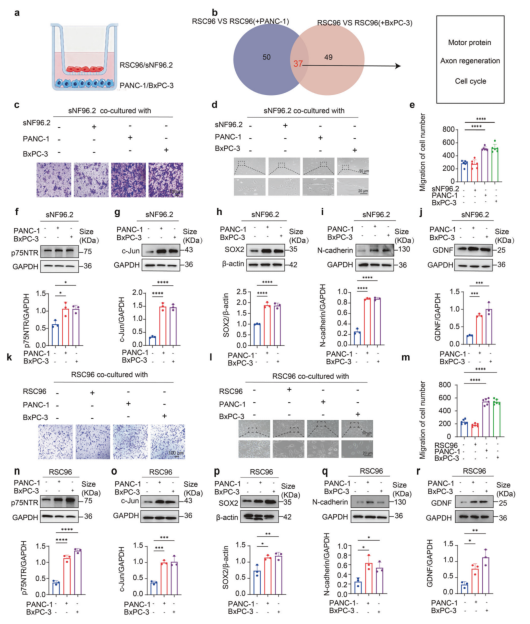
图2. 胰腺癌细胞促进SC去分化
综上,这些发现证明胰腺癌细胞不仅促进施旺细胞的迁移和形态重塑,还诱导参与施旺细胞去分化的核心基因上调。结果表明,施旺细胞显著增强了PANC-1和BxPC-3细胞的迁移、增殖和侵袭能力。为深入阐明PNI中该互作的分子基础,作者通过比较PNI邻近区域与NPNI区域点位的mRNA表达水平,进行了空间转录组基因富集分析。分析显示,神经周围癌细胞在细胞迁移和细胞周期进程相关通路中功能富集(图3a)。此外,EdU掺入实验证实,与施旺细胞共培养后,PANC-1和BxPC-3细胞的增殖活性显著升高(图3c,f)。更重要的是,Western blot分析提供了机制性证据:RSC96和sNF96.2细胞诱导了PANC-1和BxPC-3细胞的上皮-间质转化(EMT)。具体而言,作者在这些胰腺癌细胞中检测到间质marker:N-钙黏蛋白、波形蛋白和SNAI1的蛋白表达上调,同时上皮marker:E-钙黏蛋白表达下调(图3g-v)。
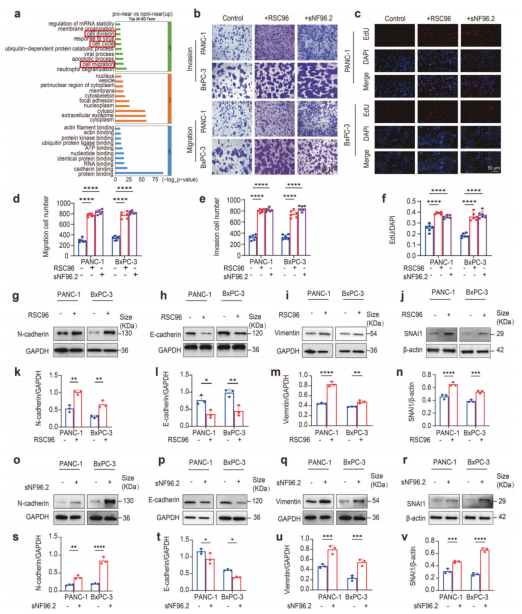
图3. SCs诱导胰腺癌症细胞的恶性进展
Result 3 共培养系统中PTGES/PGE2的升高与神经周围浸润(PNI)相关
为表征PNI背后的旁分泌信号,作者将与RSC96细胞共培养24小时后的胰腺癌细胞收集并进行RNA-seq分析。为更全面研究,作者进一步整合了另两个独立来源的RNA-seq数据集:9例经确认的PNI临床PDAC样本,以及从GEO数据库(GSE102238)获取的28例PNI+与28例PNI-样本的转录组数据。作者随后通过Venn分析鉴定了这三个数据集的交集基因。其中六个蛋白编码基因——NUF2、NEK2、MELK、C1GALT1、ADGRF1和PTGES——在PNI+样本中显著上调(图4a)。这些基因中,NUF2、NEK2和MELK主要参与细胞增殖过程(包括细胞周期进程和有丝分裂),表明它们可能驱动肿瘤细胞快速分裂。值得注意的是,根据空间转录组结果,虽然C1GALT1和ADGRF1在PNI与NPNI区域的表达水平相当,但PTGES在肿瘤区域呈现特异表达,并在PNI区域特异性富集,而在NPNI区域的表达可忽略不计(图4b,c)。这种独特的表达pattern进一步证实了PTGES与PNI的关联性。综上所述PTGES(前列腺素E合成酶基因)被确定为本研究的关键候选基因。PGE2在施旺细胞(SC)介导的神经发生、轴突修复和神经再生中起重要作用。在肿瘤研究中,焦点主要集中在肿瘤源性PGE2对免疫细胞的调控,但PGE2在SC重编程中的作用及其促进PNI的机制仍不明确。mIHC分析显示正常组织中无MUC1或PTGES表达。在PNI-和PNI+组织中观察到了PTGES与MUC1共定位,但与PGP9.5无共定位。相反,p75NTR与PGP9.5共定位而不与MUC1共定位,证实了p75NTR和PTGES的表达特异性(图4d)。IHC分析进一步显示,正常组织和PDAC-PNI-组织中的PTGES H-score低于PDAC-PNI+组织(图4e,l)。Western blot结果进一步证实:PTGES在PDAC组织中过表达,且PANC-1/BxPC-3细胞与施旺细胞的相互作用增加了前列腺素合成酶PTGES的表达水平(图4f-k)。与这些发现一致,通过ELISA检测的共培养系统中PGE2水平显著升高,而该效应可被PTGES抑制剂(CAY10526)或siPTGES敲低所减弱(图4m)。总之,高PTGES/PGE2表达与PDAC的PNI相关。抑制胰腺癌细胞中的PTGES可降低共培养系统中PGE2的含量。
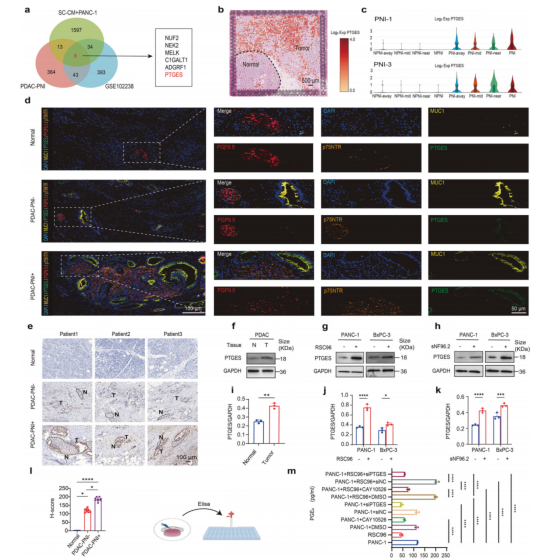
图4. 共培养系统中PTGES/PGE2的升高与PNI相关
Result 4 胰腺癌来源PGE2诱导SC活化
细胞免疫荧光(Cellular IF)进一步证实了膜标记物Dil与PGE2受体PTGER1、PTGER2和PTGER4在RSC96及sNF96.2细胞中的共定位(图5a)。为探究PTGES/PGE2诱导SC去分化的潜在作用,用梯度浓度PGE2处理施旺细胞。孵育24小时后,通过phalloidin染色结合共聚焦激光扫描显微镜评估细胞形态学变化。结果显示PGE2处理引发施旺细胞显著形态学改变:原本细长的RSC96和sNF96.2细胞发生表型转换,呈现出去分化状态的典型纺锤形和双极特征(图5b)。蛋白质免疫印迹分析显示,RSC96和sNF96.2细胞中p75NTR、c-Jun和SOX2的蛋白表达水平呈PGE2浓度依赖性升高(图5c、e-g)。此外,细胞免疫荧光检测表明PGE2处理后,两种细胞系中p75NTR、c-Jun和SOX2的相对荧光强度均显著增加(图5d、h-j)。值得注意的是,用CAY10526预处理胰腺癌细胞可削弱其在共培养系统中诱导施旺细胞迁移的能力。3D细胞迁移实验证实RSC96和sNF96.2细胞迁移能力增强,同时获得细长形态表型。关键的是,该促迁移效应未被非恶性HPNE细胞引发。相反,CAY10526或siPTGES处理显著损害施旺细胞向胰腺癌细胞的定向迁移(图5m)。背根神经节(DRG)外植体与胰腺癌细胞共培养显示,CAY10526或siPTGES处理显著抑制DRG轴突生长,生长指数明显降低(p < 0.01)(图5n、u-v)。为明确PTGES/PGE2调控通路的特异性,本研究选用高表达PTGES的胰腺癌细胞系BxPC-3作为对象。利用基因编辑技术构建PTGES基因敲除的BxPC-3细胞系,并重复前述实验流程。实验结果与前期结果一致。综上,这些发现表明胰腺癌来源的PGE2对促进施旺细胞活化和迁移至关重要,而阻断胰腺癌细胞中PTGES功能可削弱施旺细胞的去分化能力。
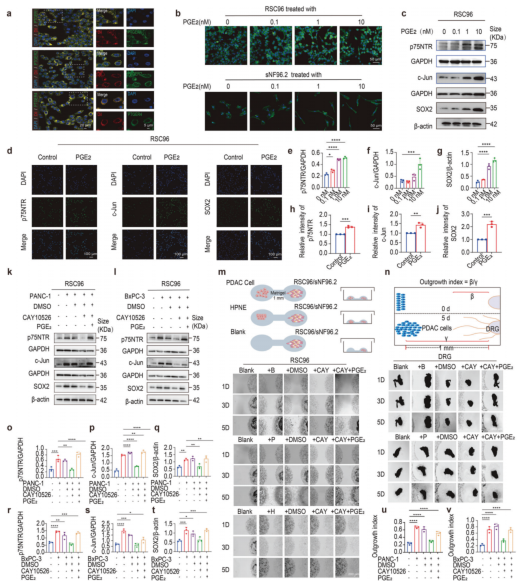
图5. 胰腺癌来源PGE2诱导SC活化
Result 5 去分化的SC分泌LIF和ADAMTS-1以促进PNI
为了揭示PGE2促进神经周围浸润(PNI)的机制,用PGE2(10 nM)处理RSC96细胞24小时后进行RNA-seq分析。与胰腺癌细胞共培养后,RSC96细胞的转录组呈现差异表达。Venn结果显示,白血病抑制因子LIF(|log2FC| =1.12, p < 0.001)和含血小板反应蛋白基序1的去整合素金属蛋白酶ADAMTS-1(|log2FC| =1.67, p < 0.001)在处理组中显著上调(图6a)。RT-qPCR显示,胰腺癌细胞和PGE2可上调RSC96及sNF96.2细胞的LIF表达水平(图6b-e)。Western blot分析证实,胰腺癌细胞和PGE2处理使施旺细胞(SCs)中ADAMTS-1蛋白表达增加(图6f-i,l-o)。CAY10526或siPTGES预处理可降低RSC96和sNF96.2细胞中ADAMTS-1蛋白表达水平,而该效应可被PGE2逆转(图6j、k、p、q)。CAY10526处理或siPTGES敲低降低sNF96.2细胞中LIF 表达,该效应可被PGE2逆转。LIF中和抗体(AB-449-NA)处理降低共培养系统中的轴突生长指数(图6r,u),并减少侵袭神经的胰腺癌细胞数量(图6s、t、v、w)。使用PTGES-KO BxPC-3细胞,作者证实施旺细胞中ADAMTS-1和LIF的诱导需要癌细胞中功能性PTGES。小鼠模型实验中,经施旺细胞预处理的胰腺癌细胞形成更重的肿瘤并导致更差的坐骨神经功能评分。CAY10526或AB-449-NA处理显著降低肿瘤重量并改善坐骨神经评分(补充图6n-q)。透射电子显微镜(TEM)显示肿瘤神经侵袭导致髓鞘损伤,表现为严重脱髓鞘(补充图6r)。施加CAY10526或AB-449-NA可改善该脱髓鞘现象。总之,PGE2诱导施旺细胞分泌营养因子LIF并降解细胞外基质,从而促进神经侵袭(图6x)。
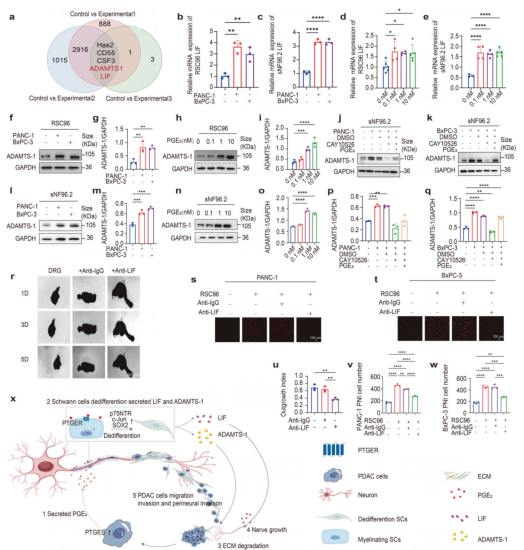
图6. PGE2促进SC分泌LIF和ADAMTS-1以驱动PNI的发展
研究总结
本研究指出胰腺导管腺癌(PDAC)通过PTGES/PGE2信号轴驱动施旺细胞去分化,激活其PTGER受体并上调p75NTR/c-Jun/SOX2核心通路。去分化施旺细胞分泌白血病抑制因子(LIF)及基质降解酶ADAMTS-1,形成"癌细胞-PGE2-施旺细胞-LIF"级联反应:LIF促进癌细胞迁移侵袭及上皮-间质转化(EMT),ADAMTS-1降解神经周基质,二者协同介导肿瘤沿神经侵袭。靶向干预实验证实,PTGES抑制剂(CAY10526)或LIF中和抗体(AB-449-NA)可显著阻断施旺细胞去分化,减轻神经髓鞘损伤,抑制动物模型中肿瘤神经浸润并改善坐骨神经功能。该研究揭示PTGES/PGE2-LIF轴是PDAC神经周围侵袭(PNI)的关键驱动机制,为临床干预提供新靶点。
原文链接
Wang, L., Liu, Q., Zhang, Z. et al. Prostaglandin E2-driven dedifferentiation of Schwann cells leads to perineural invasion in pancreatic ductal adenocarcinoma. Sig Transduct Target Ther 11, 122 (2026).
欧易生物单细胞时空多组学协助客户转化文章500+篇,其中CNS主刊9篇,年处理单细胞样本数量达30000例,累计完成单细胞项目超10000个。






